Биология клетки/Часть 1. Клетка как она есть/2/11
| ← Предыдущая глава | Глава 2.11 | Следующая глава → |
| Химический состав живого: молекулы | ||

Вода в активных клетках составляет обычно 75-85 % по массе. Воды меньше в клетках жировой ткани (около 40 %), ещё меньше может быть в клетках покоящихся стадий (в семенах растений 5-15 % воды). Как в клетке, так и в целом в биосфере Земли вода выполняет важнейшие функции, связанные с ее уникальными свойствами. Свойства эти, в свою очередь, зависят от строения молекул воды.
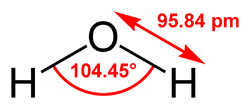
Молекула воды состоит из одного атома кислорода и присоединенных к нему двух атомов водорода. Связь между ними — ковалентная полярная. Электронная плотность сильно смещена в сторону кислорода, так как он имеет высокую электроотрицательность. Так как химические связи расположены в молекуле воды под углом, на одном полюсе (к которому ближе атомы водорода) сосредотачивается частичный положительный заряд, на другом (там, где находится атом кислорода) — частичный отрицательный заряд. Таким образом, молекула воды представляет собой электрический диполь.
В воде присутствуют межмолекулярные водородные связи
[править]Между молекулами воды образуются водородные связи, причём каждая молекула воды может образовать такие связи, в первом приближении, с четырьмя «соседними».
В жидкой воде молекулы хаотически движутся, и «соседство» это непостоянное; подробнее о структуре жидкой воды см. [1].

Во льду каждая молекула образует связи ровно с четырьмя соседними. Тем не менее, обычный природный лёд имеет гексагональную кристаллическую решётку, причём молекулы в ней упакованы менее плотно, чем в жидкой воде.
Водородные связи определяют уникальные свойства воды
[править]У воды очень высокие температуры кипения, плавления и парообразования, так как нужно затратить дополнительную энергию на разрыв водородных связей. Только вода в обычных земных условиях находится во всех трех агрегатных состояниях одновременно. Другие вещества со сходным строением и молекулярной массой, такие как H2S, HCl, NH3 при обычных условиях являются газами.
По их отношению к воде все вещества делятся на гидрофильные и гидрофобные
[править]
Все вещества по отношению их к воде в первом приближении делятся на гидрофильные и гидрофобные. Гидрофильные («любящие воду») вещества обычно имеют полярные молекулы (или кристаллические решетки с ионными связями).
Многие гидрофильные вещества хорошо растворяются в воде (а если это жидкости — то смешиваются с ней в любых соотношениях). К гидрофильным веществам можно отнести поваренную соль NaCl, аммиак NH3, спирт C2H5OH.
Но многие гидрофильные вещества нерастворимы. Тогда их поверхность хорошо смачивается водой. К таким веществам относится, например, шерсть (состоящая из белка кератина), бумага (состоящая из целлюлозы) и др.
Гидрофобные («боящиеся воды») вещества плохо растворяются в воде, не смачиваются ею (а если это жидкости — то не смешиваются с ней).
- Вопрос 1
- Почему вещества с полярными молекулами и ионной кристаллической решеткой гидрофильны, а вещества с неполярными молекулами гидрофобны?
- Вопрос 2
- Почему некоторые гидрофильные вещества растворимы в воде, а другие — нет?
Гидрофильность и гидрофобность — частный случай лиофильности и лиофобности. Кроме гидрофильности, можно говорить про липофильность (олеофильность) и др.
Задача 1
Мениск — поверхность воды, налитой, например. в пробирку. Какую форму — вогнутую или выпуклую — будет иметь мениск, если налить воду в пробирку из гидрофильного материала? гидрофобного материала? Объясните, почему.
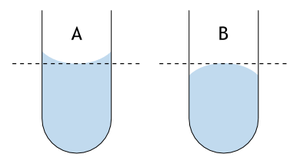
B: Выпуклый мениск.
Некоторые органические вещества амфифильны
[править]
Амфифильность — свойство молекул, одна часть которых гидрофильна, а другая гидрофобна. К амфифильным веществам относятся фосфолипиды, жирные кислоты и их соли (например, мыло), а также липопротеиды и др.. Белки также обладают амфифильными свойствами, так как обычно в их состав входят аминокислоты с гидрофильными и с гидрофобными радикалами.
За счет амфифильных свойств фосфолипидов при взаимодействии с водой они формируют мицеллы, липосомы и липидные бислои (см. Взаимодействие фосфолипидов с водой)..
Амфифильность белков влияет на образуемые ими третичные и четвертичные структуры молекул, а также позволяет молекулам мембранных белков встраиваться в клеточные мембраны.
Вода — полярный растворитель
[править]Вода хорошо растворяет полярные, или гидрофильные вещества — например, растворимые соли, аминокислоты, сахара. Молекулы воды окружают ионы или молекулы вещества, отделяя тем самым частицы друг от друга. Следовательно, в растворе молекулы (или ионы) смогут двигаться более свободно, а значит, быстрее будут протекать химические реакции. Гидрофобные вещества не будут растворяться в воде, зато молекулы H2O, притягиваясь друг к другу, смогут отделить гидрофобное вещество от самой толщи воды. Например, фосфолипиды, из которых состоит клеточная мембрана, могут благодаря взаимодействию с водой формировать липидный бислой.
Вода выполняет разнообразные функции в клетке и в организме
[править]Вода — полярный растворитель (см.выше)
Вода — реагент
Вода в качестве реагента участвует во многих химических реакциях:
- В ходе фотосинтеза у растений происходит фотолиз воды — водород из состава воды входит в органические вещества, а свободный кислород выделяется в атмосферу.
Уравнение фотосинтеза:
- Вода участвует в гидролизе — разрушении веществ с присоединением воды. Например, гидролиз жиров, белков и углеводов происходит при переваривании пищи, а при гидролизе АТФ выделяется энергия, обеспечивающая нужда клетки.
- При гидролизе солей вода является источником протонов и электронов.
Вода поддерживает форму клеток
Вода практически несжимаема (в жидком состоянии), и поэтому служит гидростатическим скелетом клетки. За счет осмоса вода создает избыточное давление внутри вакуолей растительных клеток. это тургорное давление обеспечивает упругость клеточной стенки и поддержание формы органов (например, листьев).
Вода обеспечивает транспорт веществ у растений и животных
- У растений, благодаря, в частности, капиллярному эффекту, осуществляется всасывание из почвы раствора минеральных солей и их подъем от корня к другим частям растения по сосудам. Транспорт продуктов фотосинтеза происходит посредством перемещения по ситовидным трубкам водного раствора сахарозы.
- Вода обеспечивает транспорт питательных веществ и выведение из организма в растворенном виде продуктов обмена веществ у животных (вода — основной компонент плазмы крови и лимфы), а также играет важную роль в работе выделительной системы.
Вода участвует в терморегуляции
Вследствие своей большой теплоемкости — 4200 Дж/(кг x К) — вода обеспечивает примерное постоянство температуры внутри клетки. Вода может переносить большое количество теплоты, отдавая ее там, где температура тканей ниже, и забирая там, где температура более высокая. Также при испарении воды происходит значительное охлаждение из-за того, что много энергии тратится на разрыв водородных связей при переходе из жидкого состояния в газообразное. Испарение жидкости — единственный способ, который позволяет теплокровным поддерживать постоянную температуру, когда температура окружающей среды становится выше температуры тела.
Полезные книги и статьи по теме:
- [2] М. А. Констаниновский. Почему вода мокрая. (По этой ссылке можно скачать книгу в формате djvu). Простым и понятным языком описываются основные свойства воды.
- [3]Вода знакомая и загадочная. Леонид Кульский, Воля Даль, Людмила Ленчина
(наряду с полезными сведениями книга содержит изложение непроверенных и неподтвержденных гипотез об «активированной» воде!)
- [4]Water Structure and Science (англ.) — достаточно сложная научная книга о воде
- Hydrophobe — Статья о гидрофобности и сверхгидрофобности из англоязычной Википедии
- [5] Анимация "Свойства воды " (англ. текст)
Неорганические вещества. Функции ионов
[править]Калий — один из главных биогенных элементов, необходимых для роста растений. При его недостатке в почве резко падает урожайность, поэтому главное использование калия человеком — производство минеральных удобрений. В организме калий находится в виде катионов в основном в цитоплазме (у животных его концентрация в цитоплазме примерно в 40 раз выше, чем в крови), у растений также в клеточном соке вакуолей.
Кальций — распространенный макроэлемент в организме растений, животных и человека. В организме человека и других позвоночных большая его часть содержится в скелете и зубах в виде фосфатов. Из различных форм карбоната кальция (извести) состоят скелеты большинства групп беспозвоночных (губки, коралловые полипы, моллюски и др.). Ионы кальция участвуют в процессах свёртывания крови, а также в обеспечении постоянного осмотического давления крови. Ионы кальция также служат одним из универсальных вторичных посредников и регулируют самые разные внутриклеточные процессы — мышечное сокращение, экзоцитоз, в том числе секрецию гормонов и нейромедиаторов и др. Концентрация ионов кальция в цитоплазме клеток человека составляет около 10−7 моль, в межклеточных жидкостях около 10−3 моль.
Фосфор, как и кальций, в организме позвоночных в наибольшем количестве содержится в составе минеральных солей скелетных тканей. Скелет позвоночных состоит в основном из гидроксиапатита (его эмпирическая формула — Ca5(PO4)3(OH))
Внутриклеточная и внеклеточные концентрации некоторых ионов (внутриклеточные концентрации указаны для мышечной клетки теплокровного животного), ммоль/л
| Ион | Внутриклеточная концентрация | Внеклеточная концентрация |
|---|---|---|
| Na+ | 12 | 145 |
| K+ | 155 | 4 |
| Cl- | 4 | 110 |
| HCO3 - | 8 | 27 |
| Ca2+ | 10−4 | 2 |
| Фосфат-ионы | 2 | 2 |
| Анионы органических соединений | 155 | - |
[6] И. С. Кулаев Неорганические полифосфаты и их роль на разных этапах клеточной эволюции. Сросовский образовательный журнал, 1006, N 2, с.28-35
Органические вещества, органические соединения — класс соединений, в состав которых входит углерод (за исключением карбидов, карбонатов, оксидов углерода и цианидов).
Название органические соединения появилось на ранней стадии развития химии во время господства виталистических воззрений. Вещества при этом разделялись на минеральные — принадлежащие царству минералов, и органические — принадлежащие царствам животных и растений. Считалось, что для синтеза органических веществ необходима особая «жизненная сила», присущая только живому, и поэтому синтез органических веществ из неорганических невозможен. Это представление было опровергнуто Фридрихом Вёлером в 1824 году путём синтеза «органической» мочевины из «минерального» цианата аммония, однако деление веществ на органические и неорганические сохранилось в химической терминологии и по сей день.
Количество известных органических соединений давно перевалило за 10 млн. Таким образом, органические соединения — самый обширный класс веществ. Многообразие органических соединений связано с уникальным свойством углерода образовывать цепочки из атомов углерода, что в свою очередь обусловлено высокой стабильностью (то есть энергией) углерод-углеродной связи. Связь углерод-углерод может быть как одинарной, так и кратной — двойной или тройной. При увеличении кратности углерод-углеродной связи возрастает её энергия, то есть стабильность, а длина уменьшается. Высокая валентность углерода — 4, а также возможность образовывать кратные связи позволяет атомам углерода, содединяясь в молекулы, образовывать структуры различной размерности (линейные, плоские, объёмные).
Различная топология образования связей между атомами, образующими органические соединения (прежде всего, атомами углерода), приводит к появлению изомеров — соединений, имеющих один и тот же состав и молекулярную массу, но обладающих разной структурой и потому различными физико-химическими свойствами. Данное явление носит название изомерии.
Большинство органических веществ горючи, а при нагревании обугливаются.
