Координационная химия
Введение
[править]Наблюдаемый мир является лишь "фотографией", застывшей конфигурацией разлетающейся с ускорением материи Вселенной, на фоне огромного количества времени, на протяжении которого Вселенная эволюционирует. Человеческая жизнь, а может и само существования человечества - это лишь какой-то миг. Законы, по которым функционирует материя, позволяют ей комбинироваться, конфигурироваться, благодаря чему образуются наблюдаемые структуры. С созданием квантовой хромодинамики появилась надежда на построение единой теории фундаментальных взаимодействий. Модели, которые содержат все известные типы взаимодействий (сильное, слабое, электромагнитное и гравитационное) называются моделями супергравитации. Объединение электромагнитного и слабого взаимодействий благодаря идее калибровочных полей указало на возможные пути дальнейшего развития принципа единства физики, объединения фундаментальных физически взаимодействий. Идея супергравитации основывается на идеях суперматематики (в частности, суперсимметрии). Фермионы считаются носителями субстрата материи, а бозоны - носителями её структуры (переносчики взаимодействий).
В простейшем варианте теории большого объединения для преобразования кварков в лептоны нужно двадцать четыре поля. Двенадцать из квантов этих полей уже известны: фотон, две W-частицы, Z-частица и восемь глюонов. Другие двенадцать квантов - новые сверхтежелые промежуточные бозоны, объединенные общим названием X- и Y-частиц (имеют цвет и электрический заряд). Эти кванты соответствуют полям, поддерживающим большую калибровочную симметрию и перемешивающим кварки с лептонами. Соответственно X- и Y-частицы могут преобразовывать кварки в лептоны (и наоборот).
Мы же рассмотрим материю более общо. В 1913 году Нильс Бор применил идею квантования к теории строения атома, над которой работал Е.Резерфорд. Согласно классической электродинамике, электрон не может стойко излучать электромагнитные волны и утрачивать энергию. Значит, радиус его орбиты должен уменьшаться, и за короткое время порядка 10-8 с он должен упасть на ядро. Это значит, что законы классической физики нельзя применять к движению электронов в атоме.
Лекция 1
[править]Для описания строения химических систем используются два вида симметрий.
- Группы симметрии кристаллов (пространственные группы) используются для описания строения твердых тел с упорядоченной структурой, изучаемые кристаллохимией и квантовой химией твердого тела.
- Группы симметрии молекул (точечные группы) являются основой для классификации молекулярных структур, их электронных состояний и для исследования связанных с ними свойств. Точечными группы названы потому, что при всех действиях с молекулой по крайней мере точка остается неподвижной.
Элементы симметрии - это воображаемые точки, линии или плоскости в тех объектах, которые рассматриваются. К элементам симметрии принадлежат: плоскости, центр оси и т.д. Оси симметрии имеют разный порядок, то есть количество отображений в себя при вращении на 360 градусов. Случаются и более сложные элементы симметрии - зеркально-поворотные оси симметрии (отображение в себя при повороте на определенный угол вокруг этой оси и отображение на плоскости, перпендикулярной оси поворота).
Операция симметрии - это действие над объектом, которое переводит его в совмещение с самим собой. К операциям симметрии принадлежат:
- вращение
- отображение в плоскости ;
- несобственное вращение то ест вращение с одновременным отображением в плоскости, перпендикулярной оси вращения.
Операцию можно представить как произведение двух операций:
Между операциями симметрии существует связь. Операции вращения допускают наличие осей симметрии, операции отображения связаны с наличием плоскостей симметрии, а операция возможна при зеркально-поворотных осях определенного порядка.
Лекция 2
[править]При определении симметрии молекулы рассматривают как наборы атомов с фиксированными координатами (заряд и распределение электронной плотности не рассматриваются). Точечные операции симметрии - это действия над молекулой, переводящие ее в положение, неотличимое от исходного. Это значит, что в результате применения операций симметрии ни один из атомов не попадает в точку с координатами, не включенными в исходный набор, и в каждой точке с координатами оказывается или атом номер либо атом этого же химического элемента.
Эквивалентными атомами являются атомы одного и того же химического элемента, которые меняются местами благодаря действиям операций симметрии.
Единичный элемент (идемпотент) в точечной группе - тождественное преобразование, в результате которого система возвращается в исходное положение, или с системой вообще не производится никаких действий.
Умножение в точечной группе - последовательное выполнение двух операций, причем первой выполняется операция, стоящая справа .
Для точечных групп используют обозначения Шенфлиса, а для пространственных групп - систему обозначений Германа-Могена, которая предусматривает включение трансляционной симметрии.
Аксиомы групп
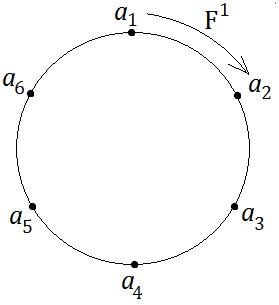
[править]Каждая математическая наука изучает множества, на которых введены определенные отношения (предикаты) и операции В случае, если на множестве введены лишь отношения, то такое множество называется реляционной системой (или моделью). Пусть множество состоит из точек образующих вершины правильного шестиугольника. Введём операцию полагая, что и Алгебра не имеет подалгебр, отличных от неё, поскольку производя операцию над произвольной точкой а затем, беря получим все 6 точек.
Группой называется множество объектов или операций (элементов группы), которые обладают следующими свойствами: 1. Для этого множества определен "закон умножения", то есть закон, по которому любым двум элементам взятым в определенном порядке, единственным образом ставится в соответствие элемент такой, что При этом если для всех то группа называется коммутативной (или абелевой). 2. Умножение ассоциативно: для всех 3. Среди элементов имеется единичный элемент такой, что для всех
Примером группы является множество состоящее из двух элементов - чисел 1 и -1, а вместе с ними и операцией умножения Таким образом, система образует группу, для которой справедлива следующая таблица умножения.
| 1 | -1 | |
| 1 | 1 | -1 |
| -1 | -1 | 1 |
Единицей этой группы является число
Для множества с определенной на нем операции умножения, т.е. системы справедлива следующая таблица умножения.
| 1 | -1 | i | -i | |
| 1 | 1 | -1 | i | -i |
| -1 | -1 | 1 | -i | i |
| i | i | -i | -1 | 1 |
| -i | -i | i | 1 | -1 |
Выделенные группы называются циклическими. Группа, проектирующаяся на бесконечную циклическую группу, называется индикабельной.
Подгруппа группы называется изолированной, если Изолятором подгруппы в группе называется наименьшая изолированная подгруппа группы содержащая
Если подмножество частично упорядоченного множества то - частично упорядоченное множество относительно индуцированного порядка где для если в
-группой называется непустое множество с бинарной операцией и бинарным отношением такими, что система является группой, а - частично упорядоченным множеством, причем
Группа является частично левоупорядоченной, если на ней задан частичный порядок и верно
-группой называется группа являющаяся одновременно частично правоупорядоченной и левоупорядоченной относительно некоторого частичного порядка. Группа является правоупорядочиваемой, если она изоморфно вложима в группу автоморфизмов подходящего линейного упорядоченного множества. Класс правоупорядочиваемых групп совпадает с классом групп изоморфно вложимых в решеточно упорядоченные группы.
Если на действует группа операторов то частичный порядок на называется -порядок, если для любых и отношение влечет неравенство Через обозначен образ элемента под действием оператора
Частично упорядоченная группа является:
- связной, если порядок является связным частично упорядоченным множеством
- направленной, если порядок - направленное множество
- решеточно упорядоченной (-группой, если порядок является решеткой)
- линейно упорядоченной (-группой), если порядок является линейно упорядоченным множеством.
Любая -группа является алгебраической системой сигнатуры где - точная верхняя грань, - точная нижняя грань элементов
Лекция 3
[править]Геометрическое строение молекулы определяется координатами ее атомов. Например, в декартовой системы координат:
| Атом 1: | |||
| Атом 2: | |||
| ... | ... | ... | ... |
| Атом n: |
Такой способ позволяет фиксировать направления осей для каждого атома. При применении точечных операций симметрии по крайней мере одна точка должна оставаться неподвижной, все оси и плоскости симметрии должны пересекаться в этой точке, которую принято выбирать в качестве начала координат.
Например, геометрическое строение молекул воды определяется следующими координатами:
| 0 | 0 | 0 | |
| 0 | 0,76 | 0,59 | |
| 0 | -0,76 | 0,59 |
- Группа квадратных матриц , на которую гомоморфна данная группа называется представлением
- Число строк или столбцов называется размерностью представления.
- Набор функций с помощью которых построены матрицы называется базисом представления (функции преобразуются по представлению )
- Если все матрицы представления различны, представление изоморфно группе; такое представление называется точным.
В качестве базиса могут быть орбитали (атомные, гибридные, молекулярные и т.д.), многоэлектронные волновые функции, естественные и нормальные колебательные координаты и другие наборы функций.
Действие операции симметрии точечной группы молекулы на каждую из ее функций представляется в виде линейных комбинаций:
Коєффициенты записываются в матрицу преобразования для этой операции. Таким образом, в заданном базисе каждой операции симметрии группы сопоставляется квадратная матрица размерности описывающая преобразование базисных функций под действием данной операции. Совокупность таких матриц для всех элементов точечной группы образует представление точечной группы.
Если представление построено в базисе размерности а представление построено в базисе полученное путем линейного преобразования исходного базиса
или, в общем виде,
то такие представления и называются эквивалентными. Преобразование представления к любому эквивалентному называется подобным преобразованием:
Характер операции обозначается в представлении - это сумма диагональных элементов матрицы
Характер представления - это совокупность характеров операций для данного представления. Свойства характеров:
1. Характер операции равен размерности базиса 2. Характер операции, принадлежащих одному классу, совпадают. 3. Эквивалентные представления имеют одинаковые характеры. 4. Если матрицы представления можно составить из матриц представлений меньшей размерности, расположив их вдоль диагонали (прямая сумма), то для каждой операции имеет место
Лекция 4
[править]Под воздействием операций симметрии атомы молекулы перемещаются в пространстве.
Пусть начальные координаты преобразование к новым координатам осуществляется посредством линейного преобразования:
которое можно представить квадратной матрицей с элементами
Эта матрица называется матрицей преобразования. Коэффициенты удовлетворяют условию (правило Кронеккера):
и определитель, равен +1.
На плоскости выделяют следующие два рода движения.
1. Движение первого рода не выводит с плоскости и не изменяет ориентации фигур (параллельный перенос или вращение).
2. Движение второго рода, которое выводит из плоскости (обращение плоскости в пространстве) и изменяет ориентацию фигуры (симметрия относительно прямой с последующим переносом или вращением).
В случае поворота на угол по часовой стрелке матрица преобразования имеет вид
Эта матрица является частным случаем матрицы преобразования координат, элементы которой выражены через углы Эйлера: Для этой матрицы
или
Установление точечной группы позволяет решить вопрос о наличии или отсутствии у нее оптических изомеров.
Хиральность - это свойство объекта быть несовместимым со своим отображением в идеальном плоском зеркале.
В трёхмерном пространстве любая фигура, обладающая плоскостью симметрии или центром симметрии ахиральна. Однако, существуют ахиральные фигуры, не обладающие ни центром, ни плоскостью симметрии, например:
Эта фигура инвариантна относительно меняющего ориентацию преобразования и поэтому ахиральна, но не обладает ни плоскостью, ни центром симметрии. Фигура
также ахиральна, так как начало координат является для неё центром симметрии, но у неё нет плоскости симметрии.
Общим математическим условием хиральности является отсутствие у молекулы зеркально-поворотных осей симметрии В частном случае, поскольку наличие элементов и также говорит об отсутствии у молекулы оптических изомеров.
Молекула, которая не имеет собственной оси вращения, называется дисимметричной (асимметричная молекула вообще не имеет никаких элементов симметрии). Оптически активные молекулы должны быть дисимметричны, они принадлежат точечным группам, имеющим в качестве элементов симметрии только простые поворотные оси.
Вместе с конфигурацией и конформацией хиральность относится к основным понятиям стереохимии. Энантиомерами, или оптическими изомерами, называют пары оптических антиподов. Такие изомеры характеризуются противоположными по знаку и одинаковым по величине вращениями плоскости поляризации света.
Лекция 5
[править]Операции вращения Индекс указывает на количество совмещений объекта с самим собой при вращении на 360 градусов. Угол называют элементарным углом вращения. Например, равносторонний треугольник вращается на градусов, совмещаясь сам с собой. Таким образом элементарный угол для для для и так далее. Индекс обозначает количество поворотов на элементарный угол: означает поворот на 120 градусов, - поворот на 180, - на 360 градусов. Операция тождественна с операцией покоя, которая обозначается
Операции отображения дополняются индексами то есть Операция - это отображение в горизонтальной плоскости, то есть в плоскости, перпендикулярной к оси симметрии высшего порядка. Плоскости отображения для операции проходят через ось симметрии вертикально. Операция - это отображение в вертикальных плоскостях симметрии, которые проходят через биссектрисы координатной плоскости
Операции несобственного вращения являются "произведением" двух операций симметрии: и Иногда они имеют специальные обозначения. Например, операцию обозначают символом и называют инверсией:
При наличии оси второго порядка и перпендикулярной ей плоскости в теле можно обнаружить точку, где все линии, которые через неё проходят, соединяют эквивалентные точки фигуры. Такая точка называется центром инверсии, или центром симметрии. Центр инверсии находится посередине отрезков, которые соединяют эквивалентные точки фигуры. В молекуле инверсия каждого атома через центр симметрии приводит к совмещению его с таким же атомом.
Например, для ромбической пирамиды () известно четыре симметрии: - спокойствие, - вращение на 180, и - отображения в плоскостях. При всех операциях на месте остается высота пирамиды (общее условие - чтобы при любой операции оставалась неподвижной хотя бы одна точка). Между тем, как ромбическая пирамида, так и треугольник - это фиксированное расстояние между точками, следовательно, можно также "дёргать" и растягивать стороны.
Количество операций симметрии для данной молекулы называется числом симметрии. Например, молекула воды (точечная группа ) имеет четыре операции симметрий: и а значит, число симметрий для неё равняется 4. Молекула аммиака - тригональная пирамида (точечная группа ) имеет следующие операции симметрии: следовательно, число симметрии равняется шести.
Точечные группы симметрии делятся на четыре типа: 1. Изотропные - сферические (), икосаэдрические ( и ), октаэдрические ( и ) и тетраэдрические ( и ). 2. Диэдрические содержат взаимно перпендикулярных осей симметрии и 3. Осевые имеют лишь одну ось симметрии порядка 4. Несобственные осевые, или альтернирующие при группы обозначаются как при как
| Точечная группа | Операция симметрии | Пример |
|---|---|---|
| транс- | ||
| операций |
Последовательное выполнение операций симметрии называется их произведением. Например, в группе
Таким образом, произведение двух операций симметрии определяет третью операцию, которая характерна для точечной группы. В рассмотренном примере плоскости симметрии являются взаимно перпендикулярными, ось симметрии находится на пересечении двух плоскостей симметрии. Если произведение двух операций симметрии не зависит от порядка их выполнения, то операции коммутируют, например, Если оси симметрии находятся друг к другу под отличными от 180 углами, например под углом 120 в тригональной пирамиде или тригональной призме, то много операций симметрии не коммутируют, таким образом, результат зависит от порядка проведения операций.
Таким образом, набор операций симметрии для какой-либо точечной группы образует множество, которое называется группой.
Выделенные операции симметрии образуют группу, поскольку:
- определен закон умножения: последовательное выполнение двух операций дает третью операцию, входящую в заданный набор (умножение коммутативно)
- умножение ассоциативно:
и т.д.
- есть идемпотент
- каждый элемент - обратный самому себе.
Поскольку умножение коммутативно, группа абелева.
Лекция 6
[править]Для установления поведения координат данной молекулы, а также её атомных и молекулярных орбиталей, при применении тех или иных операций симметрии, составляют таблицы характеров. Например, для точечной группы таблица характеров будет следующей.
| Координаты или атомные орбитали | |||||
| 1 | 1 | 1 | 1 | ||
| 1 | 1 | -1 | -1 | ||
| 1 | -1 | 1 | -1 | ||
| 1 | -1 | -1 | 1 |
| Координаты или атомные орбитали | ||||
| 1 | 1 | 1 | ||
| 1 | 1 | -1 | ||
| 2 | -1 | 0 |
В столбцах характеров приведены соответствующие операции симметрии, а строки содержат характеры неприводимых представлений.
Действие операции симметрии на некоторую функцию должно привести к изменению координат, от которых зависит рассматриваемая функция, но одновременно должна изменяться и сама функция. Поскольку операции преобразования координат не могут изменять значение функции в конкретной точке физического пространства, значение функции в точке, заданной новым координатами, должно быть тем самым, которое имела первоначальная функция в неизменённых координатах:
Если в качестве старых координат взять координаты можно получить другую форму этого уравнения:
Таким образом, чтобы определить результат действия операции симметрии на функцию от старых координат, достаточно рассмотреть первоначальную функцию в зависимости от координат, для которых выполнены обратные преобразования.
Лекция 7
[править]Если все матрицы можно привести к квазидиагональному виду
одним и тем же преобразованием подобия, то представление называется приводимым, а в противном случае - неприводимым. Таким образом, в результате линейного преобразования базиса приводимое представление разлагается на представлений меньшей размерности:
Пусть - элемент группы порядка Элемент
называется сопряженным к Совокупность взаимно сопряженных элементов называется классом. Число элементов в классе называется порядком класса.
Свойства неприводимых представления:
- число неэквивалентных неприводимых представлений равно числу классов в группе
- сумма квадратов размерностей неприводимых представлений равна порядку группы. У абелевых групп все неприводимые представления одномерны, число неприводимых представлений равно числу классов и равно числу элементов группы
- размерность неприводимых представлений конечной группы является делителем ее порядка
- характеры неприводимых представлений удовлетворяют условиям ортогональности:
Число неприводимых представлений, их размерности и характеры однозначно определены для каждой точечной группы, поэтому характеры неприводимых представлений могут быть сведены в таблицы.
Обозначения, которые обычно используют для неприводимых представлений, были введены Р.Малликеном в 1933 году. В символах неприводимых представлений отражаются их размерность, четность, наличие других однотипных неприводимых представлений (НП).
1. Одномерные НП обозначаются символами и в зависимости от характера операции поворота вокруг главной оси:
- если символ представления "";
- если то символ представления "".
2. Если молекула имеет центр инверсии, то в зависимости от характера для операции инверсии НП подразделяются на чётные, "", и нечётные, "" Например и т.д. 3. В каждой точечной группе есть НП, у которого характеры всех операций равны +1. Его называют полносимметричным и для конечных групп обозначают или (а также ). 4. Если в точечной группе есть несколько НП типа "" (или "", "", ""), их нумеруют: и т.п. В точечных группах и имеющих три взаимно-перпендикулярных оси символы представлений указываю, для какой из этих осей, или В группе НП обозначают и 5. Для обозначения НП, по которым преобразуются многоэлектронные волновые функции, используют прописные буквы для НП. по которым преобразуются орбитали - строчные
Представление - полносимметричное, описывает поведение s-орбиталей, координаты (орбитали ) и орбитали Эти орбитали при любых преобразованиях группы неизменны (все характеры равны +1). Представление описывает поведение орбитали при преобразованиях симметрии и имеет характеры: 1, 1, -1, -1. В самом деле, при операции покоя () и вращении вокруг оси на 180 () орбиталь АО остается без изменений. При отображении в плоскостях и орбиталь меняет знак на противоположный. Символами обозначаются изображения, обращающие знак при повороте вокруг главной оси (в данном случае ).
Лекция 8
[править]В зависимости от базисного набора для каждой точечной группы можно построить любое число приводимых представлений. В то же время число неприводимых представлений конечной группы относительно невелико, при этом каждое НП задает определенный способ поведения его базисных функций под действием операций группы, поэтому классификация функций по НП точечной группы молекулы создает универсальный язык для описания их свойств симметрии.
Для решения этой задачи нужно:
- определить на какие НП можно разбить приводимое представление, построенное в выбранном базисе
- найти базисные функции каждого НП.
Пусть - номер НП; - число, которое показывает, сколько раз НП входит в приводимое представление (ПП); и - размерности ПП и НП:
Характер операции в ПП равен
Сложное представление является приводимым, а простые представления - неприводимыми. Для приведения приводимого представления к сумме неприводимых () можно воспользоваться формулой:
где - целочисленные коэффициенты, которые находятся по формуле:
Здесь - число симметрии, - число операций симметрии в классе - характер неприводимого представления; - характер приводимого представления.
Характеры точечной группы
- атомные орбитали водорода:
| 3 | 0 | 0 | 1 | 1 | 1 |
- валентные атомные орбитали атома азота:
| 4 | 1 | 1 | 2 | 2 | 2 |
- все валентные атомные орбитали аммиака:
Размерность этого представления равняется 7. Матрицы можно построить из матриц первых двух представлений (1) и (2).
Одна функция может быть базисом одномерного представления точечной группы, если при всех операциях симметрии она преобразуется в себя.
- Характеры всех операций в одномерных представлениях совпадают с самими матрицами и показывают, как преобразуется базисная функция под действием операции симметрии.
- Среди представлений любой группы есть тривиальное тождественное представление, в котором каждому элементу симметрии сопоставляется одна и та же одномерная матрица, единственный элемент которой равен 1.
- Набор функций не может быть базисом представления, если для описания действия какой-либо операции симметрии точечной группы молекулы на любую из взятых функций необходим выхода за его пределы Таким образом, если молекула содержит эквивалентные атомы, в базис любого представления должны быть включены преобразующиеся друг через друга орбитали каждого из них.
Лекция 9
[править]Основные понятия квантовой механики состоят в следующем. Подобно тому, как в классической механике свойства систем могут выражаться заданием координат и импульсов всех частиц, так и в квантовой механике операторы величин выражаются с помощью операторов координат и импульсов. Операторы в квантовой механике используются для описания физических величин, характеризующих квантовые объекты. В классической механике какая-нибудь физическая величина (например, энергия) является переменной или функцией, имеет конкретное числовое значение или изменяется по известному закону. В квантовой механике каждой физической величине ставится в соответствие оператор, который может содержать "условную" часть или вообще может не иметь числового значения, как, например, оператор дифференцирования. Значение данной физической величины рассчитывается исходя из действия соответствующего оператора на волновую функцию при условии, что волновая функция является собственной функцией данного оператора. Значением физической величины является собственное значение оператора.
Оператором координаты является просто координата; его действие на какую-либо функцию состоит в умножении на вектор определяемый координатами то есть, или Оператор импульса определяется через его проекции (например, на оси декартовой системы координат):
Функция заменяется на оператор который получается из классического выражения этой функции заменой переменных на соответствующие операторы: Например, оператор кинетической энергии электрона получается заменой в выражении соответствующих компонент импульса операторами:
Можно также воспользоваться оператором Лапласа, в результате оператор кинетической энергии электрона приобретет вид
Потенциальная энергия является функцией лишь координат и времени, поэтому оператор выражается через операторы координат по тем же формулам, что и потенциальная энергия в квантовой механике. Например, оператор потенциальной энергии взаимодействия электрона с ядром заряда будет иметь следующий вид: Полная энергия классической системы равна сумме кинетической и потенциальной энергий. Таким же образом, в квантовой механике оператор полной энергии (оператор Гамильтона, или гамильтониан) равен сумме операторов кинетический и потенциальной энергий. Например, для одноэлектронного атома получим:
Две физические величины могут быть одновременно измерены с любой наперед заданной степенью точности лишь при условии, что их операторы коммутируют. Например, допустим, что величины и одновременно измеримы, из чего следует, что обоим операторам и соответствует одна и та же собственная функция и собственные значения и соответственно: Подействуем оператором на правое, а оператором на левое уравнения: Функция является собственной функцией для этих операторов: Теперь вычтем из левого уравнения правое уравнение: Выражение в скобках и есть коммутатором операторов и Волновая функция отлична от нуля, а значит равенство справедливо лишь в том случае, когда коммутатор равен нулю:
Конкретизируя сказанное, рассмотрим операторы импульса и координаты Удостоверимся в том, что они некоммутируют; имеем: то есть, Таким же образом и и Это означает, что вследствие некоммутации операторов импульса и координаты координата и импульс не могут быть одновременно измерены с любой заданной точностью.
Лекция 10
[править]Химическая связь в молекулах может рассматриваться с точки зрения молекулярных орбиталей (МО). Соображения о симметриях дают возможность унифицировать и до определенной степени упростить строение МО. При рассмотрении молекул типа пользуются следующей схемой.
1. Выбор базиса атомных орбиталей атома с оглядкой на его энергию.
2. Классификация атомных орбиталей по симметрии, пользуясь таблицей характеров.
3. Составление линейных комбинаций атомных орбиталей согласно энергии и симметрии атомов
4. Выведение молекулярных орбитлей как линейных комбинаций атомных орбиталей (ЛКАО).
5. Приблизительное расположение МО по величине увеличения энергии.
6. "Заселение" МО валентными электронами.
К примеру, рассмотрим молекулу воды.
1. Электронное строение атома - Атомная орбиталь не берет участия в образовании МО, как и вакантная Лишь атомные орбитали и подходят по энергии. Подходящими по энергии орбиталями могут быть лишь -орбитали. Таким образом, для строения МО воды отобраны и атома Оксигена и атома Гидрогена.
2. Из следующего рисунка понятно, что орбиталь соответствует неприводимому представлению - НП a - НП

3. Линейные комбинации Гидрогена составляются с тем, чтобы они имели одинаковые с орбиталями знаки, с которыми они перекрываются. Для подходит комбинация (обе орбитали перекрываются с положительной частью орбитали), а для - линейная комбинация Орбиталь () не перекрывается Гидрогена, а значит является несвязной. Оксигена принедлежит НП - тому же НП, что и поэтому она не может комбинироваться с ЛКАО Гидрогена.
4. МО в виде ЛКАО:
Коэффициенты не равны единице, уравнения МО не нормированы. Все МО являются трицентровыми. Для связующих () МО на линии связи МО не имеют узлов, а у антисвязующих ( и ) МО смена знака функции имеет место на линиях связи.
5. В первом приближении уровни связующей и антисвязующей МО определяются прежде всего интегралами перекрывания. Угол равен приблизительно 105 градусам, то есть перекрывание водорода значительно больше с ()-орбиталью, нежели с ()-орбиталью (угол приблизительно равен 53, угол - приблизительно 37). Таким образом, орбиталь находится ниже

Количество МО должно быть равно количеству базисных атомных орбиталей: четыре атомные орбитали Окисгена и две атомные орбитали Гидрогена. Таким образом, молекула воды содержит шесть МО:
6. Количество валентных электронов равняется 8 (шесть от Оксигена и два от Гидрогена). По принципу Паули электронная конфигурация воды имеет вид: Высшей занятой орбиталью является несвязующая

Если при образовании молекулы из атомов электрон занимает орбитали с низкой энергией, то полная энергия системы уменьшится, возникает более стойкое состояние - образуется химическая связь. Поэтому орбиталь называется связующей. Переход электрона на орбиталь увеличивает энергию системы, связь при этом не образуется, наоборот, система стает менее стойкой. Такая связь называется антисвязующей.

Связующее и антисвязующее действия обусловлены видом волновой функции молекулярных орбиталей. При сложении атомных волновых функций и величина (а значит и ) в пространстве между ядрами возрастает - появляется зона высокой электронной густоты, которая притягивает ядра и осуществляет химическую связь. При вычитании и электронная густота между ядрами уменьшается, что усиливает их отталкивание.
Лекция 11
[править]Образование двухэлектронной двохцентровой связи может происходить не только вследствие спаривания электронов соседних атомов, но и иным путём. В частности, при донорно-акцепторной связи один атом отдаёт пару электронов, а другой предоставляет вакантную орбиталь. Например, Нитроген в молекуле аммиака образует донорно-акцепторную связь с протоном, имеющим вакантную -орбиталь:
В соединениях Бор имеет одну -вакантную атомную орбиталь и образует связи с донорами электронных пар:
Бор с Нитрогеном посредством донорно-акцепторной связи способны имитировать соединения Карбона. Например, является аналогом гексафлуоретана, а имитирует тетраметилметан.
Рассмотрим молекулу Распределение электронов по квантовым ячейкам в возбужденном атоме Карбона и в атоме Оксигена следующий.

Возможно образование двух химических связей, поскольку в атоме Оксигена два неспаренных электрона. Однако при "переходе" одного электрона от Оксигена к Карбону в образовавшихся ионах и будет по три неспаренных электрона.

Эти ионы имеют ту же электронную конфигурацию, что и атом Нитрогена. При соединении и возникает тройная связь. Тройная связь прочнее двойной; его образование приведет к состоянию с более низкой потенциальной энергией.
В молекуле диборана электронов меньше, чем это необходимо для образования двохэлектронных связей. Казалось бы, она должна быть подобна по структуре к
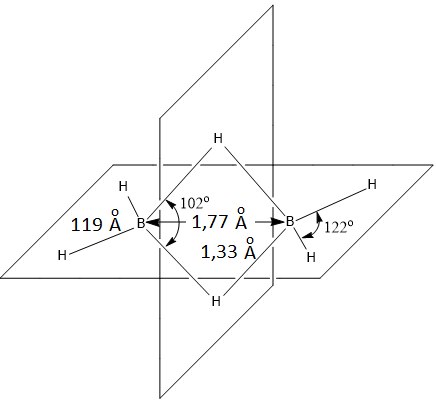
Однако, в отличие от у лишь 12 валентных электронов. Согласно экспериментальным сведениям атомы Водорода неравноценны: четыре из них легко замещаются (например, на группы ), а замещение других связано с распадом молекулы (например, на две молекулы ). У диборана четыре двухэлектронные концевые -связи, другие четыре электрон объединяют радикалы с помощью водородных мостечков, лежащих в радикалах Таким образом, вокруг каждого атома Бора формируется искаженный тетраэдр. Таким образом формируются так называемые "банановые" связи электрондефицитных молекул

Соединения с дефицитом электронов являются их акцепторами. Поэтому при взаимодействии с Калием за счет электрона последнего происходит образование бораната калия все связи при этом стают двухэлектронными.
Лекция 12
[править]Каждый атом или ион в кристаллической жидкости всегда окружён другими атомами, ионами или молекулами. В многоатомных ионах кислоротсодержащих кислот, например в вокруг атома неметалла находятся атомы гидрогена или металла. Число частиц (ионов или молекул), которые окружают данный ион (или атом), называется координационным числом.
В структуре комплексных соединений можно отличить координационную (внутреннюю) сферу - группировку, состоящую из центральной частицы (комплексообразователя - иона или атома) и лигандов (-дендов), молекул или ионов противоположного знака. В формулах комплексных соединений координационная сфера обозначается квадратными скобками. Например, Количество лигандов, окружающих комплексообразователь, называется координационным числом. Ионы, находящиеся вне координационной сферы образуют внешнюю сферу комплекса. Координационная сфера сохраняется и в растворах комплексных соединений. например, являются ионами, образовавшимися в результате диссоциации указанных соединений.
Комплексы могут быть получены в результате соединения простых веществ, например, или
Комплексных соединений значительно больше, чем всех остальных неорганических веществ. Например, гемоглобин (комплексообразователь - двухвалентное железо) и хлорофилл (). Комплексообразование характерно для ионов переходных металлов, в частности, и ионов элементов VIII группы периодической системы. Лигандами в комплексных соединениях часто являются ионы галогенов и нейтральные молекулы этилен- и бензол- могут образовывать -комплексы и сэндвич-структуры.
Для некоторых комплексообразователей координационное число постоянное, однако для большинства ионов-комплексообразователей оно может быть разным. Это зависит от природы лигандов и условий образования комплексов. Например, в комплексах встречаются координационные числа 2 и 4.
Некоторые лиганды содержат несколько групп в своих молекулах, которыми они могут соединяться к комплексообразователю. Например, в молекуле содержится две группы которые легко присоединяются к ионам Каждый из этих лигандов в комплексах может занимать место двух обычных лигандов, например, Координационная ёмкость (детантность) равняется 2.
Комплексные соединения также именуют:
- аквасоединения (лиганды - молекулы ),
- аммиакаты (лиганды - ),
- гидросоединения (лиганды - ионы ),
- кислотокомплексы (ацидокомплексы) - лигандами являются кислотные остатки - например,
Известны соединения смешанного типа. Названия комплексных соединений образуются также, как и названия обычных солей ( - хлорид натрия, сульфат калия), однако указываются также лиганды и ступень окисления центрального иона. Молекулы обозначаются "аква" и "амин".
Рекомендуемая литература
[править]1. Физические методы в химии, том 1 - Драго Р.
2. Сизова О.В., Иванова Н.В., Ванин А.А. - Молекулярная симметрия в неорганической и координационной химии: Учеб. пособие, 2-е издание, 216 с., 2016.
























































































































































































![{\displaystyle \mathrm {[Cu(NH_{3})_{5}]^{2+}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/d9fdb3c715fc6856297091c5e454409c389aec08)











![{\displaystyle \mathrm {[PtCl_{4}]^{2-}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/de8bf05e967b1cda79205b01d332699a40d97a6a)











































![{\displaystyle \sum _{i=1}^{h}[\chi ^{(P)}(g_{i})]^{*}\cdot \chi ^{(P)}(g_{i})=h\cdot \delta _{P,Q}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ebf0caa5faad02bbb36b0cddfb54c6f419e29341)

















































































![{\displaystyle [{\hat {A}},{\hat {B}}]=0.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8608ebd0aa75bf0324d6d9a0d5598bbfffda2a12)


![{\displaystyle [{\hat {p}}_{x},{\hat {x}}]f={\hat {p}}_{x}{\hat {x}}(f)-{\hat {x}}{\hat {p}}_{x}=-i\hbar {\frac {\partial }{\partial x}}(x\cdot f)-x(-i\hbar ){\frac {\partial }{\partial x}}(f)=-i\hbar \cdot x{\frac {\partial f}{\partial x}}-i\hbar \cdot f+i\hbar \cdot x{\frac {\partial f}{\partial x}}=-i\hbar \cdot f;}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d3bbdcb91c5b0f3f5c495e94458c1e3fb8ffc893)
![{\displaystyle [{\hat {p}}_{x},{\hat {x}}]=-i\hbar .}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1d8105be4b0c1b8a1afb0393ecb8f0f59b301f61)
![{\displaystyle [{\hat {p}}_{y},{\hat {y}}]=-i\hbar ,}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9d9a78fd596a6b5d7800cc722ac209d152c1029e)
![{\displaystyle [\hbar {p}_{z},{\hat {z}}]=-i\hbar .}](https://wikimedia.org/api/rest_v1/media/math/render/svg/662e66ee434bd7e6c4bb5395916246fd4fce0f54)





























































![{\displaystyle \mathrm {K_{4}[Fe(CN)_{6}],\,\,K_{2}[HgI_{4}],\,\,[Ag(NH_{3})_{2}]Cl} .}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f16f22ad26f69a4595be953f1a4905b58d3ffb38)
![{\displaystyle \mathrm {[Fe(CN_{6})]^{4-},\,\,[HgI_{4}]^{2-}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/7bcea362485cda2298c26306c979b72159f8ea05)
![{\displaystyle \mathrm {CuCl_{2}+4NH_{3}=[Cu(NH_{3})_{4}]Cl_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/dc3745549721c06e2b347420757e6770cb2d6935)
![{\displaystyle \mathrm {AgI+KI=K[AgI_{2}]} .}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5a94683f88c9a293abcbf3b11d4d693d603f6904)













![{\displaystyle \mathrm {[Cr(H_{2}O)_{6}]Cl_{3},\,\,[Ca(H_{2}O)_{6}]Cl_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/df08260fca08c16f3baa50f3e62a83c2f1ac4546)
![{\displaystyle \mathrm {[Cu(NH_{3})_{4}]SO_{4},\,\,[Ag(NH_{3})_{2}]Cl} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/b33cd7335dafab256d6944bfabe1d08d43058d76)

![{\displaystyle \mathrm {K_{2}[Zn(OH)_{4}],\,\,Na_{2}[Sn(OH)_{6}]} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/ce7e0f340a484cd0a6b1adbba801a2e46529ce12)
![{\displaystyle \mathrm {K_{4}[Fe(CN)_{6}]} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/fe518ea131040be16fcab342bd12ad5d04b5969b)

