Иммунология/Одностраничная версия
СПИСОК АББРЕВИАТУР
[править]BCR — антигенраспознающий рецептор В-лимфоцитов (B-cell receptor)
CDR — участок, определяющий комплементарность (Complementarity determining region)
CLP — общий лимфоидный предшественник (Common lymphoid progenitor)
ELP — ранний лимфоидный предшественник (Еarly lymphoid progenitоr)
G-CSF — гранулоцитарный колониестимулирующий фактор
GM-CSF — гранулоцитарно-макрофагальный колониестимулирующий фактор
GM-линия — гранулоцитарно-макрофагальная линия
HLA — лейкоцитарный антиген человека (Human leukocyte antigen)
IFN — интерферон
IL — интерлейкин
ITAM — активационный тирозинсодержащий мотив иммунорецепторов (Immunoreceptor tyrosine-based activation motif )
ITIM — ингибирующий тирозинсодержащий мотив иммунорецепторов (Immunoreceptor tyrosine-based inhibition motif )
KIR — иммуноглобулиноподобный рецептор киллерных клеток (Killer cell Ig-like receptor)
LFA — функциональный антиген лимфоцитов (Lymphocyte fuctional antigen)
MBL — маннозасвязывающий лектин (Mannosa-binding lectin)
M-CSF — моноцитарно-макрофагальный колониестимулирующий фактор
MHC — главный комплекс гистосовместимости (Major histocompatibility complex)
MHC-I — молекула главного комплекса гистосовместимости I класса
MHC-II — молекула главного комплекса гистосовместимости II класса
NK-клетки — естественная киллерная клетка (Natural killer)
PAMP — патогенассоциированные молекулярные паттерны, образы патогенности (Pathogen-associated molecular patterns)
PI3K — фосфатидилинозитол 3-киназа
PLC — фосфолипаза С
SCF — фактор стволовых клеток (Stem cell factor)
TCR — антигенраспознающий рецептор Т-лимфоцитов (T-cell receptor)
TGF — трансформирующий фактор роста (Transforming growth factor)
TIL — лимфоцит, инфильтрирующий опухоль (Tumor-infiltrating lymphocyte)
TLR — Toll-подобный рецептор (Toll-like receptor)
TNF — фактор некроза опухоли (Tumor necrosis factor)
АКТГ — адренокортикотропный гормон
АПК — антигенпрезентирующая клетка
АТФ — аденозинтрифосфат
БЦЖ — бацилла Кальмета — Жерена
ВИЧ — вирус иммунодефицита человека
ГДФ — гуанинозиндифосфат
ДНК — дезоксирибонуклеиновая кислота
ЛПС — липополисахарид
РНК — рибонуклеиновая кислота
РТПХ — реакция «трансплантат против хозяина»
СКВ — системная красная волчанка
ТКИН — тяжелая комбинированная иммунная недостаточность
ТН — тимуснезависимый
ТН-1 антиген — тимуснезависимый антиген (ответ) типа 1
ТН-2 антиген — тимуснезависимый антиген (ответ) типа 2
цАМФ — циклический аденозинмонофосфат
СТРУКТУРА И ФУНКЦИИ ИММУННОЙ СИСТЕМЫ
[править]ОПРЕДЕЛЕНИЕ БИОЛОГИЧЕСКОГО ЯВЛЕНИЯ «ИММУНИТЕТ»
[править]Введение в предмет
[править]Иммунология — наука об иммунитете. Иммунитет — некое защитное биологическое свойство живых многоклеточных организмов, предохраняющее эти организмы от инфекционных болезней(и не только от них). Иммунитетом мы будем называть только и исключительно те защитные процессы, которые реализуются с участием лимфоцитов. Остальные защитные механизмы связаны и с иммунитетом, и между собой в едином организме, работают вместе. Но они различимы и каждый характеризуется особыми признаками, позволяющими отличать один от другого. Основные функции иммунитета
- Распознавание и элиминация из организма собственных, но ненужных клеток(в первую очередь поврежденных инфекцией, травмированных), т.е. некое уникальное самораспознавание и явилось тем новым эволюционным приобретением многогоклеточных. Носителем нового свойства стали тоже новые, особые дифференцированные клетки — лимфоциты. Появившись последним, иммунитет опирается и вписывается, сопрягается со всеми остальными защитными системами многоклеточных, работает не отдельно от них, а исключительно вместе с ними.
- Защита от инфекции, от пищевых, ингаляционных и аппликаторных внешних веществ, проникающих во внутреннюю среду.
- Реакция на трансплантат.
Предмет иммунологии
[править]Лимфоциты взаимодействуют со всеми клетками системы крови, сосудов, по которым и через стенку которых лимфоциты попадают в ткани. Лимфоциты способны вступать в контакты со всеми клетками организма. Лимфоциты через специальные рецепторы воспринимают информацию от нервной системы, эндокринной системы, об уровне глюкозы в крови. Предметом иммунологии как отдельной науки являются не все способы защиты организма от инфекций, а в первую очередь лимфоцитарный иммунитет и тесно связанные с ним филогенетически, онтогенетически и морфологически фагоцитоз, белки острой фазы и сосудистые реакции, которые совместно осуществляют такую объединенную защитную реакцию, которую называют воспалением.
Антигены
[править]Антигенами называют молекулы, способные вызывать иммунный ответ, т.е. комплекс реакций, направленных на их удаление из внутренней среды организма. Антигены — это не особый класс соединений: ими могут быть белки и некоторые другие макромолекулы (например, полисахариды), в том числе комплексированные с любыми химическими структурами. Антигенность молекулы определяется ее способностью вызывать реакцию иммунной системы организма (подобно пахучим веществам — любым соединениям, воспринимаемым органами обоняния). Таким образом, отнесение вещества к антигенам определяется не на основании его объективных характеристик, а исходя из его способности вызывать реакцию иммунной системы данного конкретного организма (т.е. как бы «с точки зрения» иммунной системы). Более того, комплексы признаков, которыми должен обладать антиген «с точки зрения» В- и Т-лимфоцитов, существенно различаются. Все это осложняет изучение антигенов, в том числе и в практическом аспекте.
Чужеродность антигенов
[править]Основная функция иммунной системы состоит в защите организма от биологической агрессии, исходящей, как правило, извне от патогенов и их продуктов, чужеродных для макроорганизма. Эндогенная агрессия в виде развития опухолей тоже часто связана с приобретением собственными клетками организма определенных черт чужеродности.
Основополагающим структурно-молекулярным компонентом врожденной системы неспецифической защиты являются образраспознающие рецепторы (pattern recognition receptors - PRR). PRR узнают высоко уникальные, не имеющих аналогов в макроорганизме, консервативные молекулярные структуры, которые были названы патоген-ассоциированными молекулярными структурами (pathogen-associated molecular patterns – РАМР).
Наиболее известными РАМР являются липополисахариды (LPS), представляющие структурные компоненты внешней мембраны грам-отрицательных бактерий; тейхоевые и липотейхоевые кислоты, которые являются мембранными компонентами преимущественно грам-положительных бактерий; пептидогликаны грам-положительных и грам-отрицательных бактерий; липоарабиноманноза микобактерий; зимозан грибов; двуспиральные вирусные РНК; бактериальные ДНК.
Каждая патоген-ассоциированная молекулярная структура является маркером достаточно больших кластеров микроорганизмов, поэтому процесс их распознавания PRR носит неспецифический характер.
Ранее в качестве маркеров чужеродности рассматривали именно антигены. В настоящее время более значимыми носителями признаков чужеродности считают PAMP, поскольку именно они ответственны за включение процессов, составляющих основу иммунной защиты. Соответствие между PAMP (отвечают за активацию врожденного иммунитета) и антигенами (отвечают за запуск адаптивного иммунитета) не до конца выяснено. В ряде случаев одна и та же молекула сочетает в себе свойства PAMP и антигена, в других случаях в роли PAMP и антигена выступают разные молекулы патогенов.
В любом случае чужеродные молекулы можно рассматривать как маркеры клеток, потенциально опасных для организма. Эти молекулы служат наиболее ранним сигналом опасности, распознаваемым задолго до проявления патогеном своих вредоносных качеств. Таким образом, эволюция избрала косвенный путь выявления потенциально опасных агентов по их чужеродности для данного организма. Это послужило основанием для определения антигенов, данного Р.В. Петровым: антигены — это биологические тела и молекулы, несущие признаки чужеродной генетической информации. Поскольку чужеродность проявляется относительно конкретного организма, молекула, воспринимаемая как антиген одним организмом, может не восприниматься в качестве такового другим организмом. Связь антигенности с чужеродностью макромолекулы для данного организма наглядно проявляется при оценке иммуногенности гомологичных белков. Иммуногенность возрастает по мере увеличения «эволюционного расстояния» между донором и реципиентом белка. В основе повышения иммуногенности лежит увеличение различий в первичной структуре белков. Эти закономерности используют при серологической оценке степени эволюционного родства видов.
Однако чужеродность — не абсолютная характеристика антигена. Об этом свидетельствует возможность образования аутоантител, т.е. антител к собственным молекулам организма. В тех случаях, когда аутоантигенами являются компоненты тканей, в норме изолированных от иммунной системы («забарьерные ткани»), это не нарушает общего принципа чужеродности. В других случаях аутоантитела образуются в ответ на действие чужеродных субстанций, имеющих структурное сродство с аутологичными компонентами; эти антитела перекрестно реагируют с аутоантигенами. Так бывает, например, при стрептококковой инфекции, при которой образуются антитела к микробным полисахаридам, реагирующие с полисахаридами соединительной и эпителиальных тканей. Лишь в редких случаях, обычно при патологии, затрагивающей иммунную систему, механизмы селекции клонов лимфоцитов и иммунорегуляцию, возникает истинная реакция на собственные антигены (например, при системной красной волчанке).
В организме всегда присутствуют многочисленные аутоантитела, взаимодействующие с собственными молекулами организма. Такие антитела продуцируются в основном В1-клетками. Эти антитела обладают низким сродством к антигенам, часто полиспецифичны; они не способны активировать некоторые эффекторные механизмы врожденного иммунитета (например, разрушение носителя антигена фагоцитом). В связи с этим такие аутоантитела не повреждают ткани, а напротив, выполняют ряд важных функций (транспорт макромолекул, элиминацию отработавших молекул и другие гомеостатические функции). Функционально важную группу аутоантител образуют антитела к идиотопам иммуноглобулинов ( анти-антитела). Они копируют конфигурации антигенных эпитопов, служа их «внутренними образами» и играют определенную роль в регуляции иммунного ответа
Иммуногенность антигенов
[править]Иммуногенность обусловливает способность антигена вызывать иммунный ответ независимо от его специфичности. Биологической основой для проявления этого свойства антигенов служат те механизмы развития иммунного ответа, которые предполагают участие, помимо лимфоцитов, определяющих специфическую компоненту реакции, некоторых вспомогательных клеток, а также кооперацию различных типов лимфоцитов. Способность чужеродных веществ вовлекать в реакцию весь необходимый клеточный ансамбль и составляет основу их иммуногенности. Иммуногенность антигенов зависит не только от свойств молекулы, но и от пути и режима их введения в организм, от дополнительных воздействий.
Структурно-химические основы иммуногенности
[править]Антигенами могут быть прежде всего белки и углеводы. Липиды, нуклеиновые кислоты и другие органические вещества слабоиммуногенны и эффективны лишь в составе комплексных соединений (например, в виде конъюгатов с белками). В составе таких конъюгатов они могут обусловливать антигенную специфичность. Использование конъюгатов низкомолекулярных соединений (гаптенов) с белками-носителями, введенное в научную практику К Ландштейнером, сыграло ключевую роль в анализе свойств антигенов. В частности, с помощью конъюгатов было показано, что специфичность антигена определяется преимущественно гаптеном, а иммуногенность — белком-носителем. С позиций современной иммунологии, предполагающей необходимость кооперации В-лимфоцитов, вовлекаемых в гуморальный иммунный ответ, с Т-хелперами, иммуногенность в значительной степени обусловливается способностью антигена активировать Т-хелпер. Важным условием развития иммунного ответа служит предварительная активация дендритных клеток в результате распознавания ими PAMP. Именно поэтому следует признать, что иммуногенность молекул антигена во многом определяется наличием в их составе PAMP, т.е. их способностью сформировать при поступлении в организм «провоспалительный фон».
Важнейшим качеством, определяющим иммуногенность антигенов, является размер молекулы. С повышением молекулярной массы полимерных молекул увеличивается их иммуногенность. Исключения известны лишь для углеводных антигенов, для которых это правило срабатывает лишь до определенного предела. Универсальной шкалы зависимости иммуногенности от молекулярной массы не существует. Для белков пороговый размер молекулы, определяющий появление иммуногенности, ниже, чем для углеводов. Для белков эта граница, вероятно, связана с появлением а-спиральной структуры (7—10 аминокислотных остатков), однако она варьирует в зависимости от конкретного состава, в том числе от пособности остатков участвовать в формировании а-спирали. Минимальная описанная молекулярная масса иммуногена составляет 450 Да (арсанил — N - ацетил— DL -тирозин). При переходе от мономерной формы флагеллина (40 кДа) к полимерной (20 000 кДа) титры антител возрастают на два порядка. Для углеводов граница между низкой и высокой иммуногенностью располагается на «уровне» молекулярной массы в десятки тысяч: полимер декстрана с массой 52,3 кДа слабоиммуногенен, а с массой 90,7 кДа обеспечивает развитие достаточно сильного ответа. Численность антителообразующих клеток, появляющихся в селезенке при иммунизации тремя полимерами пневмококкового полисахарида с молекулярными массами 220, 121 и 40 кДа, отличается примерно на порядок (со снижением молекулярной массы уровень ответа убывает).
Помимо формирования определенных структур, от которых зависит иммуногенность (например, а-спирали), размер молекулы важен и для увеличения числа групп, обусловливающих специфичность ответа, — антигенных детерминант, или эпитопов, т.е. повышения валентности антигена. Значение этого фактора также проявляется наиболее четко при использовании конъюгатов, содержащих различное число гаптенных групп. С повышением числа идентичных групп иммуногенность конъюгата растет, даже если его размеры не увеличиваются. Однако после достижения определенной эпитопной плотности дальнейшее возрастание иммуногенности с увеличением числа эпитопов прекращается, и может наблюдаться даже снижение иммуногенности вследствие стерических помех в распознавании детерминант, их взаимной маскировки. Естественно, чем больше величина молекулы, тем больше детерминант она может вместить без подобного перенасыщения.
Влияние валентности на иммуногенность имеет значение также в связи с разнообразием эпитопов, присутствующих на молекуле. Установлено, что молекула приобретает иммуногенность лишь при условии достаточного разнообразия ее структуры. Так, поли-Ь-лизин иммуногенен только для ограниченного числа животных, например для некоторых линий морских свинок. Однако введение в состав этой молекулы боковых цепей или чередование лизина с другими остатками в составе основной цепи делает полимер иммуногенным практически для любых реципиентов.
Наконец, роль размера молекулы в проявлении ее иммуногенности может быть проиллюстрирована на примере молекулярных агрегатов. Их высокая иммуногенность в значительной степени обусловлена тем, что они активно подвергаются эндоцитозу, это важно для процесса обработки антигена и его представления Т-хелперам.
Давно отмечено, что иммуногенность антигенов зависит от жесткости их структуры, т.е. способности сохранять достаточно определенную конфигурацию, детали которой и являются объектами распознавания лимфоцитарными рецепторами. Стабилизации конформации способствует присутствие ароматических, заряженных, полярных аминокислотных остатков. Так, молекула желатина, утратившая жесткость конформации в результате обработки, практически неиммуногенна, но становится иммуногенной после введения в ее состав ароматических аминокислот. Наоборот, гидрофобные остатки в большом количестве препятствуют формированию а-спирали и стабилизации конформации молекул. Чрезмерную гибкость придают полимерам остатки пролина, особенно повторяющиеся. В обоих случаях снижение стабильности молекул сопровождается ослаблением их иммуногенности. На «уровне» выбора участка молекулы, определяющего специфичность антител (см. далее), однако предпочтительной является достаточно высокая его гибкость, позволяющая «подстроиться» под структуру активного центра иммуноглобулино-вого рецептора BCR.
Существует еще одно свойство антигенов, от которого зависит их иммуногенность: они должны принадлежать к тем классам полимеров, из которых построены организмы высших животных. Так, полипептиды, состоящие из D-аминокислот, не свойственных позвоночным, не иммуногенны или слабо иммуногенны для этих животных. Полагают, что это связано с затруднениями деградации этих веществ из-за отсутствия необходимых ферментов (частичное разрушение является условием вовлечения в иммунный ответ Т-хелперов, т.е. реализации иммуногенности). Считают, что со снижением способности расщепляться ферментами связано уменьшение иммуногенности белков после их рацемизации щелочами. Таким образом, хотя антигены по определению должны быть чужеродны для организма-хозяина, эта чужеродность не должна переходить определенные границы. Она проявляется в рамках типичного для высших животных и их окружения класса макромолекул, для расщепления которых организм располагает необходимым арсеналом ферментов.
Генетические аспекты иммуногенности
[править]Поскольку иммуногенность антигена зависит от эффективности процессов обработки, которым он подвергается в организме, следует ожидать, что она зависит и от генотипа реципиента, что имеет место в действительности. Существование генетического контроля иммунного ответа на конкретные антигены показано в разнообразных экспериментах. Так, при иммунизации инбредных морских свинок полимерами (Glu — Lys)n или конъюгатом динитрофенил — поли-L-Lys свинки одной линии отвечали образованием антител на оба конъюгата, а свинки другой линии не отвечали ни на один из них. Гибридологический анализ показал, что отвечаемость детерминируется одним доминантным геном.
Аналогичные результаты получены также в экспериментах на мышах с использованием других синтетических полипептидов. Если мышей иммунизировать разветвленными полипептидами (Т, G) — A-L и (His, G) — A-L (эти полипептиды содержат основную цепь, образованную поли-L-лизином, с боковыми полиаланиловыми цепями, заканчивающимися остатками тирозина и глутаминовой кислоты или гистидина и лизина), то мыши линии C57BL/6 дают высокий иммунный ответ на первый, но не на второй пептид. Мыши линии СВА, наоборот, сильно реагируют на второй и слабо — на первый пептид. И в этом случае сильный ответ детерминируется одним доминантным геном.
И у морских свинок, и у мышей показана связь генов иммунного ответа (1г-1) с комплексом МНС. Связь иммуногенности с MHC обусловлена различиями в сродстве аллельных вариантов молекул MHC к различным пептидным фрагментам антигенов, выступающих в качестве эпитопов для Т-клеток. Уровень иммунного ответа в значительной степени определяется эффективностью презентации антигенного пептида, а она зависит от способности пептидов встраиваться в молекулы MHC. Таким образом, генетическая детерминация структуры MHC (точнее, участка, связывающего пептид) одновременно распространяется на контроль уровня иммунного ответа.
В столь четкой форме генетическая детерминация иммуногенности проявляется лишь в отношении некоторых достаточно простых по структуре антигенов. Существуют и другие гены иммунного ответа; отвечаемость на сложные антигены подвержена комплексному генетическому контролю . Данные генетических исследований особенно наглядно подчеркивают относительность понятия «иммуногенность» и зависимость иммуногенности от свойств организма, в который введен антиген. Оказывается, что иммуногенность антигена может зависеть от особенностей реакции организма в большей степени, чем от структуры антигена.
Тимусзависмость антигенов
[править]Гуморальный иммунный ответ на белковые антигены обычно требует участия не только В-, но и Т-клеток и ослабляется в отсутствие тимуса
(у генетически бестимусных или тимэктомированных вскоре после рождения животных). При этом В-клетки распознают нативный антиген, тогда
как Т-клетки — его фрагменты (эпитопы), встроенные в состав молекул MHC (см. далее). Т-клетки могут выступать в качестве клеток-помощников при иммунном ответе только на те молекулы, чьи фрагменты могут встраиваться в состав молекул MHC (например, на белковые антигены). Ответ на другие антигены (например, полисахаридные) осуществляется В-клетками без участия Т-лимфоцитов. Именно поэтому они могут вызывать ответ у бестимусных nude-мышей. Иногда исключение Т-клеток из ответа на антигены обусловлено другими механизмами. Антигены, способные индуцировать иммунный ответ без участия Т-лимфоцитов, называют тимуснезависимыми, или Т-независимыми (ТН).
ТН-антигены, как правило, крупные молекулы (с молекулярной массой порядка 103кДа). По химической природе это могут быть полисахариды, ЛПС или белки. Они поливалентны, содержат повторяющиеся эпитопы. Полимеризация и агрегирование тимусзависимых антигенов нередко делает их ТН, а конъюгирование полисахаридов с белками, наоборот, переводит полисахаридные антигены из разряда ТН в тимусзависимые. Многие из ТН-антигенов медленно деградируют и длительно персистируют в организме. Для ответа на эти антигены не требуются их обработка и презентация АПК. По этой причине иммунный ответ на такие антигены не контролируется генами МНС. Однако это не означает, что в иммунном ответе на тимуснезависимые антигены участвуют только В-лимфоциты. Вспомогательные клетки (макрофаги, дендритные клетки, Т- и NK-лимфоциты) в той или иной степени вносят вклад в иммунный ответ на эти антигены. Например, они могут служить источником цитокинов, способствующих
пролиферации В-лимфоцитов, например, BAFF — цитокина семейства TNF, играющего ключевую роль в гомеостазе В-лимфоцитов (см. далее).
Важные сведения были получены при изучении ответа на ТН-антигены мышей с мутацией хid, затрагивающей тирозинкиназу btk и блокирующей дифференцировку В-лимфоцитов до стадии, на которой экспрессируется мембранная молекула Lyb-5. Эти мыши, а также новорожденные особи других линий, у которых не успели созреть Lyb-5+ В-клетки, отвечают не на все ТН-антигены. Антигены, на которые способны отвечать мыши с мутацией xid, обозначают как тимуснезависимые антигены 1 типа (ТН-1; Thymus-independent I), а антигены, ответ на которые у этих мышей отсутствует — как тимуснезависимые антигены II типа (ТН-2). В настоящее время установлено, что у Хid-мышей практически отсутствует одна из субпопуляций В-лимфоцитов — CD5+ B1a-клетки и специфический ответ на ТН-2 антигены связывают преимущественно с этими клетками. В качестве примера ТН-1 антигенов можно привести большинство бактериальных ЛПС, полифлагеллин, полисахарид бордетелл, а также их конъюгаты с гаптенами. Важно отметить, что ТН-1 антигены обладают митогенными свойствами в отношении В-клеток. К ТН-2 антигенам относят полисахаридные антигены (в том числе бактериальные), конъюгаты гаптенов с фиколлом, леваном, некоторые разновидности ЛПС, некоторые синтетические антигены (например, поливинилпирролидон).
Основной изотип антител, специфичных к тимуснезависимым антигенам, — IgM; при этом переключения изотипа обычно не происходит, отсутствует «созревание аффинитета» и практически не формируется иммунологическая память и, как следствие, не развивается вторичный иммунный ответ. Известны, однако, исключения из этих правил (например, переключение на IgA в слизистых оболочках).
ТН-антигены не презентируются Т-хелперам в составе MHC. Именно поэтому Т-хелперы не участвуют в ответе на эти антигены. Активацию
В-клеток ТН-антигенами лучше рассмотреть на примере ТН-2 антигенов. Способность активировать B-клетки без помощи Т-лимфоцитов обусловлена особенностями структуры ТН-2 антигенов. Важнейшие их свойства, как уже отмечалось, — наличие большого числа повторяющихся эпитопов и достаточно крупный размер молекулы. При связывании ТН-2 антигена происходит кластеризация BCR на поверхности лимфоцита. Это способствует активации киназ, ассоциированных с BCR, и индукции сигнала, достаточного для преодоления порога активации В-лимфоцитов. Вероятно, определенный вклад в активацию ТН-2 специфических клеток вносит распознавание ими PAMP, входящих в состав большинства ТН-антигенов.
ТН-1 антигены активируют В-лимфоциты несколько иначе. Механизм этой активации в настоящее время до конца не известен. Известно, что ТН-1
антигены способны активировать клетки через митогенные и паттернраспознающие рецепторы. Однако при низких концентрациях антигена такая
активация возможна только при его концентрировании на В-клетках при помощи BCR (поэтому в этих условиях на ТН-1 антигены отвечают только
клетки специфичных клонов). Не вполне ясно, поступают ли при этом в клетку активационные сигналы от BCR, связавших антиген. Митогенность
ТН-1 антигенов проявляется при повышении их концентрации до уровня, при котором для активации В-клеток дополнительное концентрирование
антигена при помощи BCR не требуется. Таким образом, в митогенных концентрациях ТН-1 антигены способны активировать все В-клетки, независимо от специфичности их BCR. В настоящее время лучше всего изучен ответ на ТН-1 антиген — ЛПС, который связывается с LBP и CD14 и в составе этого комплекса активирует клетку через TLR-4. Тем не менее, в ответе В-клеток на ТН-1 антигены остается много неясного.
Считают, что степень участия Т-хелперов или иных вспомогательных клеток (например, естественных киллеров) в ответе на ТН-2 антигены
выше, чем при ответе на ТН-1 антигены. Показана роль в развитии ответа на эти антигены ряда цитокинов (IL-3, GM-CSF, IFNγ, BAFF).
Толерогенность
[править]Альтернатива индукции иммунного ответа при ответе на антигены — развитие неотвечаемости. Это не просто отсутствие ответа, а активное и избирательное его подавление в отношении данного конкретного антигена. На уровне клетки эту реакцию называют анергией, а на уровне организма — иммунологической толерантностью. Толерантность индуцируется при введении высоких доз белков и полисахаридов при отсутствии молекулярных агрегатов. Для белков может развиться также низкодозная толерантность. Одно из важных свойств антигенов, способствующих индукции толерантности, — способность избегать поглощения АПК (например, отсутствие молекулярных агрегатов). Проявлению толерогенности способствует также относительно низкая молекулярная масса и высокая эпитопная плотность. Таким образом, одни и те же молекулы могут выступать в качестве иммуногенов и толерогенов или не оказывать действия на иммунную систему в зависимости от их физического состояния (степени агрегированности). Имеет значение также присутствие в микроокружении цитокинов, регулирующих активность дендритных клеток, обрабатывающих и презентирующих антиген Т-лимфоцитам: IL-12 и IFNγ способствуют проявлению иммуногенности, а IL-10 — толерогенности молекул антигенов. Очень важную роль играет степень экспрессии на поверхности дендритных клеток костимулирующих молекул (что, в свою очередь, зависит от наличия PAMP в молекуле антигена) — анергия развивается при слабой экспрессии этих молекул.
Специфичность антигенов
[править]В иммунологии под специфичностью понимают избирательность взаи-модействия индукторов и продуктов иммунных процессов, в частности,
антигенов и антител. Выше, при рассмотрении структуры антигенраспознающих рецепторов и антител упоминалось, что их сродство к антигенам и способность взаимодействовать с ними связана с четко ограниченным участком — активным центром или антигенсвязывающим участком.
Антигенные детерминанты
[править]Специфическое взаимодействие антител с молекулой антигена связано с относительно небольшим участком ее поверхности, соответствующим
по размеру антигенсвязывающему участку рецепторов и антител. Как уже упоминалось, при изучении иммунного ответа на конъюгаты гаптенов
с белками-носителями было установлено, что специфичность конъюгата определяют молекулы гаптена, к которым направлены образующиеся
антитела. Связь специфичности антигенов с относительно небольшими участками ее поверхности подтвердилась при анализе специфичности природных молекул белков и полисахаридов, а также при изучении ответа на синтетические полипептиды.
В этих работах было, в частности, установлено, что практически в любой молекуле антигена есть несколько детерминант, или эпитопов. Для антигенов с монотонной структурой (например, углеводных антигенов) характерны повторяющиеся однотипные детерминанты. Для белков свойственны разнообразные детерминанты, против каждой из которых в принципе может быть индуцирована выработка антител, отличающихся по специфичности от антител к другим детерминантам. При этом внутри молекулы устанавливается определенная иерархия детерминант, когда одна из них является доминирующей (явление иммунодоминантности), т.е. в спектре антител, которые образуются при введении этого антигена, преобладают антитела, специфичные к данной детерминанте. После ее искусственного удаления доминирующая роль переходит к другому эпитопу.
Связь специфичности антигенов с относительно небольшими фрагментами их молекул объясняется самой природой этой специфичности. Она
служит отражением пространственного соответствия (комплементарности) эпитопа и активного центра рецептора. Чем больше это пространственное соответствие, тем выше сродство эпитопа к активному центру рецептора. Распознавание эпитопа рецептором — пусковой момент иммунного ответа. Антитела, продуцируемые в результате такого ответа, соответствуют по своей специфичности рецептору и, следовательно, специфичны к упомянутому выше эпитопу.
Эпитоп представляет собой выпуклость на поверхности макромолекуярной глобулы, соответствующая по величине и конфигурации полости
активного центра антитела. Для того, чтобы эпитоп мог проникнуть в полость, размер эпитопа должен быть несколько меньше размеров полости
активного центра. Если протяженность активного центра составляет 6 нм, то длина эпитопа — до 4 нм, а его объем — 2–3 нм3. Эпитоп белковой молекулы может содержать 7–15 аминокислотных остатков (это соответствует массе 0,6–1 кДа), а эпитоп углеводной молекулы — 6 моносахаридных остатков. Наибольшую роль в обеспечении специфичности взаимодействия с активным центром играют концевые остатки в составе эпитопа (на долю концевого сахара приходится 39% энергии взаимодействия с антителом, а на долю 6-го остатка — только 6%). Учитывая постепенное убывание вклада мономеров во взаимодействие с активным центром, можно заключить, что суждения о границах эпитопа и его размерности весьма относительны.
Анализ специфичности антител, образуемых одним организмом, а также моноклональных антител, получаемых при иммунизации одного животного, показывает, что против одного эпитопа образуется широкий спектр разных антител. Это еще раз подчеркивает относительность представлений
об эпитопной структуре антигенов и невозможность однозначной локализации эпитопов. Эпитопная структура представится еще более размытой,
если учесть различия в индивидуальной реакции на антиген различных представителей одного или разных видов животных. Это отсутствие жесткого соответствия между структурами эпитопов и активных центров становится более понятным, если учесть, что в основе механизма формирования антигенраспознающего репертуара рецепторов лимфоцитов лежат случайные процессы . При вторичном иммунном ответе специфичность образующихся антител и их сродство к антигену становится выше за счет особого отбора, которому подвергаются предшественники антителообразующих клеток в ходе иммунного ответа.
Разрешающая способность распознавания гаптенов антителами детально изучена с помощью реакции задержки. Сущность ее состоит в том, что исследуемый свободный гаптен, взаимодействуя с антителами, препятствует реакции с ними конъюгата гаптен — белок, дающий видимые эффекты типа преципитации. При использовании идентичных гаптенов в свободной форме и в конъюгате реакцию можно полностью блокировать. При отсутствии идентичности степень подавления реакции будет тем выше, чем больше сходство между гаптенами. Аналогичные результаты можно получить при оценке перекрестной реакции конъюгатов, содержащих сравниваемые гаптены, с антителами к одному из них. Анализ, выполненный с помощью этих методик, позволил установить высокую разрешающую способность серологического распознавания (т.е. распознавания с помощью сыворотки, содержащей антитела). Выяснилось, что антитела различают оптическую конфигурацию углеводов, замещение атомов водорода в циклических соединениях на кислотные и азотсодержащие группы (в определенной степени даже на галогены). Четко распознаются позиции замещения (орто, мета, пара), особенно при замещении кислотными группами. Наконец, распознается заряд детерминанты, которому соответствует противоположный заряд активного центра.
Линейные и конформационные эпитопы
[править]Белковые молекулы имеют сложную пространственную структуру, при этом гидрофильные остатки экспонированны на поверхности, тогда как
гидрофобные скрыты в глубине белковой глобулы. Эпитопы, как правило, соответствуют гидрофильным поверхностным структурам, содержащим циклические остатки, которые придают эпитопу пространственную индивидуальность. При свертывании белковой глобулы могут сближаться остатки, отдаленные друг от друга в линейной последовательности. Это обстоятельство определяет существование двух типов эпитопов — линейных и конформационных. Первые образованы линейной последовательностью аминокислотных остатков, вторые — отдаленными друг от друга остатками, сближенными на поверхности белковой глобулы. Нарушение третичной структуры белка, вызванное разрывом дисульфидных связей или денатурацией, приводит к исчезновению конформационных детерминант при полной сохранности линейных.
Существование конформационных детерминант можно продемонстрировать на примере молекулы лизоцима.

Нативная молекула этого белка содержит петлю, соответствующую последовательностям 60–83, скрепленную дисульфидной связью. При иммунизации лизоцимом петля выступает как иммунодоминантный эпитоп. Разрыв связи приводит к распрямлению петли, ликвидации эпитопа и нарушению взаимодействия с антителами к нативной молекуле. Нативные и линейные эпитопы могут сосуществовать в одной молекуле, как, например, в молекуле миоглобина, содержащей конформационный эпитоп, захватывающий остатки 34, 53 и 113, а также ряд линейных эпитопов.

Взаимоотношение линейных и конформационных эпитопов можно наглядно проиллюстрировать на примере синтетических полипептидов, содержащих остатки Glu, Ala и Tyr. В одном из таких пептидов триада Glu–Ala–Tyr повторяется последовательно и многократно, причем полипептидная цепь имеет α-спиральную конфигурацию. В другом полипептиде к линейному пептиду, образованному остатками Ala, «подшивали» боковые группы Glu–Ala–Tyr. К пептидам обоих типов получали антитела.
Линейный полипептид формирует коформационный эпитоп
Glu:Ala:Tyr :Glu:Ala:Tyr :Glu:Ala:Tyr :Glu:Ala:Tyr :Glu:Ala:Tyr :Glu:Ala:Tyr:
Разветвленный полипептид формирует линейные
(секвенциальные) эпитопы
Tyr Tyr Tyr Tyr
Ala Ala Ala Ala
Glu Glu Glu Glu
Ala:Ala:Ala:Ala:Ala:Ala:Ala:Ala:Ala:Ala:Ala:Ala:Ala:Ala:Ala:Ala:Ala:Ala:
Оказалось, что при реакции антител с пептидами не наблюдалось перекрестных реакций, т.е. пептид 1 не реагировал с антителами к пептиду 2 и наоборот. Реакция полипептидов второго типа со своими антителами блокировалась трипептидом Glu–Ala–Tyr. Реакция полипептидов первого типа со своими антителами блокировалась линейными пептидами, образованными как минимум 17 чередующимися остатками Glu, Ala, Tyr, формирующими α-спираль. Таким образом, антитела к линейному полипептиду были направлены к конформационной детерминанте, формируемой α-спиралью, а антитела к разветвленному полипептиду — к линейной детерминанте.
Существование конформационных эпитопов демонстрирует важность распознавания не только линейной структуры, но и пространственной
конфигурации молекул. Это положение можно проиллюстрировать на примере перекрестной реактивности гаптенов различной химической природы
с белковыми эпитопами антиидиотипических антител (т.е. анти-антител, распознающих некоторые идиотопы антител, специфичных к этим гаптенам). Перекрестная реактивность в этом случае основана на том, что конфигурация активного центра (и в определенной степени идиотопов) комплементарна конфигурации как эпитопа иммуногена, так и антиидиотопа. Следовательно, эпитоп и антиидиотоп, если не идентичны, то сходны друг с другом по конфигурации.
Анализ специфичности конформационных детерминант с помощью методов, разработанных при изучении гаптенов и применяемых для линейных (секвенциальных) детерминант , практически невозможен. При извлечении из целой молекулы конформационная детерминанта изменяет свою
конфигурацию и теряет способность реагировать с антителами. Эти эпитопы изучают, подбирая белки (от родственных видов, мутантных линий
клеток и особенно часто — синтетические белки), отличающиеся единичными заменами аминокислотных остатков. При этом для оценки реакции
часто используют, твердофазный иммуноферментный анализ, позволяющий достичь высокой производительности и степени стандартизации.
Размеры конформационных эпитопов варьируют даже в более широких пределах, чем линейных эпитопов: они соответствуют 6–17 аминокислотным остаткам. Так, в молекулах миоглобина размер конформационного эпитопа составляет 6–8, а в молекуле бычьего сывороточного альбумина —
10–12 остатков. Расположение частей конформационных детерминант на большом расстоянии в линейной структуре молекулы описано, например,
для аллотипических детерминант иммуноглобулинов, уже упоминавшихся эпитопов миоглобина и т.д. Как в линейных, так и в конформационных
эпитопах роль отдельных остатков может существенно варьировать. Так, в формировании описанной выше петлевой детерминанты лизоцима клю-чевую роль играет остаток в положении 68. В данном случае проявляется фактор гибкости эпитопа, позволяющий «подогнать» конфигурацию конформационного эпитопа, к структуре активного центра антител. Подгонка происходит за счет остатков, обеспечивающих эту гибкость (например, пролина).
Важным и практически неизученным является вопрос об активных факторах, обусловливающих иерархию эпитопов и реализуемых через ингибирование одними эпитопами иммунного ответа на другие эпитопы, что может происходить с участием супрессорных клеток.
Несмотря на то что знания о структурных основах конформационных и линейных эпитопов белков пока далеко не полные, их достаточно, чтобы с высокой долей уверенности прогнозировать, какие участки белковой молекулы окажутся антигенными детерминантами. В основе расчетов лежат различные соображения. В первую очередь выбираются участки с высоким соотношением гидрофильных и гидрофобных остатков (условие локализации эпитопа на поверхности молекулы), а также с аминокислотными остатками, придающими этому участку гибкость. Детерминанты, сконструированные на основе такого расчета (с использованием компьютерных программ), синтезируются и с успехом используются в серодиагностике и для приготовления искусственных вакцин.
Взаимодействие антигенов и антител
[править]Определение иммунитета. «Формула» иммунного ответа
[править]АНАТОМИЯ И ЦИТОЛОГИЯ ИММУННОЙ СИСТЕМЫ
[править]Органы, ткани и клетки иммунной системы
[править]Анатомический синоним иммунной системы — лимфоидная система. В организме взрослого здорового человека содержится около 1013 лимфоцитов, то есть примерно каждая клетка тела — лимфоцит. Анатомомический принцип устройства иммунной системы — органно-циркуляторный. Это значит, что есть ряд специализированных органов с организованной внутренней структурой. При этом лимфоциты не «сидят» в лимфоидных органах постоянно(в отличие от, например, гепатоцитов в печени), а интенсивно рециркулируют между лимфоидными органами и пелимфоидными тканями через лимфатические сосуды и кровь: через один лимфатический узел в 1 ч проходит ~109 лимфоцитов. Из общего количества лимфоцитов организма в каждый момент времени в крови находится только 0,2—2 %. Миграция лимфоцитов из крови в ткани и из тканей в кровь происходит сквозь стенку сосудов, и механизм этой миграции включает в себя специфические взаимодействия определенных молекул на мембране лимфоцита с определенными молекулами на мембране клеток эндотелия стенки сосудов.(такие молекулы называют адгезинами, селектинами, интегринами)."Эти взаимодействия происходят не в каком придется месте сосуда, а в определенных местах, например в лимфатических узлах — это эндотелий посткапиллярных венул. Процесс миграции лимфоцитов, конечно же, не носит характер случайного передвижения, а строго регулируется рядом факторов, зависящих от местных тканевых и системных физиологических «задач» организма. Выделяют следующие органы и ткани иммунной системы:
- Кроветворный костный мозг — центральный орган всего кроветворения, место обитания пула стволовых кроветворных клеток.
- Тимус.
- Селезенка.
- Лимфатические узлы.
- Лимфоидная ткань, ассоциированная с желудочно-ки шечным трактом (GALT — gut-associated lymphoid tissues). Это миндалины, аденоиды, аппендикс, пейеровы бляшки. Особой субпопуляцией являются внутриэпителиальные лимфоциты слизистой оболочки кишки (IEL — intra-epitelial lymphocytes).
- Лимфоидная ткань, ассоциированная с бронхами/бронхиолами (BALT — bronchial-associated lymphoid tissue). IEL слизистой оболочки дыхательной системы.
- Лимфоидная ткань других слизистых оболочек (MALT — mucosal-associated lymphoid tissue).
- Особые субпопуляции лимфоцитов в печени, которые в качестве лимфоидного барьера «обслуживают» кровь воротной вены, несущей все внешние, всосавшиеся в кишечнике вещества.
- Лимфоидная подсистема кожи, включающая в себя субпопуляцию особых диссеминированных внутриэпителиальных лимфоцитов кожи (IEL) и регионарные лимфатические узлы и сосуды лимфодренажа.
- Периферическая кровь — транспортно-коммуникацион-ный компонент иммунной системы.
Кроветворный костный мозг и тимус называют центральными органами иммунной системы потому, что на их территории происходит дифференцировка лимфоцитов из стволовой кроветворной клетки, так называемый лимфопоэз. Лимфопоэз — это дифференцировка лимфоцитов от стволовой кроветворной клетки до зрелого неиммунного лимфоцита. Зрелые неиммунные лимфоциты локализуются в периферических лимфоидных органах и циркулируют между ними через кровь. На территории периферических лимфоидных органов зрелые неиммунные лимфоциты вступают в контакты с антигенпредставляющими клетками. Если антигенраспознающий рецептор лимфоцита связывает комплементарный антиген на территории периферических лимфоидных органов, где в норме создаются все необходимые условия (корецепторные взаимодействия) для начала развития иммунного ответа, то лимфоцит вступает на путь додифференцировки в режиме иммунного ответа, то есть начинает пролиферировать и продуцировать эффекторные молекулы (цитокины, перфорин, цитолизины, гранзимы и др . в зависимости от субпопуляции лимфоцита). Дифференцировку лимфоцитов на периферии после распознавания антигена называют иммуногенезом. Зрелые неиммунные лимфоциты по-английски называют naive ^наивные) или virgine{девственные)/ Обязательным процессом в начале иммуногенеза лимфоцитов в периферических лимфоидных органах является пролиферация клонов лимфоцитов, распознавших антиген . В результате иммуногенеза развиваются клоны иммунных или эффекторных лимфоцитов, которые в англоязычной литературе называют armed (вооруженные) или effector (эффекторные) лимфоциты. Иммунные лимфоциты распознают антиген и организуют деструкцию в различных периферических тканях организма, где этот антиген присутствует. В костном мозге проходит дифференцировка всех лейкоцитов крови . По выходе из костного мозга в периферические ткани лейкоциты в норме уже никогда не будут пролиферировать (в отличие от лимфоцитов) . В ответ на адекватные сигналы 'извне они лишь будут активированы к выполнению своих предназначенных в процессе дифференцировки функций.

У взрослых млекопитающих в костном мозге сосредоточены кроветворные стволовые клетки. Ранее существовало представление о локализации стволовых клеток и ранних предшественников преимущественно в периферической части просвета костного канала, но недавние исследования показали, что стволовые клетки и клетки-предшественники равномерно распределены по всему костному мозгу. Клетки различных типов распределяются в виде островков. Размножающиеся и созревающие клетки располагаются в петлях, образуемых ретикулярными клетками. По мере созревания клетки продвигаются к центру, где проникают в синусоиды и поступают в кровоток.
Рассмотрим костный мозг в качестве органа лимфопоэза. На долю лимфоидных клеток в нем приходится 10–15% ядросодержащих клеток. Среди них 60% — созревающие клетки, а остальные — зрелые клетки, готовые к эмиграции или поступившие из кровотока. У мышей ежедневно костный мозг покидает около 50% общего числа лимфоидных клеток. Обратный приток лимфоцитов из крови в 10 раз меньше. Содержание в костном мозге В-лимфоцитов выше, чем Т-лимфоцитов (65–70 и 20–30% соответственно).
Среди клеток В-ряда преобладают пре-В-клетки, содержащие μ-цепь иммуноглобулина в цитоплазме (у человека — 5,8%), тогда как В-клетки, несущие IgM на поверхности, составляют 2,5% кариоцитов костного мозга. В костном мозгу присутствуют В-клетки памяти, содержащие мембранный IgG или (значительно реже) IgA (всего 1,3%), а также плазматические клетки-антителопродуценты (1–2%). В-клеточная ветвь кроветворения отличается высокой производительностью: за сутки в костном мозгу образуется значительно больше В-клеток, чем необходимо для обновления популяции В-лимфоцитов (у мышей — 20–50 млн). Очень много клеток гибнет в процессе перестройки генов иммуноглобулинов, а также на стадии незрелых В-клеток в процессе отрицательной селекции вследствие выбраковки аутоспецифических клонов.
Клетки Т-ряда представляют исключительно зрелые лимфоциты, поступающие из кровотока. Преобладают (60% от числа CD3+клеток) Т-клетки необычного фенотипа CD3+CD4-CD8-, сходные с Т-клетками печени, но не идентичные им. Допускается, что эти клетки развиваются вне тимуса. Среди обычных Т-клеток CD8+ клеток больше, чем CD4+ клеток: соотношение CD4+/CD8+ в костном мозгу составляет 0,5–1,0 (в крови — 1,5–2,0).
Оба типа моноположительных клеток происходят из крови. Их необычное соотношение объясняют различиями в способности клеток этих субпопуляций мигрировать в костный мозг. Поступление Т-клеток (в том числе незрелых тимоцитов) в костный мозг значительно усиливается при стрессе, что объясняют влиянием глюкокортикоидов.
Сосуществование в костном мозгу развивающихся и приходящих из крови зрелых форм лимфоцитов свидетельствует о том, что костный мозг совмещает признаки центрального и периферического лимфоидного органов.
Развитие костного мозга
Костный мозг у человека появляется впервые на 2-м месяце внутриутробного периода в ключице эмбриона, затем на 3-4 -м месяце он образуется в развивающихся плоских костях, а также в трубчатых костях конечностей - лопатках, тазовых костях, затылочной кости, ребрах, грудине, костях основания черепа и позвонках, а в начале 4-го месяца развивается также в трубчатых костях конечностей. До 11-й недели это остеобластический костный мозг, который выполняет остеогенную(костеобразующюю) функцию. В данный период костный мозг накапливает стволовые клетки, а клетки стромы с остеогенными(костеобразующими) потенциями создают микросреду, необходимую для дифференцировки стволовых кроветворных клеток. У 12-14-недельного эмбриона человека происходят развитие и дифференцировка вокруг кровеносных сосудов гемопоэтических клеток. У 20-28-недельного плода человека в связи с интенсивным разрастанием костного мозга отмечается усиленная резорбция костных перекладин остеокластами, в результате чего образуется костномозговой канал, а красный костный мозг получает возможность расти в направлении эпифизов. К этому времени костный мозг начинает функционировать как основной кроветворный орган, причем большая часть образующихся в нем клеток относится к эритроидному ряду гемопоэза. У зародыша 36 нед. развития в костном мозге диафиза трубчатых костей обнаруживаются жировые клетки. Одновременно появляются очаги кроветворения в эпифизах.
Строение красного костного мозга
Костный мозг - единственная ткань взрослого организма, в норме состоящая из незрелых, недифференцированных и низкодифференцированных клеток, так называемые стволовые клетки, близких по строению к эмбриональным клеткам. Все другие незрелые клетки, например незрелые клетки кожи, все же имеют большую степень дифференцировки и зрелости, чем клетки костного мозга, и имеют уже заданную специализацию. Красный, или кроветворный, костный мозг у человека находится в основном внутри тазовых костей и, в меньшей степени, внутри эпифизов длинных трубчатых костей и в ещё меньшей степени внутри тел позвонков. Он состоит из фиброзной ткани стромы и собственно кроветворной ткани. В кроветворной ткани костного мозга выделяют три ростка, или три клеточных линии (англ. cell lines), три популяции клеток, являющиеся родоначальниками соответствующих клеток крови - лейкоцитарный, эритроцитарный и тромбоцитарный ростки. Все эти клеточные ростки имеют общих предков - так называемые плюрипотентные стволовые клетки-предшественники, которые при созревании и дифференцировке идут по одному из трех путей развития.
Костный мозг в норме защищен барьером иммунологической толерантности от уничтожения незрелых и созревающих клеток собственными лимфоцитами организма. При нарушении иммунологической толерантности лимфоцитов к клеткам костного мозга развиваются аутоиммунные цитопении, в частности аутоиммунные тромбоцитопении, аутоиммунные лейкопении, и даже апластическая анемия. Количество полипотентных стволовых клеток, то есть клеток, которые являются самыми первыми предшественниками в ряду кроветворных клеток, в костном мозге ограничено, и они не могут размножаться, сохраняя плюрипотентность, и тем самым восстанавливать численность. Ибо при первом же делении плюрипотентная клетка выбирает путь развития, и ее дочерние клетки становятся либо мультипотентными клетками, у которых выбор более ограничен (только в эритроцитарный или лейкоцитарный ростки), либо мегакариобластами и затем мегакариоцитами - клетками, от которых отшнуровываются тромбоциты.
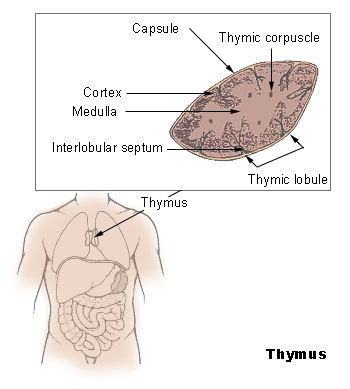
Тимус (вилочковая, или зобная, железа), эндокринная железа, играющая важнейшую роль в формировании иммунитета. Она стимулирует развитие Т («тимусных») – клеток как в собственной ткани, так и в лимфоидной ткани других частей тела. Т-клетки «атакуют» попавшие в организм чужеродные вещества, осуществляют контроль над выработкой антител против болезнетворных агентов, влияют на другие защитные реакции организма.
Тимус имеется у всех позвоночных животных, но его форма и местоположением могут быть различны. У человека тимус состоит из двух долей, расположенных в верхней части грудной клетки сразу за грудиной. У пресмыкающихся и птиц он обычно имеет вид двойной цепочки, тянущейся по обеим сторонам шеи.
Развитие тимуса. У человека тимус формируется на 6-й неделе внутриутробной жизни, развиваясь, как и у других млекопитающих, из двух сегментов, которые объединяются, образуя единый орган, состоящий из двух долей. У австралийских сумчатых животных две половины тимуса так и остаются отдельными органами.
Наибольших размеров по отношению к весу тела тимус человека достигает к моменту рождения (около 15 г). Затем он продолжает расти, хотя уже гораздо медленнее, и в период полового созревания достигает максимального веса (примерно 35 г) и размеров (около 75 мм в длину). После этого начинается постепенное уменьшение железы, которое продолжается всю остальную жизнь. У разных видов животных этот процесс протекает с разной скоростью, и у некоторых (например, у морских свинок) относительно крупный тимус сохраняется на протяжении всей жизни.
Структура тимуса Тимус состоит из двух основных частей — коры и мозгового вещества. В коре выделяют наружный, субкапсулярный слой, глубокую кору и кортикомедуллярную зону (или кортикомедуллярное сочленение). Тимус покрыт соединительнотканной капсулой, от которой внутрь коры отходят междольковые перегородки, разделяющие кору на дольки. Мозговая часть тимуса не разделена на дольки. Кортикомедуллярное сочленение служит воротами тимуса, в которые входят и выходят кровеносные сосуды и нервы. Сосудистая сеть тимуса бедна («бледный орган»). Наиболее важны в функциональном отношении посткапиллярные венулы, через стенку которых в тимус проникают клетки-предшественники и выходят зрелые Т-лимфоциты.
Гистологически тимус представляет лимфоэпителиальный орган. Он имеет трехслойную структуру, включающую обычную соединительнотканную строму, эпителиальный ретикулум и лимфоидную составляющую. Эпителиальные и большая часть соединительнотканных элементов тимуса имеют местное происхождение. Лимфоциты тимуса, называемые тимоцитами, а также макрофаги, дендритные и тучные клетки происходят из клеток-предшественников, мигрирующих в этот орган из костного мозга. Тимоциты численно преобладают и являются транзиторными элементами, поскольку подавляющее большинство их покидает тимус по мере созревания.
Соединительнотканная строма формирует капсулу, междольковые перегородки и периваскулярное пространство. В последнем содержатся фибробласты, соединительнотканные волокна, макрофаги, тучные клетки, В-лимфоциты, нейтрофилы. Доля соединительнотканного пространства в тимусе очень невелика. Основной объем органа занимает эпителиальное (внутреннее) пространство — участки тимуса, ограниченные эпителиальными клетками и базальной мембраной. Эпителиальные клетки образуют трехмерный каркас — эпителиальный ретикулум, внутри которого происходят основные события, связанные с развитием Т-лимфоцитов. Таким образом эпителиальная составляющая тимуса фактически представляет паренхиму органа. В эпителиальном каркасе кортикомедуллярной зоны содержатся макрофаги, а в мозговом веществе — еще и дендритные клетки.
Специфическая функция тимуса состоит в обеспечении развития (созревания, селекции, дифференцировки) Т-лимфоцитов. В этом задействованы преимущественно эпителиальные клетки. Определенный вклад в этот процесс вносят соединительнотканные элементы и дендритные клетки тимуса.
Гематотимический барьер. Тимус изолирован от проникновения в него клеток извне с помощью гематотимического барьера. Этот барьер состоит из трех компонентов: первый — эндотелий посткапиллярных венул. Мигрирующие клетки преодолевают его благодаря взаимному с клетками эндотелия сосудов распознаванию молекул адгезии. Установлена роль в иммиграции клеток-прешественников в тимус селектинов L и Р, α4-интегринов (VLA-4 или α4β1, α4β7). Рецепторы названных интегринов — фибронектин, VCAM-1 и MadCAM экспрессируются в зонах проникновения клеток-предшественников в тимус. В этом процессе задействованы также β2-интегрин LFA-1, β1-интегрин VLA-6 и их рецепторы ICAM-1 и ламинин соответственно. Судя по блокирующему эффекту антител, важную роль при миграции клеток в тимус играют молекулы CD44 (экспрессируемые на поверхности мигрирующих клеток и исчезающие вскоре после поступления в тимус), а также молекула VAP-1 (Vascular adhesion protein 1), экспрессируемая только в венулах тимуса. Второй компонент барьера образован макрофагами и другими клетками периваскулярного пространства. Избежать поглощенния макрофагами клеткам помогает блокада сиаловой кислотой свободных углеводных остатков их поверхностных гликопротеинов. Для перемещения в межклеточном пространстве важна экспрессия на поверхности клеток-предшественнков β1-интегринов, в частности VLA-4 и VLA-6, взаимодействующих с белками межклеточного матрикса, — соответственно фибронектином и ламинином. Продвижению клеток-предшественников способствует их инвазивность, обусловленная выделением ферментов гиалуронидазы и коллагеназы, расплавляющих межклеточный матрикс. Третий и наименее проницаемый компонент барьера — эпителиальные клетки, ограничивающие эпителиальное пространство тимуса, а также их базальная мембрана. Этот барьер преодолевается благодаря экспрессии на клетках-предшественниках Р-селектинов, взаимодействующих с молекулами GlyCAM, MadCAM, и молекулы CD44, реагирующей с гиалуронатом межклеточного матрикса. Гематотимический барьер распространяется на кору, но не на мозговое вещество тимуса, в которое могут мигрировать циркулирующие клетки крови. Полагают, что в преодолении барьера, образованного базальной мембраной, важная роль принадлежит металлопротеиназам.
Разнообразие эпителиальных клеток тимуса и их функции.
Лимфоидные клетки тимуса. Тимоциты образуют наиболее многочисленную популяцию клеток тимуса. Наименее зрелые CD4-CD8-CD3-тимоциты расположены в субкапсулярной зоне тимуса. На их долю приходится 3–5% от общего числа тимоцитов. На первой стадии (DN1) происходит чрезвычайно интенсивная пролиферация клеток. На следующих стадиях развития дваждыотрицательных клеток осуществляется перестройка V-генов TCR, экспрессия мембранных рецепторов и формирование определяемого ими первичного (т.е. не прошедшего селекции) антигенраспознающего репертуара. Все этапы развития тимоцитов проходят в определенных зонах тимуса с характерным микроокружением, формируемым в наибольшей степени эпителиальными клетками и их продуктами.
Клетки с мембранным фенотипом CD4+CD8+ составляют наиболее многочисленную фракцию тимоцитов. На их долю приходится 70–75% общего числа лимфоидных клеток тимуса. Они локализуются в коре (преимущественно в ее глубоких слоях). На этой стадии происходят оба этапа селекции — положительная и отрицательная, формируется вторичный (селекционированный) антигенраспознающий репертуар, обеспечивающий распознавание пептидов в составе молекул MHC. Кортикальные тимоциты особенно чувствительны к индукции апоптоза в связи со слабой экспрессией антиапоптотических факторов. В частности, они погибают при действии глюкокортикоидов ( кортизончувствительные тимоциты). В «отобранных» тимоцитах, получивших сигналы к дальнейшему развитию от эпителиальных клеток, усиливается экспрессия антиапоптотических факторов. Одновременно возрастает экспрессия рецепторного комплекса TCR-CD3 и появляется маркер активации CD69.
В мозговом слое тимуса сосредоточены зрелые моноположительные тимоциты. На долю CD4+CD8-клеток приходится около 10% (из них 2–3% — регуляторные CD4+CD25+клетки), на долю CD4-CD8+клеток — около 5% лимфоидных клеток тимуса. Все эти клетки экспрессируют комплекс TCR–CD3 с высокой плотностью. Медуллярные тимоциты содержат так называемые Т-рецепторные эксцизионные кольца (TREC) —кольцевые молекулярные структуры, образующиеся в процессе реаранжировки V-генов в результате замыкания в кольцо участков ДНК, вырезаемых из зародышевых V-генов . Эти структуры выявляют с помощью полимеразной цепной реакции. Различают сигнальные и кодирующие эксцизионные кольца, образующиеся соответственно при реаранжировке генов δ- и α-цепей (ген TRDV локализован внутри кластера TRAV и может подвергаться перестройке дважды — при построении зрелых генов TRDV и TRAV). Они персистируют в Т-клетках некоторое время после их выхода из тимуса и служат маркером «недавних мигрантов из тимуса». Моноположительные тимоциты обладают функцией соответственно Т-хелперов и цитотоксических Т-лимфоцитов. Однако их функциональная активность выражена слабее, чем у аналогичных клеток периферического отдела иммунной системы (например, при активации они слабее секретируют IL-2 и IFNγ). Некоторые медуллярные тимоциты, по-видимому, остаются в тимусе и служат источником цитокинов, необходимых для формирования полноценного микроокружения этого органа. Остальные тимоциты покидают тимус через посткапиллярные венулы.
Перемещение созревающих тимоцитов внутри тимуса определяется градиентом хемокинов, секретируемых стромальными (преимущественно эпителиальными) клетками, а также наличием на поверхности тимоцитов соответствующих рецепторов. Хотя не все детали этого процесса изучены досконально, известно, что перемещение тимоцитов из кортикомедуллярной в субкапсулярную зоны осуществляется по градиенту SDF-1 (CXCL12), чему способствует возрастающая на этом этапе развития клеток экспрессия соответствующего хемокинового рецептора — CХСR4. На следующем этапе развития тимоциты перемещаются с поверхности коры в глубь ее. Клетки движутся в направлении мест выработки хемокина TECK (ССL17), к которому они экспрессируют рецептор CCR9. Экспрессия рецептора CCR7 на заключительном этапе внутритимусного развития Т-клеток обеспечивает их перемещение к кортикомедуллярной зоне. Эндотелиальные клетки венул, через которые осуществляется эмиграция, секретируют хемокин ELC (CCL19), распознаваемый названным CCR7. Рецептор для сфингозина необходим для обеспечения эмиграции тимоцитов в ответ на сигнал от сфингозин-1-фосфата.
Другие клеточные популяции тимуса. Помимо тимоцитов в тимусе содержатся другие клетки гематогенного происхождения — макрофаги, В-лимфоциты, дендритные, тучные и миоидные клетки. За исключением дендритных и миоидных, упомянутые клетки не отличаются по свойствам и функции от аналогичных клеток вне тимуса.
Дендритные клетки составляют один из наиболее важных в функциональном отношении типов клеток вилочковой железы. Популяция дендритных клеток тимуса содержит примерно равные количества миелоидных и лимфоидных (плазмоцитоидных) вариантов. Большинство из них дифференцируется в тимусе из предшественников, общих для них и тимоцитов, однако некоторые дендритные клетки тимуса, как полагают, имеют внетимусное происхождение. Основная функция миелоидных дендритных клеток тимуса состоит в осуществлении отрицательной селекции и формировании центральной аутотолерантности. Считают, что плазмоцитоидные дендритные клетки в тимусе, как и вне его, секретируют IFNα, однако роль этого цитокина в тимусе точно не установлена.
Миоидные клетки обладают свойствами, характерными для мышечных и, в меньшей степени, эпителиальных клеток. Они содержат десминовые филаменты, экспрессируют мышечные белки миоглобин, тропонин, распин, синаптофизин . На их поверхности присутствуют рецепторы для ацетилхолина. Миоциты локализуются, главным образом в окружении телец Гассаля и внутри них. Интерес к этой немногочисленной клеточной популяции связан с тем, что они вовлекаются в патологию при тяжелой миастении ( миастении гравис), часто сопровождающейся развитием тимом — опухолей, растущих из эпителиальных клеток тимуса.
Лимфатические узлы
[править]
Лимфатические узлы (nodi lymphatici) — наиболее многочисленные органы иммунной системы. В теле человека их количество достигает 500. Все они располагаются на пути тока лимфы и, сокращаясь, способствуют ее дальнейшему продвижению. Их основной функцией является барьерно-фильтрационная, то есть задерживание бактерий и других инородных частиц по пути тока лимфы. Кроме того, лимфатические узлы выполняют гемопоэтическую функцию, принимая участие в образовании лимфоцитов, и иммуноцитопоэтическую функцию, образуя плазматические клетки, вырабатывающие антитела. Форма лимфатических узлов может быть самой разнообразной: округлой, овоидной, вытянутой или бобовидной. Размер варьируется от 25 до 50 мм.
Анатомия и физиология лимфатического узла
[править]
Лимфатические узлы представляют собой образования округлой, овальной, бобовидной, реже лентовидной формы размерами от 0,5 до 50 мм и более. Лимфоузлы окрашены в розовато-серый цвет. Лимфатические узлы располагаются по ходу лимфатических сосудов, как правило, гроздьями до десяти штук, возле кровеносных сосудов, чаще — возле крупных вен.
Лимфатический узел имеет выпуклую сторону, к которой в количестве 4—6 подходят приносящие лимфатические сосуды (vas lymphaticum afferena) , то есть поставляющие лимфу к лимфатическим узлам, и вогнутую сторону, называемую воротами узла (hilum). Через ворота в узел проникают питающие его артерии и нервы. Из них же выходят выносящие лимфатические сосуды (vas lymphaticum efferens), выводящие лимфу из узла, и вены. Лимфатический узел покрывает капсула (capsula), образованная соединительной тканью с примесью гладких мышечных волокон, что обеспечивает способность узла сокращаться. От капсулы вглубь узла направляются так называемые перекладины, или трабекулы (trabecula) , которые вместе с ретикулярными клетками и волокнами принимают участие в образовании стромы. В петлях стромы находятся клеточные элементы лимфатического узла, преимущественно лимфоциты. Промежутки между трабекулами заполнены лимфоидной тканью. У выпуклой стороны узла клетки уплотняются и образуют корковое вещество (cortex), внутри от которого располагается мозговое вещество (medulla). В нем содержатся заполненные лимфой синусы, окружающие отгороженные от коркового вещества элементы лимфоидной ткани, называемые мозговыми тяжами. Внутри узла лимфа циркулирует по системе синусов. Приносящие сосуды поставляют лимфу в краевой синус, представляющий собой щель между корковым веществом и капсулой. Он соединяется с промежуточными корковыми синусами (sinus corticalis), из которых лимфа попадает в промежуточные мозговые синусы (sinus medullaris). Мозговые синусы, объединяясь, образуют воротный синус, через который лимфа поступает в ворота узла, а оттуда — в выносящие лимфатические сосуды. В самом корковом веществе находятся лимфоидные узелки (nodulus lymphaticus), залегающие ближе к капсуле и имеющие округлую форму. Часть этих узелков имеет реактивные, или светлые, центры. Лимфоидная ткань, заполняющая промежутки между узелками, называется межузелковой, а лимфоидная ткань, располагающаяся внутри от узелков, — паракортикальной зоной (paracortex).
В наружной части коры есть округлые образования — лимфоидные фолликулы, служащие местом сосредоточения В-лимфоцитов. В покоящихся лимфоузлах они имеют равномерную структуру, и их обозначают как первичные фолликулы. При иммунном ответе в фолликул, помимо В-лимфоцитов, мигрируют Т-клетки, в нем формируются центры размножения — зародышевые центры. Такой фолликул называют вторичным. Ключевую роль в формировании и функционировании фолликулов и развивающихся в них зародышевых центров играют фолликулярные дендритные к летки, по происхождению не имеющие отношения к обычным дендритным клеткам и сходные с ними только по морфологии. Эти клетки имеют местное мезенхимальное происхождение.
Формирование Т- и В-зон лимфатических узлов, как и других вторич-ных лимфоидных органов, а также мозгового слоя тимуса определяется взаимодействием лимфоидных клеток и предшественников стромальных клеток, осуществляемое в эмбриогенезе. Ключевая роль в нем принадлежит мембранным лимфотоксинам (LT) — цитокинам семейства TNF — и их рецепторам. Из костного мозга в зачаток лимфатических узлов и других лимфоидных органов мигрируют специальные лимфоидные клетки, обозначаемые как клетки-индукторы лимфоидной ткани — LTIC (Lymphoid tissue inducing cells). Их мембранный фенотип — CD4+CD3-CD45+α4β7+IL-7Rα+LTαβ+CXCR5+. LTIC экспрессируют дифференцировочный фактор RORγt (Retinoid-acid-receptor-related orphan receptor— орфановый рецептор, родственный рецептору ретиноидной кислоты) и транскрипционный фактор Id2. Судя по мембранным молекулам, эти клетки имеют костно-мозговое лимфоидное происхождение, но не относятся к зрелым субпопуляциям лимфоцитов. LTIC содержат на своей поверхности мембранную форму LTαβ— тример, включающий 2 трансмембранные молекулы LTβи 1 молекулу LТα, расположенную внеклеточно. Другая сигнальная молекула LTIC, также относящаяся к семейству TNF, — RANKL (Recerptor activa-tor of NFκB-ligand). В образовании лимфоидных органов участвуют также клетки-инициаторы лимфоидной ткани — LTIN, которые имеют фенотип CD4-CD3- IL-7Rα-CD11b+CD11c+, свидетельствующий об их родстве с дендритными клетками. С этими двумя типами клеток взаимодействуют предшественники стромальных клеток — клетки-организаторы лимфоидной ткани — Lto.
LTβи RANKL распознаются рецепторами семейства TNFR на стромальных клетках, в результате чего в них генерируется сигнал, вызывающий экспрессию генов IL-7, хемокинов (CXCL13, CCL19, CCL21) и фактора TRANCE (TNF-related activation-induced cytokine). Все эти факторы действуют на лимфоидные клетки; кроме того, они привлекают зрелые лимфоциты, обеспечивают их жизнеспособность и способствуют их кластеризации с образованием зачатка фолликула. Затем мигрирующие в зачаток В-, Т- и NK-лимфоциты разделяются пространственно. К этому моменту в формирующемся органе появляются дендритные клетки, играющие роль организующего начала при формировании первичных лимфоидных фолликулов.
У взрослых организмов способность фолликулярных дендритных клеток к выработке хемокинов и факторов выживания поддерживается благодаря контактам с В-лимфоцитами, стимулирующими эту способность у дендритных клеток. Таким образом, В-лимфоциты в определенной степени сами формируют свое микроокружение. У мышей, дефектных по генам лимфотоксинов или их рецепторов, не развиваются фолликулярные дендритные клетки и не формируются лимфоидные фолликулы, а при определенной комбинации дефектов не образуются лимфатические узлы.
Т-клетки в лимфатических узлах располагаются в паракортикальных зонах, находящихся в глубоких слоях коры. Они окружают посткапиллярные венулы, через которые в ткань лимфатичекого узла из кровотока мигрируют лимфоциты. В отсутствие тимуса (при генетических дефектах или после тимэктомии сразу после рождения) эти зоны не формируются. Паракортикальные зоны служат нишами для наивных Т-лимфоцитов: стромальные клетки обладают способностью привлекать их, секретируя хемокины CCL19 (ELC) и CCL21 (SLC), к которым Т-клетки имеют рецептор (CCR7). Жизнеспособность мигрировавших Т-лимфоцитов поддерживает-ся IL-7 — одним из главных факторов выживаемости наивных Т-клеток. Помимо соединительнотканных клеток, в формировании ниши для Т-лимфоцитов участвуют дендритные клетки (истинные, происходящие из костного мозга). Поскольку эти дендритные клетки обычно охватывают своими отростками Т-лимфоциты, их называют интердигитальными (межпальцевыми) клетками. Интердигитальные клетки также продуцируют CCL19 и CCL21. TCR распознают на поверхности интердигитальных дендритных клеток молекулы MHC, несущие аутологичные пептиды. Это также повы-шает выживаемость наивных Т-лимфоцитов . При распознавани в составе этих молекулярных комплексов чужеродных пептидов, Т-клетки активируются.
Пространство между фолликулами и вне паракортикальных зон занято смешанной популяцией лимфоцитов, включающей как Т-, так и В-лимфо-циты. Здесь эти клетки контактируют между собой, что важно для развития иммунного ответа. Лимфоциты пребывают в лимфатических узлах временно. Они постоянно рециркулируют. Соотношение CD4+и CD8+Т-клеток, а также других субпопуляций Т-лимфоцитов в лимфатических узлах примерно соответствует таковому в крови.
Мозговая зона лимфатических узлов содержит мозговые шнуры, между которыми расположены медуллярные синусы. В шнурах содержатся лимфоциты обоих классов. В ходе иммунного ответа здесь сосредоточивается значительная часть плазматических клеток. В синусах расположена лимфа, содержащая лимфоциты. Эта лимфа оттекает по эфферентным сосудам и впадает в кровеносную систему.
Селезенка
[править]
СЕЛЕЗЕНКА, самый крупный лимфоидный орган, имеющий овальную уплощенную форму, похожий на железу и расположенный в левой верхней части брюшной полости, позади желудка. Она соприкасается с диафрагмой, поджелудочной железой, толстой кишкой и левой почкой. Селезенка не относится к жизненно важным органам, и врожденное ее отсутствие или хирургическое удаление не оказывает глубокого влияния на жизнеспособность и рост организма.
Селезенка служит иммунным барьером на путях гематогенного распространения патогенов и других чужеродных агентов. Ее функции более разнообразны, чем функции лимфатических узлов. Помимо функций органа иммунной системы она участвует в удалении старых лимфоцитов, регулирует объем циркулирующей крови, а у ряда животных служит органом гемопоэза. Селезенка окружена капсулой, от которой отходят трабекулы, несущие артерии. Приток лимфы через афферентные сосуды отсутствует. Через ворота из органа выходят вены. Основу селезенки составляет красная пульпа, обеспечивающая гомеостаз эритроцитов. Красную пульпу делят на синусоиды (включают все элементы крови) и губчатые образования (богаты макрофагами, лимфоцитами и плазматическими клетками). В красную пульпу мигрируют NK-клетки, практически отсутствующие в белой пульпе (как и в лимфатических узлах). Из Т- и В-лимфоцитов в красной пульпе преобладают эффекторные клетки и клетки памяти. Поскольку в красную пульпу мигрируют некоторые плазматические клетки, она принимает участие в эффекторной фазе гуморального иммунного ответа.
Красная пульпа содержит вкрапления — зерновидные тельца, представляющие собой белую пульпу, окруженную краевым (маргинальным) синусом. Именно белая пульпа выполняет функции вторичного лимфоидного органа. Строение белой пульпы во многом сходно со строением лимфатического узла . Ткань белой пульпы формируется вокруг артериолы. К ней непосредственно примыкает параартериальная муфта, в которой локализуются Т-клетки (т.е. муфта служит тимусзависимой зоной, аналогом паракортикальных зон лимфатических узлов). Муфту окружает пространство, занятое лимфоцитами обоих классов. В этом пространстве ближе к периферии белой пульпы расположены лимфоидные фолликулы, по своей структуре и функциям идентичные фолликулам лимфатических узлов и других образований периферической лимфоидной ткани.
Закономерности формирования и функционирования фолликулов в качестве ниш для Т- и В-лимфоцитов в селезенке сходны с таковыми в лимфатических узлах (различия — в деталях). Периферический отдел белой пульпы, граничащий с красной пульпой, занят краевой маргинальной) зоной, в которой преобладают В-лимфоциты (в основном MZB-клетки ). В маргинальную зону открываются капилляры, отходящие от центральной артериолы, причем кровь изливается непосредственно в этот участок селе-зеночной ткани. В маргинальной зоне происходит обмен клетками между белой и красной пульпой.
Печень
[править]
Печень — это самый крупный внутренний орган, занимающий большую часть брюшной полости. Вес печени взрослого человека составляет 1200 — 1500 г. Миллиарды клеток печени постоянно выполняют множество функций, направленных на поддержание чистоты и постоянства внутренней среды организма. Печень является фильтром нашего организма, перед которым стоит задача не допустить ядовитые, опасные вещества в общий кровоток. Печень — это главный форпост, который принимает на себя весь поток веществ, поступающих в нее из кишечника по воротной вене. Ни одно из съеденных или выпитых нами веществ не может попасть в системный кровоток, минуя печень.
Печень выполняет важные иммунные функции, что вытекает из следующих фактов:
- печень - мощный орган лимфопоэза в эмбриональном периоде;
- аллогенные трансплантаты печени отторгаются менее интенсивно, чем другие органы;
- толерантность к вводимым перорально антигенам можно индуцировать только при нормальном физиологическом кровоснабжении печени и не удаётся индуцировать после операции по созданию портокавальных анастомозов;
- печень синтезирует белки острой фазы (СРБ, MBL и др.), а также белки системы комплемента;
- в печени содержатся разные субпопуляции лимфоцитов, в том числе уникальные лимфоциты, сочетающие признаки T- и NK-клеток (NKT-клетки).
Неинкапсулированная лимфоидная ткань слизистых оболочек. Иммунные подсистемы слизистых оболочек, кожи и других тканей
[править]Лимфоидная ткань слизистых оболочек Через слизистые оболочки в организм с наибольшей вероятностью поступают экзогенные потенциально агрессивные субстанции. Выделяют 3 основные системы органов, контактирующих с внешней средой — пищеварительный, дыхательный и урогенитальный тракты, а также малые протоки экзокринных желез — слюнных, слезных, сальных, потовых. Наибольшая нагрузка при этом ложится на пищеварительный тракт. Все эти наиболее уязвимые для биологической агрессии поверхности организма имеют хорошо развитое «иммунологическое оснащение». Иммунологический аппарат слизистых оболочек представлен как организованными тканевыми структурами, так и диффузной лимфоидной тканью.
Различают афферентный и эфферентный разделы лимфоидной ткани слизистых оболочек. Первый, ответственный за прием и обработку иммунологической информации, включает преимущественно организованные лимфоидные структуры. Эфферентное звено включает диффузные элементы лимфоидной ткани. Структурированную лимфоидную ткань обозначают как ассоциированную со слизистыми оболочками (MALT — Мucosa-associated lymphoid tissue). Лимфоидные структуры всегда присутствуют в пищеварительном тракте и с меньшим постоянством — в других слизистых оболочках.
Ранее полагали, что поступление антигенов во внутреннюю среду организма связано исключительно с нарушением целостности барьеров. Однако недавно было установлено, что чужеродные молекулы и агенты в норме непрерывно поступают в организм через слизистые оболочки. Их транспорт осуществляют специализированные клетки эпителия — М-клетки (от microfold). М-клетки присутствуют в составе фолликулярного эпителия, который выстилает внутреннюю поверхность слизистой оболочки над местами расположения лимфоидных фолликулов или пейеровых бляшек . Эти клетки покрывают значительную часть поверхности лимфоидных структур слизистых оболочек (около 10% поверхности пейеровых бляшек). Микроскладки, давшие название этим клеткам, увеличивают поглощающую поверхность. М-клетки лишены слоя слизи, покрывающего другие эпителиальные клетки слизистых оболочек. Маркер М-клеток — рецептор лектина улитки европейской I (Ulex europeus) — UEAR1. Основное назначение М-клеток состоит в активном транспорте антигенного материала (включая микробные тела) из полости органа в лимфоидные структуры. Механизм транспорта пока неясен, но он не имеет отношения к MHC-зависимому процессингу антигенов. М-клетки имеют форму колокола, вогнутая часть которого обращена в сторону лимфоидных фолликулов, причем к М-клеткам непосредственно примыкает купол (dome) пейеровых бляшек или единичных фолликулов — пространство, в котором расположены Т- и В-лимфоциты — преимущественно клетки памяти. Несколько глубже в куполе, наряду с этими клетками, присутствуют макрофаги и дендритные клетки.
Выделяют 2 типа организованных лимфоидных структур слизистых оболочек — пейеровы бляшки и одиночные фолликулы. Пейеровы бляшки — настоящие лимфоидные органы, которые можно рассматривать как структурные и функциональные аналоги лимфатических узлов. Они содержатся только в подвергающейся наибольшей антигенной нагрузке слизистой оболочке тонкого кишечника. В состав пейеровых бляшек входят лимфоидные фолликулы, тимусзависимые зоны и участки совместной локализации Т- и В-клеток. Основные отличия их от лимфатических узлов состоят в отсутствии капсулы, а также в наличии особой структуры — купола бляшки, расположенного непосредственно под слоем М-клеток и предназначенного для «первичной обработки» антигенного материала. В куполе сосредоточены дендритные клетки, Т- и В-лимфоциты. Дендритные клетки поглощают антигенный материал и презентируют его Т-лимфоцитам. В пейеровых бляшках происходят и другие начальные события гуморального и клеточного иммунного ответа. Дендритные клетки локализуются также в эпителиальном слое слизистой оболочки (часть диффузной лимфоидной ткани), где они могут воспринимать антигенный материал (в основном поступающий независимо от М-клеток) и доставлять его в брыжеечные лимфатические узлы для запуска в них иммунного ответа.
Лимфоидная ткань, связанная с кожей. Кожа представляет собой барьерную ткань. Благодаря наличию многослойного ороговевающего эпителия она обладает большей прочностью по сравнению со слизистыми оболочками, содержащими однослойный неоро-говевающий эпителий. Именно поэтому через кожу поступает значительно меньше чужеродного материала, чем через слизистые оболочки. Кроме того, кожа лишена М-клеток, что исключает принудительное поглощение через нее антигенов. Все это обусловливает меньшую степень развития лимфоидной ткани кожи.
В отличие от слизистых оболочек, кожа полностью лишена структурированной лимфоидной ткани. В ней расположены только диффузные лимфоидные элементы. Афферентное иммунное звено в коже представлено двумя вариантами дендритных клеток — обычными миелоидными дендритными клетками, аналогичными таковым в слизистых оболочках, и клетками Лангерганса. Особенность последних — наличие гранул Бирбека и экспрессия на поверхности клетки лектинового рецептора лангерина (CD208). Оба типа дендритных клеток поглощают чужеродный материал, обрабатывают его и, мигрируя в региональные лимфатические узлы, презентируют Т-лимфоцитам.
Эфферентная составляющая лимфоидной ткани кожи сходна с эфферентным звеном слизистых оболочек. Содержание и популяционный состав лимфоидных клеток в эпителиальном (эпидермис) и субэпителиальном (дерма) слоях кожи, как и в слизистых оболочках, значительно различаются. В эпидермисе преобладают Т-лимфоциты, в подавляющем большинстве контактировавшие ранее с антигеном (клетки памяти и эффекторные Т-лимфоциты). В эпидермисе γδТ-клеток содержится больше, чем в кровотоке, но меньше, чем в слизистых оболочках. Значительная часть этих клеток — потомки Т-лимфоцитов, эмигрировавших из тимуса в эмбриональном периоде. Соотношение СD4+ и СD8+ Т-клеток в эпидермисе больше соответствует таковому в крови, чем в слизистых оболочках. CD4+ Т-клетки кожи экспрессируют особый маркер — молекулу CLA — адрессин, представляющий собой фукозилированный рецептор Р-селектина. Присутствие этого адрессина обеспечивает специфический хоминг несущих его Т-клеток памяти в кожу.
В дерме, как и в подслизистом слое, присутствуют практически все варианты клеток иммунной системы, включая В-лимфоциты и NK-клетки, а также клетки врожденного иммунитета. Особого внимания заслуживают эпителиальные клетки, возможно, кератиноциты. При активации бактериальными продуктами и провоспалительными цитокинами кератиноциты приобретают многие свойства макрофагов вплоть до способности к фагоцитозу и, возможно, презентации антигена клеткам памяти.
Доиммунные биологические механизмы резистентности к инфекциям.
[править]Реализация врожденного иммунитета обусловлена деятельностью многих типов клеток. Основную роль при этом играют клетки миелоидного происхождения, играющие роль классических эффекторов врожденного иммунитета. К миелоидным клеткам относят, в первую очередь, большинство лейкоцитов крови(все лейкоциты, кроме лимфоцитов). Все они развиваются в органах кроветворения (у взрослых млекопитающих, включая человека, — в костном мозгу), все проходят стадию циркуляции в составе лейкоцитов крови. Одни клетки (дендритные, тучные) циркулируют настолько кратковременно и в столь малом количестве, что при обычном определении лейкоцитарной формулы их выявить не удается. Другие клетки (нейтрофилы, моноциты) представляют основной компонент пула лейкоцитов крови. Все разновидности миелоидных клеток спонтанно мигрируют из крови в ткани, где быстро погибают (нейтрофилы) или длительно функционируют, проникая в качестве резидентных клеток практически во все органы и ткани, изменяя при этом под влиянием микроокружения свои морфофункциональные особенности (так, к тканевым формам моноцитов относят макрофаги и миелоидные дендритные клетки). Кроме того, кровоток служит депо, из которого клетки мигрируют в очаги развивающегося воспаления (например, при проникновении патогенов и т.д.), где преимущественно и реализуется их защитная функция. Таким образом, участие миелоидных клеток в обеспечении врожденного иммунитета складывается из экстренной реакции клеток, мобилизуемых из кровотока в условиях воспаления, и постоянной «фоновой» деятельности резидентных клеток. Дендритным клеткам принадлежит другая важная особенность — они обеспечивают запуск адаптивного иммунитета.
Кроветворные стволовые клетки и миелопоэз
[править]у взрослых млекопитающих, включая человека, миелопоэз происходит в костном мозгу. Все клетки крови происходят от гемопоэтических стволовых клеток. Стволовые кроветворные клетки проходят 3 стадии развития, различающиеся по способности восстанавливать кроветворение при переносе их облученным животным:
- стволовые клетки длительного действия;
- стволовые клетки короткого действия;
- мультипотентные родоначальные клетки.
Для всех стадий характерен мембранный фенотип Lin-Sca-1+c-Kit+ [Lin —линейные маркеры; Sca-1 — антиген стволовых клеток (Stem cell antigen); c-Kit — лиганд фактора стволовых клеток SCF (Stem cell factor)]. Стволовые клетки на 2-й и 3-й стадии развития несут на поверхности молекулу CD34. Этот маркер чаще всего используют в качестве идентификационного для выявления стволовых клеток и их ближайших потомков. Для гемопоэтических стволовых клеток человека характерно отсутствие линейных маркеров, нали-чие молекулы CD34 и отсутствие молекулы CD38. Последняя появляется на стадии коммитированных предковых клеток — общих лимфоидного (CLP) и миелоидного предшественников. В костном мозгу человека содержится 0,5–5% CD34+ клеток, только 1–10% из них лишены CD38, т.е. могут рассматриваться как кандидаты в стволовые клетки. Истинных стволовых клеток, т.е. клеток, способных длительно поддерживать гемопоэз in vitro или при пересадке в организм, значительно меньше — 1 на 104 Lin-CD34+Thy-1-клеток.
Стволовые клетки делятся медленно (около 5% находятся в S и G2 фазах клеточного цикла; каждая клетка делится 1 раз в 30–60 сут). Жизнеспособность стволовых клеток обеспечивается стромальными клетками костного мозга, формирующими их нишу. Большинство стволовых кроветворных клеток расположено в эндостальной части костного мозга, а также в синусоидах (соответственно — эндостальная и сосудистая ниши). Таких клеток мало в центральной части костного мозга. Основную роль в поддержании жизнеспособности и обеспечении функционирования стволовых клеток играют их контакты со специализированными остеобластами ниш. В зонах контакта происходит взаимодействие многих пар молекул, включая молекулы адгезии (интегрины и их рецепторы), мембранные цитокины (SCF и его лиганд, c-Kit), хемотаксические молекулы (хемокины и их рецепторы) и т.д. Роль растворимых факторов (цитокинов) в регуляции жизнеспособности и активности стволовых клеток невелика. Стволовые клетки входят в клеточный цикл и дифференцируются только при ослаблении связи с нишей и утрате контактов с остеобластами. Важная особенность стволовых клеток — сбалансированность процессов пролиферации и дифференцировки: на уровне популяции одна из дочерних клеток продолжает делиться, тогда как другая подвергается дифференцировке, то есть созревает. В результате пролиферирующие клетки образуют как бы ствол, от которого постоянно отделяются клетки, уходящие в дифференцировку.
Дифференцируясь, стволовые кроветворные клетки дают начало двум основным ветвям клеток крови — миелоидной и лимфоидной. Несколько схематизируя, можно сказать, что эти ветви обеспечивают развитие клеток соответственно врожденного и адаптивного иммунитета. Рассмотрим только миелоидный путь развития клеток крови. Исходные клетки этого пути развития — общие миелоидные предшественники. Они образуются как в эндостальной, так и в сосудистой нишах и отличаются от стволовых клеток отсутствием мембранной молекулы Sca-1, а от CLP — рецептора для IL-7.
Из общего миелоидного предшественника происходят все клетки крови, кроме лимфоцитов. Рассмотрим только развитие клеток врожденного иммунитета по 3 линиям дифференцировки. Наиболее важная из них — гранулоцитарно-макрофагальная, или GM-линия. Она дает начало двум дочерним линиям — моноцитарной (М-линия) и гранулоцитарной (G-линия). Вопрос о развитии эозинофилов и базофилов до конца не решен. Есть данные о наличии у них общего предшественника, дифференцирующегося впоследствии на эозинофильную и базофильную линии. С помощью традиционного морфологического подхода выделяют несколько стадий развития миелоидных клеток: миелобласты, промиелоциты, миелоциты, метамиелоциты, палочкоядерные и сегментоядерные (зрелые) формы. Клетки на 2 последних стадиях в норме присутствуют в кровотоке. Накапливается все больше свидетельств, что традиционное представление гемопоэза в виде «дерева» не точно, поскольку описаны многочисленные отклонения от сложившейся схемы. Так, известны клетки-предшественники, общие для моноцитов и В-лимфоцитов или моноцитов и Т-лимфоцитов. Гемопоэзу свойствена значительная степень пластичности.
Для дифференцировки миелоидных (как и любых других) клеток необходима экспрессия определенного набора факторов транскрипции. Эти ядерные белки обладают сродством к конкретным последовательностям ДНК в промоторных участках генов и, соединяясь с ними, обеспечивают экспрессию этих генов. Обычно с промотором соединяется целый комплекс транскрипционных факторов, среди которых есть постоянно присутствующие (конститутивные) и индуцируемые факторы; некоторые из них характерны для различных стадий развития клеток. Так, при миелопоэзе для большинства линий и стадий развития клеток выявлены относительно специфичные для них транскрипционные факторы. Например, экспрессия транскрипционного фактора Ikaros характерна для лимфоидной, но не миелоидной ветви гемопоэза. При миелопоэзе высокий уровень экспрессии фактора PU.1 необходим для развития клеток GM-линии, низкий уровень выявляют в клетках эозинофильного ряда, а в базофилах этот фактор отсутствует. Моноцитарный и гранулоцитарный ряды различаются скорее комбинацией транскрипционных факторов, чем наличием одного специфичного; нейтрофилы отличаются от моноцитов экспрессией разных изоформ фактора C/EBP. Спектры дифференцировочных факторов базофилов и других миелоидных клеток крови не перекрываются.
Незрелые кроветворные клетки легко подвергаются апоптозу. Для сохранения жизнеспособности им необходимо присутствие в микроокружении цитокинов. Основным цитокином, общим практически для всех миелоидных клеток, начиная от общего миелоидного предшественника, считают гранулоцитарно-макрофагальный колониестимулирующий фактор(GM-CSF). На ранних этапах миелопоэза сходную роль выполняет IL-3, называемый также полипоэтином. При созревании и специализации клеток для сохранения жизнеспособности им необходимы линейно-специфические цитокины: для моноцитарного ряда — моноцитарно-макрофагальный колониестимулирующий фактор (M-CSF), а для нейтрофильного — гранулоцитарный колониестимулирующий фактор (G-CSF). Подобную роль при развитии эозинофилов играет IL-5. Во всех этих случаях наряду с названными цитокинами роль фактора выживания и колониестимулирующего фактора выполняют GM-CSF и, в меньшей степени, IL-3. Базофилам для развития нужен комплекс факторов, в котором главную роль играет CSF.
Между появлением гранулоцитарно-макрофагального предшественника и его дифференцировкой на моноцитарно-макрофагальный и гранулоцитарный предшественники проходит около 5 сут — это один из самых длительных этапов миелопоэза. Следующий этап — созревание — значительно отличается по продолжительности для моноцитов и гранулоцитов: если для созревания моноцита необходимо 2–3 сут, то для созревания нейтрофильного гранулоцита — 10–12 сут. После созревания моноциты находятся в костном мозгу еще сутки и затем покидают его, поступая в кровоток. При этом клетки сохраняют способность к делению и дальнейшей дифференцировке. Нейтрофилы остаются в костном мозгу в течение 1–2 сут и выходят в кровь не просто зрелой, а старой клеткой с ограниченными способностями, неспособной к делению, индуцированной экспрессии генов и синтезу белка. Наиболее короткий промежуток времени требуется для развития в костном мозгу эозинофилов (2–4 сут). Аналогичные данные для базофилов отсутствуют.
Выход лейкоцитов из костного мозга в кровоток происходит вследствие ослабления взаимодействия хемокинов, выделяемых стромальными клетками костного мозга с рецепторами лейкоцитов. Наиболее важный хемокин, удерживающий созревающие клетки в костном мозгу, — CXC12 (SDF-1 — Stroma derived factor 1, фактор стромальных клеток 1), распознаваемый рецептором CXCR4 . Под влиянием колониестимулирующих факторов (гемопоэтинов) происходит ослабление выработки хемокинов и экспрессии их рецепторов, что позволяет созревшим клеткам покинуть костный мозг. Сегментоядерные (нейтрофильные и эозинофильные) лейкоциты пребывают в кровотоке менее 12 ч; моноциты циркулируют в течение нескольких дней. Затем клетки мигрируют из крови в ткани. Этот процесс регулируется хемокиновыми сигналами и происходит с участием молекул адгезии (селектинов, интегринов) и их рецепторов. В норме экстравазация лейкоцитов осуществляется по тем же законам, что и при воспалении, но менее интенсивно в связи с меньшей проницаемостью сосудистой стенки и более слабой хемокиновой стимуляцией.
Длительность пребывания миелоидных клеток в тканях также существенно варьирует: для нейтрофилов и эозинофилов она значительно меньше, чем для моноцитов. Так, в тканях нейтрофилы живут всего 3–5 сут, эозинофилы — 10–12 сут, тогда как моноциты (точнее, макрофаги, в которые они превращаются в тканевом микроокружении) могут находиться в тканях до нескольких лет (для разных субпопуляций макрофагов этот показатель существенно различается). Нейтрофилы, эозинофилы и базофилы мобилизуются из крови в ткани в особых экстренных случаях (острое воспаление, аллергические процессы). Моноциты/макрофаги, наоборот, играют преимущественно роль клеток, длительное время живущих и функционирующих в различных тканях. В связи с этим нужно отметить значительно более высокую производительность гранулоцитопоэза по сравнению с моноцитопоэзом. За сутки в организме человека образуется и поступает в кровоток около 1011 нейтрофилов, что по массе составляет около 100 г, т.е. примерно 0,1% от массы тела; такое же количество гранулоцитов ежедневно погибает. Производительность моноцитопоэза в 20 раз ниже: за сутки образуется и поступает в кровоток до 5×109 моноцитов. Это обусловлено значительно большей продолжительностью жизни моноцитов/макрофагов.
Существует еще по крайней мере 2 разновидности миелоидных клеток, происходящих из костного мозга, но использующих кровяное русло только в качестве кратковременного транзитного участка по пути в ткани — дендритные и тучные клетки.

Нейтрофильные сегментоядерные лейкоциты (нейтрофильные гранулоциты, или нейтрофилы) — преобладающая популяция белых клеток крови. Развитие нейтрофилов контролируется цитокинами, из которых главную роль играет G-CSF, а вспомогательную — GM-CSF, IL-3 и IL-6. Повышение содержания нейтрофилов в условиях воспаления регулируется цитокинами IL-17 и IL-23. IL-23 индуцирует образование IL-17, а он стимулирует выработку G-CSF. В крови человека содержится 2,0–7,5×109/л нейтрофилов, что составляет 50–70% от общего числа лейкоцитов крови; также в крови присутствует некоторое количество (0,04–0,3×109 /л, т.е. 1–6%) палочкоядерных форм нейтрофилов, не завершивших созревание. Ядро таких клеток не сегментировано, хотя и имеет уплотненную структуру хроматина. В кровотоке присутствует только 1–2% общего числа зрелых нейтрофилов в организме (остальные представлены в тканях, преимущественно в костном мозгу). Срок их пребывания в циркуляции составляет 7–10 ч.
После кратковременной циркуляции нейтрофилы покидают кровоток и мигрируют в ткани. Примерно 30% нейтрофилов, выходящих из кровотока, мигрируют в печень и костный мозг; около 20% — в легкие (точнее в их микроциркуляторное русло); около 15% — в селезенку. Основными хемотаксическими факторами для нейтрофилов служат лейкотриен В4 и IL-8, в небольших количествах вырабатываемые в тканях. Миграция происходит с участием молекул адгезии (β2-интегрины, Р- и Е-селектины), а также фермента эластазы, секретируемого самими нейтрофилами. Через 3–5 сут пребывания в тканях нейтрофилы подвергаются спонтанному апоптозу, т.е. запрограммированной гибели , и их фагоцитируют резидентные макрофаги, что предотвращает нанесение ущерба окружающим клеткам. В настоящее время допускается возможность превращения небольшой фракции тканевых нейтрофилов в долгоживущую форму и даже их дифференцировки в макрофаги. В целом функция тканевых нейтрофилов остается невыясненной.
Диаметр нейтрофилов составляет 9–12 мкм. Им свойственна уникальная морфология: ядро сегментированное (обычно состоит из 3 сегментов) с плотно упакованным хроматином (гетерохроматином); цитоплазма содержит нейтральные (по данным окрашивания) гранулы, что и определяет название этих клеток. Особенности хроматиновой структуры ядра(недоступность промоторных участков для дифференцировочных факторов) значительно ограничивает экспрессию генов и синтез макромолекул нейтрофилами de novo. Тем не менее, вопреки ранее существовавшим представлениям, нейтрофилы сохраняют способность к биосинтезу, хотя и в ограниченном масштабе.
Для нейтрофилов характерна экспрессия на поверхности клетки ряда молекул: CD13 (аминопептидаза N, рецептор для ряда вирусов), CD14 — рецептора для липополисахарида (ЛПС) (представлен в меньших количествах, чем на моноцитах), β2-интегринов (LFA-1, Mac-1 и p155/95); Fc-рецепторов [FcγRII (CD32) и FcγRIII (CD16)],рецепторов для компонентов комплемента (CR1, CR3 и CR4), рецепторов для хемотаксических факторов (C3aR, С5аR, рецептор для лейкотриена B4). Под влиянием ряда цитокинов (прежде всего GM-CSF) нейтрофилы экспрессируют молекулы MHC класса II (MHC-II); молекулы МНС-I экспрессируются на них конститутивно. Наиболее важные молекулы, определяющие развитие, миграцию и активацию нейтрофилов, — рецепторы для G-CSF (основного фактора, регулирующего их развитие), а также для IL-17 и IL-23, основного хемотаксического фактора — IL-8 (CXCR1, CXCR2) и хемокина, определяющего связь нейтрофилов с тканями — SDF-1 (CXCR4).
Наибольшее своеобразие свойственно гранулам нейтрофилов, представляющим разновидность лизосом. Различают 4 разновидности гранул этих клеток:
- азурофильные (первичные),
- специфические (вторичные),
- желатиназные (третичные) и
- секреторные везикулы.
Специфические гранулы содержат ферменты, проявляющие свою активность при нейтральных и слабощелочных значениях рН: лактоферрин, щелочную фосфатазу, лизоцим, а также белок BPI, связывающий витамин В12. Маркерами этой разновидности гранул служат лактоферрин и мембранная молекула CD66. В специфических гранулах содержится большое количество фермента NADPН-оксидазы, катализирующего «кислородный взрыв» и образование активных форм кислорода — главных факторов бактерицидности фагоцитов. Азурофильные гранулы содержат широкий набор гидролаз и других ферментов, активных при кислых значениях рН: миелопероксидазу, α-фукозидазу, 5’-нуклеотидазу , β-галактозидазу , арилсульфатазу , α-маннозидазу , N-ацетилглюкозаминидазу, β-глюкуронидазу, кислую глицерофосфатазу , лизоцим ( мурамилидазу), нейтральные протеазы ( серпроцидины) — катепсин G, эластазу, коллагеназу, азурацидин, а также дефензины, кателицидины, актоферрин, гранулофизин, кислые глюкозаминоглика-ны и другие вещества. Маркерами азурофильных гранул служат фермент миелопероксидаза и мембранная молекула CD63. Желатиназные (третичные) гранулы в соответствии с названием содержат желатиназу. Наконец, четвертый тип гранул — секреторные везикулы — содержат щелочную фосфатазу.
При стимуляции нейтрофилов в первую очередь происходит высвобождение содержимого секреторных пузырьков. Преодолевать базальные мембраны нейтрофилам позволяет секрет желатиназных гранул. Специфические, а затем азурофильные гранулы сливаются с фагосомами в процессе фагоцитоза (через 30 с и 1–3 мин после поглощения частицы соответственно). Комплекс бактерицидных факторов, присутствующих в гранулах, обеспечивает разрушение многих микроорганизмов. Наиболее эффективно содержимое гранул повреждает стрептококки, стафилококки и грибы (включая кандиды). Содержимое гранул, особенно азурофильных, может секретироваться в результате дегрануляции. После дегрануляции восстановления гранул не происходит.
Наряду с моноцитами/макрофагами нейтрофилы рассматривают как основные фагоцитирующие клетки. При этом нейтрофилы мигрируют из крови в очаг воспаления значительно быстрее моноцитов. Скорость мобилизации нейтрофилов дополняется их способностью развивать метаболические процессы («кислородный взрыв») в течение секунд. Все это делает нейтрофилы оптимально приспособленными для осуществления ранних этапов иммунной защиты в рамках острой воспалительной реакции.

Эозинофилы составляют небольшую часть клеток крови (у человека — 0,5–2% от числа лейкоцитов). В крови они циркулируют меньше суток (по разным данным, от 30 мин до 18 ч), после чего мигрируют в ткани и пребывают там в течение 10–12 сут. Зрелые эозинофилы представляют крупные клетки (18–20 мкм в диаметре) с сегментированным (двудольным) ядром. Они содержат крупные (до 1 мкм) эозинофильные гранулы. Помимо этих крупных гранул, называемых специфическими, или вторичными, в зрелых эозинофилах присутствуют еще три типа гранул — первичные, мелкие гранулы, а также липидные тельца.
На поверхности эозинофилов присутствуют маркерные молекулы CD9 и CD35 (рецептор для комплемента — CR1), что позволяет отличить их от нейтрофилов с помощью проточной цитометрии. Кроме того, на клеточной мембране зозинофилов содержится ряд функционально важных рецепторов для антител изотипов IgG (FcγRII, FcγRIII — соответственно CD32 и CD16) и IgE (FcεRII, или CD23), цитокинов (для IL-5, GM-CSF, IL-3 и др.) и хемокинов (в особенности рецептор для эотаксинов CCR3). На поверхности эозинофилов экспрессированы молекулы MHC, причем не только I, но и II класса, что позволяет эозинофилам в определенных ситуациях выступать в качестве АПК. Наконец, на поверхности эозинофилов представлены разнообразные молекулы адгезии, среди которых преобладают β2-, β1- и β7-интегрины и их рецепторы.
Главный щелочной белок (MBP — major basic protein), определяющий эозинофильность гранул; эозинофильный катионный белок (ECP — eosinophil cationic protein); эозинофильная пероксидаза (ЕРО — eosiophilic peroxydase) и нейротоксин, происходящий из эозинофилов (EDN — eosinophil-derived neurotoxin) — основные компоненты крупных (специфических) эозинофильных гранул. МВР (13,8 кДа) представлен в кристаллической форме и формирует сердцевину гранул. Три других белка содержатся в матриксе гранул. Для МВР и ЕСР характерна токсичность в отношении гельминтов, обусловленная способностью этих молекул встраиваться в мембрану клеток гельминтов и тем самым нарушать их целостность. ECP и EDN обладают активностью фермента, расщепляющего рибонуклеиновую кислоту (РНКазы), что определяет их участие в противовирусной защите. Все четыре белка могут быть токсичными для собственных тканей организма. В специфических гранулах присутствуют также цитокины и ферменты ( коллагеназа, эластаза, β-глюкурнонидаза, катепсин, РНКаза , миелопероксидаза). В мелких гранулах, присутствующих только в тканевых формах эозинофилов, содержатся ферменты ( кислая фосфатаза, арилсульфатаза, пероксидаза и ряд других), а в первичных гранулах — кристаллы Шарко–Лейдена, основу которых составляет липофосфолипаза. Липидные тельца содержат все необходимое для синтеза эйкозаноидов: арахидоновую кислоту, липоксигеназу и циклоксигеназу. Секреция содержимого гранул осуществляется за счет экзоцитоза и дегрануляции. При секреции кристаллический МВР переходит в растворимую форму.
Роль эозинофилов в иммунной защите в первую очередь состоит в осуществлении внеклеточного цитолиза, которому принадлежит основная роль в защите от многоклеточных паразитов. Большинство белков эозинофилов повреждают клетки макропаразитов; некоторые (MBP, ECP и EPO) — также нормальные клетки организма; ECP и EDN обладают активностью рибонуклеазы и оказывают противовирусное действие. Основные белки эозинофилов способствуют развитию аллергических реакций (через активацию тучных клеток и базофилов с участием МВР), оказывают регулирующее действие на иммунные процессы (действуя на Т-клетки).
Эозинофилам свойственна слабая фагоцитарная активность. При активации в них образуются и затем секретируются разнообразные бактерицидные вещества — производные «кислородного взрыва»: активные формы кислорода, перекиси, производные оксида азота, цианидов и галогенов.
Эозинофилы секретируют широкий спектр цитокинов: IL-2, IL-3, IL-4, IL-5, IL-6, IL-8, IL-10, IL-12, IL-13, IL-16, IL-18, TNFα, IFNγ, TGFβ, GM-CSF, а также ряд хемокинов (эотаксин — ССL11, RANTES — ССL5, MIP-1α — ССL3), эйкозаноиды (лейкотриены, фактор агрегации тромбоцитов — PAF), нейропептиды. Хемотаксическими факторами для эозинофилов служат эотаксины (CCL11, CCL24, CCL26), RANTES, а также IL-5. Основные хемокиновые рецепторы эозинофилов — CCR1, CCR2 и CCR3, взаимодействующие с RANTES и эотаксинами. Именно эотаксины 1, 2 и 3 обусловливают основное направление спонтанной миграции эозинофилов — в пищеварительный тракт (они локализуются в lamina propria слизистых оболочек). Во время менструальных циклов и при беременности усиливается миграция эозинофилов в матку и молочные железы, где они принимают участие в морфогенезе. Ограниченные количества эозинофилов мигрируют в тимус. Привлечение эозинофилов в очаг аллергического поражения осуществляется преимущественно провоспалительным хемокином RANTES(CCL5), лейкотриенами, PAF и IL-5. Из молекул адгезии наиболее важны для миграции эозинофилов в ткани интегрины: β7- (α4β7), β1- (VLA-4 — α4β1) и все три β2-интегрина , экспрессируемые на поверхности эозинофилов.
Функция эозинофилов в норме заключается в регуляции развития тучных клеток и морфогенетических процессов, связанных с беременностью и половым циклом у самок. Малоизученным остается участие эозинофилов в положительной селекции Т-клеток в тимусе. Благодаря механизму внеклеточного цитолиза, основными факторами которого служат белки гранул эозинофилов, при биологической агрессии эти клетки играют ключевую роль в защите от некоторых гельминтов и других патогенов. Являясь источником ряда цитокинов, эозинофилы участвуют в запуске Th2-зависимых иммунных процессов, в частности аллергических.
Тучные клетки и базофилы
[править]Тучные клетки (мастоциты) и базофилы представляют тканевые клетки, содержащие в цитоплазме базофильные гранулы. Оба типа клеток имеют костномозговое происхождение и принадлежат к миелоидному ряду. Их объединяет ряд других свойств, о которых будет сказано ниже. В отличие от базофилов, относящихся к клеткам крови, тучные клетки не циркулируют в крови и представляют тканевые клетки. Мастоциты реагируют на разного рода повреждающие воздействия, участвуют в развитии воспаления, служат основными эффекторными клетками при гиперчувствительности немедленного типа и входят в первую линию иммунной защиты, обеспечивая в первую очередь защиту от многоклеточных паразитов. Базофилы также могут выполнять аналогичные функции. Однако если тучные клетки, находясь в очагах повреждения, реагируют на него немедленно, вовлечение базофилов в подобные реакции требует их миграции в ткани, что исключает участие базофилов в инициации и осуществлении ранних этапов реакций врожденного иммунитета.
Окончательная дифференциация предшественников этих клеток происходит в селезенке. Базофилы могут созревать как в костном мозгу, так и в селезенке, и мигрируют в кровоток. Дифференцировка тучных клеток проходит иначе: в кровоток поступают предшественники тучных клеток (у человека эти клетки в циркуляции имеют фенотип CD13+CD33+CD34+CD38+CD117+). Из кровотока предшественники тучных клеток мигрируют в ткани (в наибольшем количестве — в слизистую оболочку кишечника), где и завершается созревание мастоцитов. Основные факторы, определяющие дифференцировку тучных клеток — SCF и IL-3; в качестве
кофакторов выступают IL-4, IL-9, IL-10 и фактор роста нервов (NGF). В частности, эти факторы обусловливают формирование гранул и пролиферацию клеток. В слизистых оболочках в роли фактора, необходимого для развития тучных клеток, выступает IL-33. Тучные клетки сохраняют способность к делению и имеют длительный срок жизни — месяцы и даже годы.
Диаметр тучных клеток варьирует от 10 до 20 мкм. Они имеют овальную форму с ворсинчатой поверхностью. Мембранный фенотип тучных клеток выражается формулой FcεRI+CD13+CD29+CD45+CD117+СD123+. Среди мембранных молекул тучных клеток наиболее важны для реализации их функции высокоаффинные рецепторы IgE — FcεRI.
Как уже было сказано, главная морфологическая особенность этих клеток — наличие в их цитоплазме большого количества базофильных гранул (10–150 на клетку). Гранулы разновидностей тучных клеток варьируют по составу, однако они всегда содержат вазоактивные амины, главный из которых — гистамин — реализует значительную часть эффектов тучных клеток при аллергических реакциях. Кроме того, в гранулах содержатся хондроитинсульфаты А и С и/или гепарин, а у некоторых видов животных (например, у кроликов) — серотонин. В состав гранул входят также ферменты: прежде всего протеазы, а также дегидрогеназа, пероксидаза, РНКаза, гистидинкарбоксилаза и кислые гликозамингликаны. Выделяют
3 группы протеаз тучных клеток:
- триптазы (ферменты со специфичностью, близкой к трипсину; у мышей — 5 разновидностей),
- химазы (сходны по специфичности с химотрипсином; у мышей — 4 варианта) и
- карбокси-пептидазу А (относится к металлопротеиназам).
Перечисленные факторы, содержащиеся в гранулах, — предобразованные вещества. Перекрестное cвязывание рецепторов FcεRI комплексами IgE-антител с аллергенами обусловливает высвобождение содержимого гранул (дегрануляцию) и проявление всех основных реакций гиперчувствительности немедленного типа . Дегрануляция может быть вызвана также повышением содержания внутриклеточного цАМФ или концентрацией в цитозоле ионов Са2+. Дегрануляция не сопровождается гибелью клеток — гранулы после выброса регенерируют. Тучные клетки несут некоторые патогенраспознающие рецепторы (TLR-2, TLR-3, TLR-4), что позволяет им распознавать патогены и их продукты напрямую.
При стимуляции тучные клетки синтезируют и секретируют эйкозаноиды и цитокины. Из эйкозаноидов в тучных клетках в наибольшем количестве вырабатываются лейкотриен С4 и простагландин E2. Спектр цитокинов, секретируемых тучными клетками, сходен со спектром цитокинов, продуцируемых Т-хелперами 2-го типа (Th2 ): IL-3, IL-4, IL-5, IL-6, IL-10, IL-13, GM-CSF. Тучные клетки вырабатывают также провоспалительные (IL-1, IL-8, IL-12, IL-18, IL-21,
IL-23, TNFα) и гомеостатические цитокины (IL-7 и IL-15), а также TGFβ, некоторые хемокины и интерфероны основных типов. IL-4, TNF и GM-CSF мастоциты вырабатывают спонтанно, образование остальных цитокинов индуцируется стимуляторами. Активированные тучные клетки продуцируют ряд пептидных ростовых факторов (сосудистый — VEGF, фибробластный — FGF, фактор роста нервов — NGF). Спектр секертируемых цитокинов (особенно спонтанная выработка IL-4) определяет иммунорегуляторную функцию тучных клеток, главное проявление которой — участие в индукции дифференцировки Th2-клеток.
Для тучных клеток характерны поверхностные маркеры: CD117 (с-Kit) — рецептор для SCF и CD123 — рецептор для IL-3. SCF и IL-3 (помимо их роли в качестве факторов, определяющих развитие тучных клеток) служат основными факторами роста зрелых мастоцитов. Тучные клетки несут на своей поверхности также высокоаффинные FcγI-рецепторы и рецепторы для компонентов комплемента C3b и С3d (мукозные тучные клетки лишены CR1), что свидетельствует об их участии в реакциях врожденного
иммунитета. На поверхности тучных клеток присутствуют молекулы МНС обоих классов; наличие МНС-II, а также костимулирующих молекул CD86 придает мастоцитам способность выполнять функции АПК, особенно при индукции Th2-клеток.
Тучные клетки локализуются в подслизистом слое слизистых оболочек (особенно в кишечнике), соединительнотканном слое кожи (дерме),
серозных оболочках, селезенке, периваскулярной соединительной ткани.
В 1 г названных тканей содержится 104–106 тучных клеток. Мастоциты легко идентифицировать по окрашиваемости толуидиновым синим или алциановым синим. Выделяют два варианта тучных клеток:
- слизистые, или мукозные (тип t),
- серозные (тип сt).
Названия отражают 2 главных отличительных признака этих клеток — преимущественную локализацию и преобладающий тип протеаз (триптазы — t или хемотриптазы — ct). Оба типа тучных клеток происходят из костного мозга, но только клетки t-типа в своем развитии зависят от тимуса и отсутствуют у генетически бестимусных мышей. Продолжительность жизни серозных тучных клеток выше, чем слизистых. Основной ростовый фактор для клеток обоих типов — SCF; в качестве кофактора для слизистых тучных клеток выступают IL-3 и IL-4, для серозных — только IL-3. Преобладающий тип протеогликана в слизистых тучных клетках — хондроитинсульфат, в серозных — гепарин. На поверхности мукозных мастоцитов экспрессировано больше FcεRI, они содержат больше IgE в цитоплазме, чем серозные. Тучные клетки разных типов различаются также интенсивностью секреции эйкозаноидов: в слизистых тучных клетках больше лейкотриенов, в серозных — простагландина. Несмотря на существенные различия, до конца не известно, являются ли эти разновидности тучных клеток истинными субпопуляциями или представляют фенотипические варианты единой популяции тучных клеток, дифференцирующиеся под влиянием факторов микроокружения. У разных типов тучных клеток микроокружение различается: мастоциты типа t локализованы главным образом в подслизистом слое мукозы, а тучные клетки типа ct — в серозных полостях, дерме и миндалинах. Участие в защите от паразитов и развитии аллергических реакций доказано только для слизистых тучных клеток (типа t), тогда как серозные мастоциты причастны скорее к развитию склеротических процессов.
В противоположность тучным клеткам базофилы в норме представлены в кровяном русле. Их содержание в крови очень невелико — до 0,5% от числа лейкоцитов. По своей морфологии базофилы сходны как с другими типами гранулоцитов, так и с тучными клетками. Однако от других гранулоцитов базофилы отличаются наличием базофильных гранул, а от мастоцитов — сегментированным ядром, округлой формой и меньшей величиной. Для базофилов миграция в очаг аллергии — основное условие выполнения их функций. Базофилы мигрируют из кровотока в очаг аллергического воспаления наряду с эозинофилами и нейтрофилами. На них больше, чем на тучных клетках, экспрессировано рецепторов для хемотаксических факторов —
бактериального формилметионильного пептида, анафилатоксинов С3а и С5а, α- и β-хемокинов (СXCR1, СXCR4, CCR1, CCR2, CCR3). Как и тучные клетки, базофилы несут на своей поверхности высокоаффинные (FcεRI) и низкоаффинные (FcεRII, или CD23) рецепторы для IgE, Н2-рецепторы для гистамина. Однако, в отличие от мастоцитов, базофилы не экспрессируют FcRγI. Спектр TLR, экспрессируемых базофилами, значительно беднее, чем у тучных клеток. В отличие от мастоцитов, базофилы не несут на своей поверхности с-Кit. В состав базофильных гранул входят: гистамин, протеазы(химаза и триптаза) и некоторые другие ферменты, пептидогликаны (преимущественно хондроитинсульфаты), гликозаминогликаны. Количество гранул в базофилах меньше, чем в тучных клетках, и они содержат меньше протеаз. Спектр активных веществ, секретируемых базофилами, ограничен; он включает: лейкотриен C4, IL-4, IL-13 и ряд других цитокинов. Функция базофилов в тканях сходна с функцией тучных клеток — они поддерживают аллергический процесс, инициированный тучными клетками, высвобождая содержимое гранул в ответ на перекрестное связывание FcεRI. В отличие от тучных клеток, базофилы не способны восстанавливать гранулы.
Моноциты и макрофаги
[править]Моноциты и макрофаги представляют стадии развития миелоидных клеток. Они образуют мононуклеарную фагоцитирующую систему. Роль макрофагов в качестве одних из основных фагоцитирующих клеток установлена в 1882 г. И. И. Мечниковым, давшим этим клеткам их название. В 20-е гг. ХХ века Л. Ашоф (L. Aschoff) создал учение о ретикуло-эндотелиальной системе — защитной системе, объединяющей тканевые фагоцитирующие клетки. Позже для обозначения практически той же системы стали
использовать термин «мононуклеарная фагоцитирующая система» .
Циркулирующий вариант клеток — моноцит, тканевый — макрофаг. Превращение моноцита в макрофаг происходит под влиянием тканевого микроокружения и сопровождается экспрессией новых генов, то есть может рассматриваться как дифференцировка клеток. Эту дифференцировку регулирует M-CSF. Моноциты представляют довольно крупные клетки (диаметром 9-15 мкм) с ядром бобовидной формы и тонкой структурой хроматина. Макрофаги значительно крупнее моноцитов (диаметр составляет 20-25 мкм) и имеют распластанную форму. В отличие от округлых моноцитов, макрофаги имеют неправильные очертания и морфологически полиморфны.
Часто морфологических признаков оказывается недостаточно для дифференциации моноцитов от макрофагов, а также для определения их разновидностей. В этом случае используют дополнительные приемы, такие как определение ферментов или мембранных молекул-маркеров. Наиболее важные в функциональном отношении мембранные молекулы моноцитов/макрофагов — рецепторы, предназначенные для распознавания PAMP, в первую очередь — толл-подобные рецепторы (TLR). Ни на каких других клетках эти рецепторы не представлены так разнообразно, как на моноцитах и макрофагах. Это обеспечивает макрофагам и моноцитам возможность распознавать фактически все основные группы паттернов. На этих клетках обнаружены все разновидности TLR, для которых характерна экспрессия на поверхности клеток — TLR-1, TLR-2, TLR-4, TLR-5, TLR-6, TLR-11. С мембранным рецептором TLR-4 функционально связан один из основных маркеров моноцитов и макрофагов — молекула CD14. CD14 взаимодействует с комплексом бактериального ЛПС с ЛПС-связывающим белком, что облегчает взаимодействие ЛПС с TLR-4. TLR, распознающие чужеродные нуклеиновые кислоты (TLR-3, TLR-7, TLR-8, TLR-9), локализованы внутриклеточно — на мембранах цитоплазматических гранул. К группе мембранных молекул, распознающих паттерны, следует отнести молекулу CD13 (аминопептидаза N), характерную для моноцитов, но не макрофагов. Как уже было отмечено, CD13 обладает сродством к антигенам оболочки ряда вирусов.
Для моноцитов/макрофагов свойственна также экспрессия других рецепторов врожденного иммунитета — лектиновых. Лектиновые рецепторы моноцитов и макрофагов распознают свободные D-гликозильные остатки глюкозы, галактозы, маннозы, фукозы, N-ацетилглюкозамина, N-ацетилгалактозамина . На собственных клетках организма такие остатки экранированы остатками сиаловой кислоты и экспонируются преимущественно на старых клетках, подлежащих элиминации. Патогены (бактерии, грибы, простейшие) несут на поверхности гликоконъюгаты с неэкранированными гликозильными остатками, распознаваемыми лектиновыми рецепторами макрофагов, что облегчает фагоцитоз патогенов. В результате распознавания происходит эндоцитоз (пиноцитоз, фагоцитоз) образующихся комплексов. Наиболее важный рецептор лектиновой группы — маннозный рецептор (MR, CD206), характерный для макрофагов и слабее эксперссированный на моноцитах. И на моноцитах, и на макрофагах присутствуют лектиновые рецепторы DC-SIGN (CD209) и дектин-1. Экспрессия дектина-1 подавляется при активации макрофагов. Сигналом к фагоцитозу является также связывание с лигандами так называемых scavenger-рецепторов («мусорщиков»), к которым относят
молекулу MSR (Macrophage scavenger receptor, СD36), обладающую сродством к коллагену.
Другая группа рецепторов, разнообразно представленных на моноцитах/макрофагах, — Fc-рецепторы (молекулы, распознающие Fc-участок молекул иммуноглобулинов, обычно в связанном с антигеном состоянии). Эти рецепторы обеспечивают распознавание и облегчают фагоцитоз и разрушение моноцитами и макрофагами опсонизированных антителами клеток (в том числе патогенных); параллельно происходит активация фагоцитов. Моноциты экспрессируют полный набор Fcγ-рецепторов — FcγRI (CD64), FcγRII (CD32) и FcγRIII (CD16). На макрофагах присутствуют только FcγRII и FcγRIII. Моноциты — единственный тип клеток, спонтанно экспрессирующих FcγRI, обладающий наиболее высоким сродством к молекуле IgG и способный связывать его даже в свободном состоянии, а не только в составе иммунного комплекса, как это происходит обычно. На моноцитах и макрофагах представлены также рецепторы для Fc-части IgA (FcαR) и низкоаффинные рецепторы для IgE — FcεRII (CD23). Эти рецепторы участвуют в регуляции синтеза антител соответствующих изотипов.
Благодаря присутствию на поверхности моноцитов и макрофагов рецепторов для комплемента (CR) эти клетки распознают фрагменты факторов комплемента, прикрепленные к поверхности патогенов. Большинство рецепторов распознает фрагменты C3b и C3d — CR1 (CD35), CR3 (CD11b/CD18, или Мас-1) и CR4 (CD11c/CD18, или р150,95). Функция этих рецепторов сходна с таковой Fc-рецепторов: они облегчают распознавание клеток-мишеней фагоцитами и поставляют в фагоцитирующие клетки активационные сигналы. Моноциты/макрофаги экспрессируют также рецепторы для фактора C1q и хемотаксических факторов-анафилатоксинов C3a и C5a.
Поскольку для проявления функциональной активности моноцитам/макрофагам важно взаимодействие с межклеточным матриксом (в процессе миграции) и с другими клетками (при участии в реакциях иммунитета), на их поверхности представлено большое число молекул адгезии. Среди них особенно важны интегрины, например β1-интегрины, обеспечивающие связи с молекулами межклеточного матрикса (коллагеном, фибронектином, ламинином). Из β1-интегринов на моноцитах экспрессированы VLA-4, VLA-2, VLA-5 и VLA-6; 3 последних на макрофагах отсутствуют. VLA-2, VLA-5 и VLA-6 взаимодействуют с названными молекулами матрикса, а VLA-4 — еще и с мембранной молекулой лимфоцитов и самих активированных макрофагов VCAM-1. Все 3 β2-интегрина — LFA-1, Mac-1 (CR3) и p150,95 (CR4) — присутствуют на поверхности как моноцитов, так и макрофагов. β2-Интегрины взаимодействуют преимущественно с интегриновыми рецепторами ICAM-1 (CD54), ICAM-2 (CD102) и ICAM-3 (CD50), присутствующими как на Т-лимфоцитах, так и на самих макрофагах (особенно после их активации), а также на активированных эндотелиальных и эпителиальных клетках. За адгезию к эндотелиальным клеткам, необходимую при транссосудистой миграции, отвечает молекула PЕCAM (CD31). К молекулам адгезии необходимо отнести также CD15 (Lewis X) — углеводный компонент мембранных гликоконъюгатов (разветвленный трисахарид), служащий рецептором для молекул адгезии селектинов, который распознает углеводы.
Функционально важную группу поверхностных молекул моноцитов/макрфоагов образуют молекулы MHC и костимулирующие молекулы. Роль МНС состоит в представлении (презентации) антигенных пептидов TCR. Если молекулы МНС-I присутствуют на всех ядросодержащих клетках организма, то молекулы МНС-II экспрессированы только на специализированных АПК, к которым наряду с дендритными клетками и В-лимфоцитами относят макрофаги. Экспрессия молекул МНС-II усиливается при активации клеток. Презентация антигена — узловое событие иммунного ответа, связывающее реакции врожденного и адаптивного иммунитета. В ходе презентации молекула МНС распознается как самим TCR, так и корецепторами — СD8 и СD4, обладающими сродством к молекулам МНС-I и MHC-II соответственно. Молекула CD4 в небольшом количестве экспрессирована на некоторых макрофагах, что делает их чувствительными к инфицированию вирусом иммунодефицита человека (ВИЧ), для которого молекула CD4 служит основным рецептором. Помимо презентации антигена, для эффективной активации Т-клеток необходима их костимуляция. Она достигается при взаимодействии пар молекул АПК и Т-лимфоцита, называемых костимулирующими. Со стороны АПК (в том числе макрофага) в роли костимулирующих выступают молекулы CD80 и CD86. Первая из них появляется на поверхности клетки только после активации, вторая экспрессируется конститутивно (даже на покоящихся клетках), но при получении активационного сигнала ее экспрессия усиливается.
Важная группа мембранных молекул моноцитов/макрофагов — рецепторы для цитокинов. Из них наиболее специфичен для моноцитов и макрофагов Fms (CD115) — рецептор для их линейного фактора M-CSF. Наличие Fms позволяет дифференцировать моноциты и их предшественники от клеток гранулоцитарного ряда, на которых этот рецептор отсутствует. Для проявления макрофагами их функций, как эффекторных клеток иммунитета, особенно важны рецепторы для интерферона γ (IFNγRI и IFNγRII — CD119); для провоспалительных цитокинов (которые они сами же и секретируют) IL-1 (CD121a, CD121b) и TNF (CD120a, CD120b); а также рецепторы для IL-6, IL-12, IL-18, колониестимулирующего фактора GM-CSF (CD116) и ряда других цитокинов. Высокая подвижность моноцитов и особенно макрофагов требует экспрессии рецепторов для хемотаксических факторов. Некоторые из них (рецепторы для С3а и С5а) уже упоминались. Моноциты и макрофаги располагают широким спектром рецепторов для специализированных хемотаксических цитокинов — хемокинов, особенно провоспалительных: CXCR1, ССR1, CCR2, CCR3, CCR4, CCR5,
CCR8, CX3CR1.
При гистохимической идентификации моноцитов/макрофагов определяют наличие в клетках неспецифической эстеразы, диффузно распределяющейся в цитоплазме. Выявление ряда ферментов позволяет оценить степень зрелости этих клеток. Так, например, миелоперокидаза содержится в значительном количестве в моноцитах; их превращение в макрофаги сопровождается утратой этого фермента. Экспрессия 5’-нуклеотидазы, β-галактозидазы и аминопептидазы при этом, наоборот, возрастает, а трансглутаминазу удается выявить только в зрелых макрофагах. Помимо названных, в макрофагах присутствуют и другие ферменты — коллагеназа, протеиназы, липазы, нуклеазы, фосфатазы и др. Некоторые ферменты макрофагов участвуют в реализации бактерицидной активности: кислород-зависимой (NADPH-оксидаза, миелопероксидаза, каталаза), не зависящей от кислорода (лизоцим, катепсины, эластаза, аргиназа, протеазы и другие гидролазы), и в генерации оксида азота (индуцибельная NO-синтаза).
В связи со значительными различиями свойств моноцитов/макрофагов и нейтрофилов физиологическая роль этих клеток практически не перекрывается, даже несмотря на то, что основная функция тех и других — фагоцитоз. Если нейтрофилы ответственны за самый ранний этап защиты, осуществляемой с помощью фагоцитоза (проходит интенсивно, но кратковременно), то моноциты/макрофаги, помимо фагоцитоза (реализуется менее интенсивно и более продолжительно), выполняют многочисленные
другие функции, в том числе опосредованные секретируемыми ими гуморальными продуктами.
Среди секреторных продуктов макрофагов наиболее важную роль в развитии воспаления и реакций врожденного иммунитета играют цитокины. Их секреция, как правило, происходит при активации клеток. Спектр цитокинов, секретируемых моноцитами и макрофагами, очень широк: цитокины семейства IL-1 (IL-1β, IL-18, в меньшей степени IL-1α, представленный на мембране макрофагов и рецепторный антагонист IL-1) и другие провоспалительные цитокины — TNFα, IL-6, IL-12, IL-23, IL-27. Макрофаги продуцируют все 3 разновидности колониестимулирующих факторов (GM-CSF, G-CSF и M-CSF), интерфероны (особенно IFNα, но также IFNβ и IFNγ), гомеостатический цитокин IL-15, супрессорные цитокины (IL-10 и трансформирующий фактор роста β — TGFβ), ростовые/ангиогенные факторы (фибробластный — FGF, тромбоцитарный — PDGF и сосудистый эндотелиальный — VEGF). Моноциты/макрофаги образуют большую часть провоспалительных хемокинов: CXCL8 (IL-8), CCL5 (RANTES), макрофагальные воспалительные белки (ССL3, ССL4, ССL9, ССL10, ССL15, ССL18, ССL23), макрофагальные хемотаксические белки (ССL2, ССL7, ССL8, ССL12, ССL13) и др.
Миграция моноцитов в ткани сопровождается их превращением в разнообразные формы макрофагов и дендритных клеток.
Дифференцировка моноцитов в дендритные клетки будет рассмотрена в следующей главе. Выделяют две основные разновидности макрофагов — резидентные и воспалительные. Резидентные макрофаги возникают в результате спонтанной («плановой») миграции моноцитов из кровотока в ткани, не связанной с воспалением, тогда как воспалительные макрофаги образуются в процессе экстренной миграции в очаги воспаления. Превращение в макрофаги сопровождается увеличением размера и формы клеток (обусловлены перестройкой цитоскелета), изменением экспрессии некоторых мембранных молекул (ослабевает экспрессия CD13, CD14, CD15, β1-интегринов, FcγRI, усиливается экспрессия CD16). Это сказывается на ответе клеток на внешние стимулы. Воспалительные макрофаги обладают высокой фагоцитарной и бактерицидной активностью, выделяют ряд цитокинов и других гуморальных веществ, важных для формирования воспаления и реализации иммунной защиты. Эти свойства позволяют воспалительным макрофагам играть роль эффекторных клеток воспаления и врожденного иммунитета. Резидентные макрофаги выполняют преимущественно гомеостатические и регуляторные функции, участвуя в разрушении старых клеток и регуляции иммунных и воспалительных процессов, а также выступают в роли АПК. Резидентные макрофаги обладают более длительным сроком
жизни (годы по сравнению с неделями для воспалительных макрофагов).
Воспалительные и резидентные моноциты мигрируют из кровотока в ткани по-разному, поскольку в первом случае решающая роль принадлежит гуморальным факторам и молекулам адгезии, индуцируемым в процессе воспаления, а во втором — невоспалительным гомеостатическим факторам. В качестве хемокина для резидентных макрофагов выступает фракталкин(С X3CL1). Рецепторы для этого хемокина (CX3CR1) экспрессированы в большом количестве преимущественно на CD14+CD16+ моноцитах, при миграции в ткани становящихся резидентными макрофагами. СD14hiCD16- моноциты слабо экспрессируют этот рецептор, но несут рецептор CCR2 для провоспалительных хемокинов преимущественно группы МСР (CCL2, CCL7, CCL8, CCL13, CCL16). В связи с этим СD14hiCD16- клетки обладают способностью
мигрировать в очаги воспаления и превращаться в воспалительные макрофаги. Наличие рецептора CCR2 — очень важное свойство СD14hiCD16- клеток, поэтому эту субпопуляцию моноцитов иногда обозначают как CD14hiCCR2+. Эти клетки экспрессируют еще несколько хемокиновых рецепторов, отсутствующих у предшественников резидентных макрофагов: CCR1, CCR4, ССR7, CXCR1, CXCR2. Эти рецепторы распознают практически все провоспалительные и часть гомеостатических цитокинов. В свою очередь, предшественники резидентных макрофагов, помимо рецептора для фракталкина, несут еще несколько хемокиновых рецепторов, отсутствующих или слабо экспрессированных на воспалительных моноцитах — ССR5 и CXCR4 (отметим, что эти рецепторы служат корецепторами для ВИЧ и, следовательно, способствуют инфицированию этим вирусом макрофагов).
Резидентные макрофаги, локализованные в разных органах, могут существенно различаться по морфологии, составу экспрессируемых поверхностных маркеров, спектру секретируемых цитокинов и функциям. Большинство из них имеют собственные названия. Так, макрофаги печени, называемые клетками Купфера, имеют звездчатую форму; они занимают пространство между
сосудами печени и гепатоцитами и участвуют в фильтрации продуктов, поступающих из кровотока в паренхиму печени. Численность этих клеток очень велика: на их долю приходится до 50% клеток мононуклеарной фагоцитирующей системы. Определенным своеобразием отличаются альвеолярные макрофаги (способны мигрировать в просвет альвеол), перитонеальные макрофаги, макрофаги центральной нервной системы (микроглия), почек (мезангиальные клетки), костей (остеокласты), тимуса (их важнейшая функция состоит в удалении тимоцитов, в массовом порядке погибающих в процессе развития и селекции), макрофаги вторичных лимфоидных органов и т.д. Вариабельность макрофагов проявляется также и на уровне активированных клеток. Однако в этом случае разнообразие обусловлено не только собственными свойствами моноцитов/макрофагов, но и природой стимуляторов.
Дендритные клетки
[править]Для зрелых дендритных клеток характерны 3 фундаментальных свойства, объединяющие все их разновидности:
- отростчатая, древовидная морфология в тканях и наличие псевдоподий и ворсинок (вуалевые клетки) в циркуляции и культуре клеток;
- высокая экспрессия зрелыми клетками молекул МНС не только I, но и II класса в сочетании с костимулирующими молекулами (CD80, CD86);
- способность захватывать (путем пиноцитоза и, в меньшей степени, фагоцитоза) и обрабатывать антиген с последующим его п
редставлением Т-лимфоцитам, что вызывает активацию последних.
Дендритная морфология не является исключительной особенностью дендритных клеток. Так, в коже мышей присутствуют дендритные Т-лимфоциты, гистогенетически не родственные дендритным клеткам. Только сочетание перечисленных свойств может служить основанием для отнесения клетки к разряду дендритных.
Дендритные клетки происходят от кроветворных стволовых клеток, т.е. имеют костномозговое происхождение. Главные особенности развития дендритных клеток:
- дендритные клетки происходят как из миелоидных, так и из лимфоидных предшественников;
- способность к дифференцировке в дендритные клетки присуща представителям этих ростков на разных стадиях их развития. Наряду с этим допускается существование специализированного предшественника дендритных клеток;
- в периферической крови присутствуют дендритные клетки на промежуточных стадиях развития, после чего они мигрируют в ткани;
- по крайней мере для некоторых дендритных клеток характерно перемещение из барьерных тканей в лимфоидные, сопровождающееся их созреванием.
Большинство дендритных клеток принадлежит миелоидному ряду. В условиях культуры удается получить миелоидные дендритные клетки двумя способами: путем культивирования клеток костного мозга, обогащенных CD34+ стволовыми элементами, в присутствии GM-CSF и других цитокинов (чаще всего — TNFα, иногда — IL-3, SCF, FLT3L или TGFβ) или при культивировании выделенных из крови моноцитов в присутствии GM-CSF и IL-4. Культивирование моноцитов in vitro в присутствии M-CSF
приводит к дифференцировке CD14+ макрофагов, а культивирование в присутствии GM-CSF (для клеток человека — в сочетании с IL-4) — к дифференцировке CD14- дендритных клеток. Считают, что и in vivo миелоидные дендритные клетки могут развиваться как из гранулоцитарно-моноцитарных предшественников, так и из моноцитов.
Сходным образом происходит развитие лимфоидных дендритных клеток — они дифференцируются из CLP, а также из предшественников В- и Т-лимфоцитов, в частности из тимоцитов на самой ранней стадии их развития в тимусе — DN1 клеток. Миелоидные и лимфоидные предшественники дендритных клеток экспрессируют цитокиновый рецептор FLT-3 (Fms-like tyrosine kinase 3), что отличает их от предшественнков других клеток (в частности моноцитов и лимфоцитов). Таким образом обычная дендритная клетка может дифференцироваться из 6–7 клеточных источников в пределах двух гистогенетических рядов.
Незрелые дендритные клетки обоих рядов циркулируют в крови, составляя в сумме менее 0,5% от общего числа лейкоцитов крови. В кровотоке присутствуют предшественники как миелоидных, так и лимфоидных дендритных клеток, а также клеток Лангерганса. Маркерами миелоидных предшествнеников служат молекулы CD11c и MHC-II.
Преобладающая разновидность циркулирующих в крови незрелых дендритных клеток — плазмоцитоидные дендритные клетки, относящиеся к лимфоидному ряду. Их название обусловлено внешним сходством с плазматическими клетками — потомками В-лимфоцитов, секретирующими антитела. Плазмоцитоидные дендритные клетки меньше моноцитов (8–10 мкм), а их ядро имеет менее выраженную выемку. В присутствии IL-3 и бактериальных продуктов они дифференцируются в зрелые лимфоидные дендритные клетки. На плазмоцитоидных клетках человека отсутствуют молекулы, характерные для миелоидных дендритных клеток (CD83, CD11b, CD11c), а также свойственные большинству миелоидных клеток — CD13 и CD14. Однако в них экспрессирован ген RAG, ответственный за запуск перестройки генов антигенраспознающих рецепторов и выражены признаки перестройки генов TCR, характерные для Т-клеток (пре-Tα). Если для моноцитов характерна экспрессия CD45RA и рецептора для GM-CSF, то для
плазмоцитоидных клеток — CD45R0 и рецептора для IL-3. Молекулы МНС-II на плазмоцитоидных клетках экспрессированы слабее, чем на миелоидных, и локализуются не только на поверхности, но и в цитоплазме. В спектре TLR , экспрессируемых плазмоцитоидными дендритными клетками, преобладают рецепторы, локализующиеся в цитоплазматических гранулах и распознающие нуклеиновые кислоты. Плазмоцитоидные дендритные клетки — главные источники интерферонов типа I (α, β, ω ) синтез которых запускается в ответ на распознавание TLR специфического паттерна. Это определило их альтернативное название —
клетки-продуценты интерферона (IPC — от Interferone-producing cells). Они секретируют большие количества этих цитокинов преимущественно в 1-е сутки после стимуляции вирусными нуклеиновыми кислотами.
Не достигнув полной зрелости, миелоидные и лимфоидные дендритные клетки мигрируют в ткани. Этому способствует наличие на поверхности этих клеток хемокиновых рецепторов практически ко всем β-хемокинам. Дендритные клетки широко представлены в различных органах и тканях, однако они присутствуют в них в малом количестве, что и послужило причиной их позднего открытия. По аналогии с макрофагами тканевые дендритные клетки иногда разделяют на резидентные (стационарные) и
воспалительные. Резидентные дендритные клетки присутствуют преимущественно в барьерных тканях — коже и слизистых оболочках. Известно несколько разновидностей этих клеток, формирующихся под влиянием микроокружения — дендритные клетки дермы, эпидермиса, слизистой оболочки кишечника, слизистой оболочки легких.
Эпидермальные дендритные клетки обладают наибольшим своеобразием. Большинство из них представлено клетками Лангерганса, относящимися к миелоидному ряду. Эти клетки были описаны гистологами в конце XIX века как отростчатые клетки эпидермиса (по современной гистологической классификации — белые отростчатые эпидермоциты), но их природа и связь с иммунными процессами была установлена только в результате их изучения как дендритных клеток. Клетки Лангерганса имеют ряд существенных особенностей, отличающих их от других дендритных клеток. Прежде всего это присутствие в цитоплазме слоистых включений — гранул Бирбека . На поверхности клеток Лангерганса присутствует лектиновый рецептор лангерин (CD208) и «неклассическая» молекула МНС — CD1a, предназначенная для презентации липидных антигенов. Лангерин присутствует уже на циркулирующих предшественниках этих клеток. Гистогенез клеток Лангерганса до конца не выяснен. В настоящее время считают, что они развиваются местно из предшественников дендритных клеток, мигрирующих из костного мозга.
В условиях воспаления дендритные клетки барьерных тканей интенсивно поглощают (путем пино- или фагоцитоза) окружающий материал, в том числе чужеродные продукты; активируются патогенами (точнее «образами патогенности» — PAMP, представленными на поверхности патогенов) и подвергаются действию провоспалительных цитокинов. Под влиянием этих стимулов незрелые дендритные клетки покидают ткани и с тканевой жидкостью через лимфатические сосуды поступают в региональные лимфатические узлы. В процессе миграции происходит созревание дендритных клеток: их способность к эндоцитозу значительно ослабевает; они осущест-вляют переработку поглощенного материала и встраивают пептидные фрагменты белков в молекулы MHC; на поверхности клеток усиливается экспрессия молекул МНС-II и костимулирующих молекул CD80 и CD86. Усиленная экспрессия MHC-II, CD80 и CD86 способствует выполнению дендритными клетками их основного назначения — презентации антигенных пептидов Т-лимфоцитам. В ходе миграции изменяется набор экспрессируемых дендритными клетками мембранных рецепторов для хемокинов, что способствует попаданию их в зоны лимфатических узлов, занимаемые Т-лимфоцитами (Т-зоны). Вместо рецепторов для хемокинов, экспрессируемых клетками барьерных тканей, на созревающих дендритных клетках появляются рецепторы CCR7 и CXCR4. Именно эти
рецепторы распознают хемокины, выделяемые стромальными клетками Т-зон лимфатических узлов. Рецепторы CCR7 и CXCR4 экспрессируют также наивные Т-лимфоциты, в результате чего они тоже мигрируют в Т-зоны лимфатических узлов. В Т-зонах происходит презентация антигена. Зрелые дендритные клетки, доставившие антиген в лимфатический узел, становятся частью стромы Т-зон и обозначаются как интердигитальные дендритные клетки, поскольку между их отростками-«пальцами» располагаются Т-лимфоциты. Сходное происхождение имеют интердигитальные клетки Т-зон пейеровых бляшек и селезенки, хотя пути миграции клеток в эти структуры иные (не лимфогенные).
Резидентные миелоидные дендритные клетки также заселяют органы на стадии незрелых и даже клеток-предшественников. Завершая свое развитие местно, они уже не покидают орган. Тканевое микроокружение достаточно сильно влияет на их свойства (сходно с резидентными макрофагами и тучными клетками). Многие из них сосредоточены в лимфоидных органах. Различают дендритные клетки тимуса, зародышевых центров, маргинальной зоны селезенки, печени и т.д.
Судьба плазмоцитоидных дендритных клеток в процессе и после их миграции в лимфоидные органы также изучена достаточно подробно. В отличие от предшественников миелоидных дендритных клеток, попадающих в лимфатические узлы с афферентной лимфой, плазмоцитоидные дендритные клетки проникают в лимфатические узлы тем же путем, что и Т-лимфоциты — через высокий эндотелий посткапиллярных венул. При стимуляции (вирусами или IL-3) плазмоцитоидные дендритные клетки в течение первых суток интенсивно секретируют интерфероны I типа, а затем в течение вторых суток дифференцируются в зрелые лимфоидные дендритные клетки. При этом на них значительно возрастает экспрессия молекул МНС-II, появляются костимулирующие молекулы CD80 и CD86. Клетка продолжает секретировать интерфероны, но в меньшем количестве. При стимуляции вирусами созревающая дендритная клетка способствует дифференцировке Т-клеток-продуцентов IFNγ (Th1-клеток), а при стимуляции IL-3 — Т-клеток — продуцентов IL-4 (Th2-клеток).
В настоящее время в качестве конечных продуктов дифференцировки
миелоидных и лимфоидных дендритных клеток (особенно у человека) рассматривают соответственно субпопуляции DC1 и DC2 . Наиболее характерные отличительные черты этих клеток — особенности экспрессии молекул CD11c и рецептора для IL-3 — CD123: миелоидные клетки DC1 имеют фенотип CD11chi CD123lo (выявлена минорная разновидность миелоидных дендритных клеток с фенотипом CD11clоCD123-), а лимфоидные DC2 — CD11c- CD123hi
. В периферической крови содержится по 0,2% клеток DC1 и DC2. Дифференцировка DC1 и DC2 может регулироваться действием на
клетки-предшественники различных комбинаций провоспалительных и противовоспалительных факторов . DC1-клетки обладают сильной способностью активировать Т-лимфоциты при презентации антигена, а также индуцируют дифференцировку Тh1-клеток , В то же время DC2-клетки при презентации антигена направляют дифференцировку Т клеток по Th2-пути. И наконец, можно получить дендритные клетки, избирательно индуцирующие регуляторные Т-клетки, т.е. являющиеся толерогенными.
Клетки, вовлекаемые в иммунные процессы
[править]Важная особенность функционирования системы врожденного иммунитета — способность вовлекать в развитие реакций, помимо «профессиональных» клеток иммунной системы, клетки других типов, прежде всего сосудистого эндотелия, эпителия слизистых оболочек, кожи, печени и т.д. Для вовлечения в реакции эти клетки должны быть активированы под влиянием стимулов двух типов:
- патогенов и выделяемых ими продуктов;
- провоспалительных цитокинов и других продуктов активированных клеток иммунной системы, прежде всего макрофагов.
В распознавании микроорганизмов и их продуктов участвуют специализированные патогенраспознающие рецепторы (в первую очередь TLR), экспрессируемые на покоящихся клетках сосудистого эндотелия. Так, показано присутствие TLR-2, TLR-4 и других рецепторов, распознающих PAMP на эпителиальных и эндотелиальных клетках. На эндотелиальных и многих эпителиальных клетках конститутивно (спонтанно) экспрессированы рецепторы для цитокинов, например для IL-1, TNFα, IL-6, IL-8 и других.
В ответ на связывание соответствующих цитокинов эндотелиальные и эпителиальные клетки активируются и приобретают некоторые черты клеток врожденного иммунитета, особенно макрофагов: они экспрессируют молекулы адгезии (ICAM-1, ICAM-3, селектины и их рецепторы и другие молекулы); секретируют провоспалительные цитокины (IL-1, IL-6, TNFα); колониестимулирующие факторы и хемокины; приобретают способность к фагоцитозу благодаря экспрессии Fсγ-рецепторов и рецепторов для комплемента, а также некоторых факторов, обеспечивающих бактерицидность. Наконец, эти клетки экспрессируют молекулы МНС-II и костимулирующие
молекулы (CD40, CD80, CD86), что придает им свойства АПК и позволяют «вести диалог» с клетками иммунной системы. Все перечисленные свойства выражены значительно слабее, чем у макрофагов. Тем не менее, они обеспечивают участие этих клеток в защитных реакциях врожденного иммунитета и (пусть и в ограниченном масштабе) позволяют выполнять роль АПК для клеток памяти.
Таким образом, вовлечение различных типов клеток существенно расширяет сферу действия провоспалительных факторов и увеличивает защитный потенциал организма. После завершения воспалительной реакции и прекращения стимуляции со стороны клеток врожденного иммунитета эти «факультативные» иммуноциты утрачивают свои макрофагоподобные свойства и восстанавливают исходный фенотип и свойственные им функции.
Система комплемента
[править]
Система комплемента была открыта раньше других гуморальных систем врожденного иммунитета. В 1898 г. сотрудник Института Пастера в Париже Ж. Борде (J. Bordet) обнаружил термолабильную составляющую системы факторов, ответственных за иммунный гемолиз, и назвал ее термином «алексин» (термин «комплемент», от лат cоmplementare — дополнять, введен П. Эрлихом
позже). Вскоре выяснилось, что комплемент — не одиночный фактор, а целая система факторов. Значительно позже, в 70-е годы ХХ века, на основе работ Л. Пиллемера (L. Pillemer), выполненных в 50-е годы ХХ века, было сформулировано представление о пропердиновой системе, которое вскоре было трансформировано в учение об альтернативном пути активации комплемента (с тех пор классическим путем активации стали называть антителозависимый путь, открытый Ж. Борде). Наконец, в 90-е годы ХХ века было признано существование 3-го пути активации комплемента — лектинового.
Активация системы комплемента осуществляется в два основных этапа (фазы):
- запуск активации (происходит при участии факторов различной природы, не относящихся к системе комплемента), завершающийся формированием С3/С5-конвертаз;
- лизис клеток-мишеней.
Пути активации кардинально различаются особенностями первой фазы, тогда как фаза клеточного лизиса одинакова для всех трех путей.
Факторы системы комплемента
[править]
Выделяют факторы, запускающие три основных пути активации комплемента, общие факторы (С3, С5, белки литического комплекса), а также регулирующие и ингибирующие белки. Факторы классического пути активации, а также общего для всех путей этапа — атаки клеточной мембраны — обозначают заглавной буквой С с добавлением порядкового номера (например, С3), обычно соответствующего последовательности их вступления в процесс активации (исключение — С4). Фрагменты, образующиеся при расщеплении компонентов комплемента обозначают так же, как «родительский» компонент, с добавлением строчных букв «a» или «b». При этом крупный фрагмент помечают буквой «b», а мелкий — «а» (например, С3а и С3b). Для факторов альтернативного и лектинового путей приняты другие обозначения.
Белки системы комплемента в норме содержатся в сыворотке крови, главным образом во фракции β-глобулинов. Только некоторые регулирующие белки представлены исключительно на мембранах клеток. Факторы комплемента вырабатываются клетками печени — гепатоцитами (до 90% всех факторов системы комплемента), а также моноцитами/макрофагами, клетками почечного эпителия, эндотелиальными клетками. Только С7 и фактор D вырабатываются преимущественно вне печени — соответственно в нейтрофилах и жировой ткани. Хотя факторы комплемента продуцируются постоянно, при воспалении под влиянием цитокинов (IFNγ, цитокины
семейства IL-1) их секреция усиливается.
Белки системы комплемента содержат домены (модули), относящиеся к различным семействам. Упомянем три семейства доменов, наиболее широко представленных среди белков комплемента. К семейству С3/α2-макроглобулина , относят С3, С4 и С5. Для всех этих белков характерна тиоэфирная связь между СООН-группой остатка глутаминовой кислоты и SH-группой цистеина (в молекуле С5 она утрачена в ходе филогенеза). Эта связь играет ключевую роль в активации альтернативного пути и в фиксации компонентов комплемента на клеточных мембранах. В присутствии воды происходит гидролиз этой связи с восстановлением групп SH и COOH.
Карбоксил при этом может формировать связь с NH2-группами различных молекул, в том числе мембранных белков клеток. Обычно эта тиоэфирная связь экранирована, и окружающие молекулы, в том числе вода, не имеют к ней доступа. Экранирование тиоэфирной связи исчезает только при определенной конформации молекулы, которую компоненты С3 и С4 могут приобретать спонтанно или при частичном расщеплении (активации). Как уже отмечалось, с неэкранированной тиоэфирной связью реагируют молекулы воды или мембранных белков.
Второй тип доменов, распространенных в белках системы комплемента, — короткие согласительные (consensus) повторы. Они характерны для белков, регулирующих активацию комплемента (фактор H, C4bp, DAF, CR1, CR2) и поэтому их называют также доменами контроля комплемента (доменами ССР — от Сomplement control proteins). Такие домены входят в состав мозаичных (т.е. со-держащих домены различных типов) белков — фактора В, С2, С1r, С1s, С6, С7, MASP-1, MASP-2, MASP-3. Третий тип доменов, распространенных в системе комплемента — модуль сериновых протеаз , присутствующий в С2, а также факторах В, D, I, MASP-1, MASP-2, MASP-3, C1r, C1s.
Основная молекула системы комплемента — С3. Она представляет собой α-глобулин, состоящий из двух полипептидных цепей, скрепленных дисульфидной связью: α (120 к Да) и β (75 кДа). Тиоэфирная связь располагается в α-цепи; ее экранирование обеспечивается конформацией α-цепи, закрепленной дисульфидной связью.
Пусковые молекулы классического и лектинового путей — соответственно С1q и МВL — принадлежат к семейству коллектинов. Они имеют большие размеры и комплексное строение. С1q и МВL образованы тремя типами цепей (А, В и С), скрученных в жгуты. Молекула С1q содержит 6, а молекула MBL — от 2 до 6 таких жгутов (т.е. всего С1q содержит 18, а MBL — от 6 до 18 полипептидных цепей), что и обусловливает их большую молекулярную массу. В собранном виде молекула C1q и тяжелый вариант молекулы MBL имеют вид «букета тюльпанов»: N-концевые домены молекул, имеющие коллагеноподобную структуру, спирально переплетаясь, формируют ствол «букета», тогда как глобулярные С-концевые части цепей образуют расходящиеся «ветви букета» (в каждой из этих ветвей присутствуют все три типа цепей — А, В и С). Бутонообразные завершения этих «ветвей» участвуют во взаимодействии с естественными лигандами — комплементсвязывающими участками молекул иммуноглобулинов-антител (в случае C1q) и лектинами (в случае MBL). Несмотря на значительное сходство четвертичной структуры C1q и MBL, они обладают низкой гомологией.
Структурное сходство характерно для некоторых белков, относящихся к разным путям активации, но выполняющим сходные функции: факторов В и С2, а также С1r, С1s, MASP-1, MASP-2 и MASP-3. Еще одну группу сходных белков образуют белки литического комплекса — С6, С7, С8 и С9; к ней относят также порообразующий белок цитотоксических лимфоцитов — перфорин . Это амфифильные белки, обладающие как гидрофильными, так и липофильными свойствами, что обеспечивает им возможность встраиваться в клеточные мембраны. Эти молекулы состоят их различных доменов — тромбоспондинового, рецептора липопротеинов низкой плотности, эпидермального фактора роста.
Активация комплемента по альтернативному пути
[править]Механизмы запуска
Альтернативный путь активации филогенетически наиболее древний. Он полностью реализуется в рамках врожденного иммунитета. Запуск альтернативного пути активации связан с гидролизом вышеупомянутой тиоэфирной связи в молекуле С3, происходящим постоянно, но в очень немногих молекулах С3 (0,5% от числа молекул сывороточного С3). Эти молекулы спонтанно (стохастически) приобретают развернутую конформацию, при которой тиоэфирная связь становится доступной для Н2О. После гидролиза тиоэфирной связи развернутая (денатурированная) конформация молекулы С3 стабилизируется. Образующийся при этом в малом количестве продукт С3(Н2О) участвует в гидролизе фактора В , делая его доступным для расщепления сывороточной трипсиноподобной сериновой протеазой — фактором D. В результате образуется два продукта расщепления фактора В — Ва (33 кДа) и Вb (60 кДа). Фрагмент Bb формирует комплекс с С3(Н2О) — С3(Н2О)Bb, обладающий активностью С3-конвертазы, т.е. способный расщеплять, а следовательно и активировать, фактор С3. Энзиматическая активность комплекса С3(Н2О)Bb обусловлена фрагментом Bb.
Комплекс С3(Н2О)Bb образуется в следовых количествах, но он запускает фазу амплификации (умножения). С3(Н2О)Bb расщепляет α-цепи С3 компонента комплемента (напомним, что С3 состоит из двух полипептидных цепей — α и β). В результате действия на С3 «затравочных» количеств С3(Н2О)Bb происходит расщепление дополнительных количеств С3. Малый фрагмент С3а (10 кДа) отщепляется от N-концевой части α-цепи. Большой фрагмент C3b (185 кДа) включает оставшуюся часть α-цепи и
β-цепь. Дисульфидные связи в молекуле сохраняются без изменений. Фрагмент С3b обладает сродством к фактору В. При этом, как и при взаимодействии с C3(H2O), фактор В расщепляется фактором D на фрагменты Ва и Вb. Это расщепление происходит уже в значительно большем масштабе. Фрагмент Вb связывается с С3b в присутствии ионов Mg2+ с образованием комплекса C3bBb, также обладающего активностью С3-конвертазы. C3bBb называют амплифицирующей конвертазой, поскольку он значительно эффективнее осуществляет конверсию С3, чем С3(Н2О)Вb. В формировании комплекса C3bBb может участвовать также фрагмент
С3b, образующийся при активации комплемента по классическому пути (см. далее); в то же время С3b-фрагмент, образующийся по альтернативному пути, может входить в состав C3-конвертазы классического пути. Это означает возможность взаимодействия и взаимного усиления двух путей активации комплемента.
Стабилизация С3-конвертазы альтернативного пути
В растворе комплекс C3bBb быстро инактивируется, диссоциируя под действием фактора Н (он вытесняет Bb из комплекса). Затем α-цепь С3b в составе комплекса С3bH расщепляется фактором I. Стабилизация комплекса С3bBb происходит только при его иммобилизации на клеточной мембране, с участием упоминавшейся выше тиоэфирной связи α-цепи С3b. Фактор Н может атаковать и прикрепленный к мембране C3bBb, однако инактивация этого комплекса происходит только при наличии на поверхности клетки остатков сиаловых кислот. Поскольку эти остатки представлены на клетках макроорганизма, но не на поверхности микроорганизмов, комплекс С3bBb относительно стабилен только на поверхности микроорганизмов. На собственных клетках макроорганизма-хозяина комплекс разрушается под действием факторов Н и I. В качестве кофакторов при этом выступают
мембранные молекулы — рецептор комплемента CR1 (СD35) и DAF (Decay-activating factor; CD55). Некоторые бактериальные продукты [ЛПС (активна его сахаридная часть) и полисахаридные токсины], напротив, стабилизируют комплекс С3bBb. Аналогичной активностью обладают зимозан, полиэлектролиты и агрегированные иммуноглобулины (последние блокируют
действие фактора Н). Таким образом, постоянно происходящая в организме активация комплемента по альтернативному пути не повреждает собственные клетки организма, но обеспечивает защиту от патогенов.
Исходным событием при обнаружении и дальнейшем изучении альтернативного пути активации комплемента стало открытие Л. Пиллемером пропердина. Пропердин, или белок Р, обеспечивает стабилизацию комплекса C3bBb за счет ослабления его спонтанной диссоциации. Под влиянием белка P время полужизни комплекса увеличивается с 60 мкс до 90 с. Помимо этого, пропердин ускоряет сборку комплекса C3bBb и предотвращает действие на него фактора Н. Пропердин способен связываться с поверхностью бактериальной клетки и усиливать фиксацию на ней С3-конвертазы (С3bBb). При этом к комплексу могут присоединяться дополнительные молекулы С3b, что приводит к появлению на поверхности клетки избытка молекул С3b, важного для проявления опсонизирующего эффекта комплемента. Комплекс Р(С3b)nBb функционирует как С5-конвертаза (хотя сохраняет активность и в отношении компонента С3); при этом ферментативная активность этого комплекса, как и в С3-конвертазе, связана с Bb.
Первый этап активации комплемента по альтернативному пути на этом завершается. Рассмотрение его механизмов позволяет заключить, что сама по себе активация С3 и фактора В происходит спонтанно и непрерывно. Направленное действие комплемента как части иммунной системы реализуется при стабилизации комплекса C3bBb на мембране бактериальных клеток, но не собственных клеток организма. Результат первой фазы активации комплемента по альтернативному пути — образование С5-конвертазы и опсонизация клеток молекулами С3b.
Активация комплемента по классическому пути
[править]Следующим этапом эволюции системы комплемента было становление лектинового пути активации. Однако в силу устойчивой традиции и связанной с ней терминологии удобнее вначале рассмотреть классический путь активации комплемента. Его кардинальное отличие от двух других путей состоит в зависимости от факторов адаптивного иммунитета, а именно — от антител и их комплексов с антигеном.
Активация С1q и образование комплекса C1qrs
Первый компонент комплемента при активации по классическому пути — С1q. Активация C1q происходит при его взаимодействии со
связавшим антиген антителом. При связывании антигена конформация молекулы иммуноглобулина изменяется, в результате чего в ее константных доменах (Сγ2 и Сγ3, а также Сμ3 и Сμ4 ) «открывается» участок, имеющий сродство к молекуле С1q. Подобный участок присутствует только в молекулах IgM, IgG1, IgG3 и (в меньшей степени) IgG2. С1q, являясь 6-валентной молекулой, взаимодействует через С-концевые участки глобулярной части «ветвей букета» (см. выше) одновременно не менее чем с двумя Сμ-доменами одной и той же молекулы IgM или с Сγ2-доменами разных молекул IgG. Этот процесс зависит от присутствия ионов Са2+. С1q может связываться также с другими молекулами, как эндогенными ( С-реактивный белок, холестеринсодержащие липиды), так и экзогенными (липид А бактериального ЛПС, некоторые вирусные белки). Однако основные активаторы С1q — иммуноглобулины в составе иммунных комплексов.
При связывании С1q с перечисленными молекулами происходит его активация, благодаря чему С1q приобретает активность сериновой протеазы (эстеразы). Субстрат для С1q-протеазы — молекулы С1r и C1s, расщепляемые на контактный и каталитический фрагменты (удерживаются в составе комплекса за счет внутримолекулярных связей). При расщеплении происходит активация каталитического фрагмента. Сначала C1q расщепляет С1r. Затем активный С1r участвует в расщеплении C1s. В результате попарного взаимодействия контактных и каталитических фрагментов C1r и C1s образуется комплекс С1qrs, обладающий активностью трипсиноподобной протеазы/эстеразы. Сближение активных участков C1r и С1s способствует их активации. Формированием комплекса C1qrs завершается фаза узнавания. Компонент C1r расщепляет C1s, активированный C1s — факторы С4 и С2. Комплекс С1qrs может существовать в растворимой и связанной с мембраной формах. Мембранная форма образуется, если иммунный комплекс
локализован на поверхности клетки (на ней же происходит фиксация компонентов комплемента).
Формирование С3-конвертазы
Следующая стадия активации состоит в образовании С3-конвертазы. С1qrs-эстераза расщепляет С4 и С2 на тяжелые (C4b и C2b) и легкие (С4а и С2а) фрагменты. C4b взаимодействует с комплексом C1qrs и затем, при участии ионов Mg2+, связывает С2b. Комплекс C4b2b обладает активностью С3-конвертазы. Ферментативная специфичность комплекса связана с С2b (подобно тому, как специфичность С3-конвертазы альтернативного пути связана с Bb).
В данном случае, как и при активации факторов В, С3 и С5 соблюдается общее правило активации системы комплемента: активация каждого очередного фактора системы комплемента происходит при его расщеплении на крупный и мелкий фрагменты. При этом крупные фрагменты («b») обладают ферментативной (протеазной/эстеразной) активностью и непосредственно участвует в активации других компонентов комплемента. Мелкие фрагменты («а») лишены ферментативной активности и не участвуют в последующих реакциях каскада. Однако им свойственны сосудорасширяющая, хемотаксическая и другие формы биологической активности, что делает их важными факторами воспаления и реакции гиперчувствительности. Так, упоминавшийся выше пептид С4а обладает хемотаксической и кининовой (сосудорасширяющей) активностью.
При формировании мембранного комплекса С1qrs4b2b он связывается с поверхностью клетки не только через комплекс «мембранный антиген–антитело», но и ковалентно (что обеспечивается благодаря разрыву тиоэфирной связи, присутствующей в составе молекулы C4b и взаимодействия СООН-группы остатка глутаминовой кислоты с NH2-группами мембранных белков). С этого момента комплекс обозначают как C4bC2b. Если комплекс остается в растворе, он быстро инактивируется. Даже связанный с мембраной комплекс подвергается атакам инактивирующих факторов — С4bp (С4b-связывающий белок), мембранных рецепторов CR1 (СD35) и DAF (CD55); все они способны вытеснять С2 из комплекса. Время полужизни комплекса C4bC2b — около 2 мин.
Расщепление С3
Конвертаза C4bС2b (как и описанная выше конвертаза C3bBb) действует на α-цепь молекулы С3. Активный центр конвертазы локализован в молекуле C2b. Как и при альтернативном пути активации, С3 расщепляется на большой фрагмент C3b, участвующий в дальнейших реакциях каскада комплемента, и малый фрагмент С3а, обладающий хемотаксической и сильной анафилактогенной активностью. Рецепторы для С3а представлены на поверхности лимфоцитов, нейтрофилов, тучных и эндотелиальных клеток,
что обусловливает его действие на эти клетки, проявляющееся, например, в повышении проницаемости сосудов и индукции дегрануляции.
С3b связывается с иммобилизованным на мембране комплексом С1qrs4b2b. При этом происходит фиксация на клетке значительно большего числа молекул С3b, чем необходимо для насыщения комплекса — часть молекул С3b формирует ковалентную связь непосредственно с молекулами клеточной мембраны (по тому же механизму, как С4b). Иммобилизованный комплекс C1qrs4b2b3b способен расщеплять компонент комплемента С5, т.е. обладает активностью С5-конвертазы. И в этом случае специфичность
фермента связана с С2b. Таким образом, С3- и С5-конвертаза — фактически один и тот же фермент (иногда их обозначают как С3/С5-конверта-за). Однако на разных этапах формирования С2b-содержащего комплекса создаются оптимальные условия для связывания и расщепления разных субстратов — сначала С3, а затем С5.
Оставаясь в жидкой фазе, фрагмент С3b быстро расщепляется в двух точках фактором I в присутствии фактора Н. В результате образуется фрагмент iC3b. Фактор I действует и на иммобилизованный C3b, но значительно слабее. Фрагмент iC3b далее расщепляется на С3c (содержит фрагменты α-цепи и связанную с ними через дисульфидные связи интактную β-цепь) и C3dg. Последний дополнительно расщепляется на фрагменты C3d и С3g. При деградации мембранного С3b фрагмент C3dg, а затем C3d
остается связанным с мембраной, поскольку именно в них локализуются остатки, формирующие тиоэфирную связь. Перечисленные фрагменты лишены ферментативной активности, но фрагменты iC3b и C3d являются лигандами для рецепторов макрофагов и некоторых других фагоцитирующих клеток. Присутствие на фагоцитах рецепторов для этих фрагментов определяет значение опсонизации.
Активация комплемента по лектиновому пути
[править]
В сыворотке крови присутствует сложный белок, относящийся к семейству коллектинов, — маннозасвязывающий лектин (MBL — от Mannosa-binding lectin). MBL принадлежит к С-лектинам, т.е. связывается с полисахаридами в присутствии ионов Ca2+. Он специфичен к остаткам маннозы (как следует из его названия) и N-ацетилглюкозамина. В зависимости от числа «жгутов»,
образованных полипептидными цепями 3 типов (см. выше), различают 2 разновидности MBL — MBL-I и MBL-II, содержащие соответственно 2 и 6 «жгутов». При связывании MBL с гликоконъюгатами клеточной мембраны он приобретает сродство к белкам MASP-1, MASP-2, MASP-3 (от англ. MBL-associated serine proteases) и MАР19 (MBL-associated protein 19). В результате образуется несколько типов комплексов — MBL-I–MASP-3 и MBL-II–MASP-1–MASP-2, а также комплексы, наряду с MASP содержащие и MАР19. Комплекс MBL-II–MASP-1–MASP-2 аналогичен по структуре комплексу C1qrs. При взаимодействии с MBL молекулы проферментов MASP активируются и приобретают способность расщеплять компоненты комплемента С4 и С2, проявляя полную функциональную аналогию с комплексом C1qrs. Дальнейшие реакции лектинового и классического путей активации полностью совпадают.
Запускать лектиновый путь комплемента способны также фиколины, сходные по структуре с коллектинами. В состав фиколинов входят домены двух типов — N-концевые коллагеновые и С-концевые фибриногеноподобные. Последние способны в присутствии Са2+ связывать углеводы, прежде всего N-ацетилглюкозамин и маннозу. Таким образом, функционально (но не структурно) этот домен является С-лектином. Выделяют 3 вида фиколинов, обозначаемые буквами L (печеночный — от liver), H (от имени автора — Hakata) и M (моноцитарный — от monocyte). Два первых (L и H) присутствуют в плазме, фиколин M связан с мембраной моноцитов. L- и H-фиколины способны связывать и активировать протеазы группы MASP и, таким образом, запускать лектиновый путь активации каскада комплемента. Кроме того, L-фиколин обладает опсонизирующей активностью подобно сурфактантам А и D, относимым к группе коллектинов.
Атака клеточной мембраны
[править]Формирование С5-конвертазы альтернативного [Р(C3b)nBb] и классичес-кого (С14b2b3b) путей активации комплемента служит основой для осуществления терминальных стадий каскада, завершающегося лизисом клетки. Результаты действия обеих С5-конвертаз идентичны: они расщепляют молекулу С5 на крупный (С5b) и мелкий (С5а) фрагменты. Специфичность действия конвертаз альтернативного и классического пути связана соответственно с Bb и C2b, тогда как С3b участвует в связывании с нативной
молекулой С5. Образующийся С5b фрагмент связывается с комплексом компонентов комплемента, фиксированных на мембране клетки. Малый фрагмент С5а остается в жидкой фазе. Он обладает даже более выраженной хемотаксической и анафилактогенной активностью, чем С3а и С4а. Все упомянутые малые фрагменты факторов комплемента (С4а, С3а, С5а) инактивируются карбоксипептидазой N, но среди них С5а обладает наибольшей стабильностью.
Расщепление С5 запускает терминальный этап активации комплемента — формирование литического комплекса. Как на мембране,
так и в растворе С5b обладает способностью связывать компонент С6 с образованием комплекса С5bC6. Компоненты С5b и С6 обладают довольно слабым сродством к фиксированным на мембране комплексам С5-конвертазы. Именно поэтому большинство комплексов С5bС6 оказывается в жидкой фазе и инактивируется. С6 в составе комплекса спонтанно связывает компонент С7. Формируемый комплекс C5bС6С7 связывает С8. Скорость взаимодействия компонентов комплемента обусловлена их доступностью: все компоненты в норме присутствуют в сыворотке крови в достаточно высоких концентрациях. Связывание каждого нового фактора (начиная с С6) повышает сродство комплекса к следующим компонентам; при этом комплекс становится все более прочным. Связь комплекса с мембраной усиливается благодаря наличию у С7 и более поздних компонентов гидрофобных (липофильных) участков.
С8 ограничивает образование новых комплексов С5bС5С7 и их прикрепление к мембране, т.е. является регулятором поздних стадий активации комплемента. Гидрофобный участок в молекуле С8 более протяженный, чем в С7. В связи с этим комплекс С5bС6С7С8 насквозь прошивает мембрану. Уже на этом этапе комплекс факторов комплемента способен формировать поры. Однако их диаметр слишком мал (3 мкм), чтобы нарушить изоляцию клеток от среды и вызвать ее гибель. Комплекс С5bС6С7С8 вызывает
медленный лизис только эритроцитов. Возможно, этот слабовыраженный лизис клеток играет роль в защите от некоторых патогенов, поскольку генетические дефекты любого из факторов от С5 до С8 приводят к нарушению устойчивости к нейссериям, тогда как дефект С9 такого эффекта не вызывает.
Завершающий этап формирования литического комплекса состоит в присоединении к комплексу С5bС6С7С8 12–20 молекул С9, повышающих литическую активность комплекса в 1000 раз. Подобно родственному белку — перфорину, С9 способен к полимеризации. Поскольку С9 имеет гидрофобный участок, он встраивается в мембрану и полимеризуется в ней с образованием пронизывающего мембрану цилиндра, используя в качестве «строительного каркаса» комплекс С5bС6С7С8. Цилиндр, образуемый
компонентами С9, может быть извлечен из мембраны только с помощью детергентов. Внутрь цилиндра обращены гидрофильные участки молекулы, а гидрофобные участки — в сторону мембранного окружения. Молекулярная масса комплекса (1–1,7)×103 кДа. Высота цилиндра — около 15 нм, диаметр — 8–12 нм. Формирующиеся поры обеспечивают возможность поступления в клетку протонов, ионов Na+ и молекул воды (но не белков), что может привести к разрыву мембраны и гибели клетки по механизму некроза. В то же время роль прямого повреждения мембраны очевидна только для эритроцитов, но не для бактериальных клеток.
Комплекс С5bС6С7С8С9n может сформироваться и в жидкой фазе, но он лишен активности из-за присутствия в его составе сывороточного белка — фактора S, препятствующего формированию литически активного димера C5bС6С7С8С9. Аналогичной ингибирующей активностью обладают липопротеины низкой плотности. Некоторые ингибирующие вещества ( протектин, DAF, С4bp, гликофорин) взаимодействуют с атакующим комплексом в составе мембраны и препятствуют лизису клеток, в частности, аутолизу клеток хозяина.
Факторы контроля системы комплемента
[править]Уже упоминалось о факторах, инактивирующих и расщепляющих активные компоненты комплемента. Эти факторы играют важную роль в предотвращении повреждающего действия комплемента на собственные клетки организма, разрушая активные компоненты на клеточной мембране и в растворимой фазе. Компоненты комплемента, фиксированные на бактериальных клетках, расщепляются факторами рассматриваемой группы медленнее представленных в свободной форме.
При запуске классического пути активации комплемента действуют C1-ингибитор (C1inh). С1inh относят к семейству антитрипсиновых протеаз (серпинов). Он специфически связывает C1r и C1s, блокируя их активность в отношении молекулы С4 и отщепляя их от комплекса C1qrs. Известен наследственный дефект С1inh, называемый по главному клиническому проявлению ангионевротический отек. Причина такого отека, иногда представляющего угрозу жизни, состоит в чрезмерной активации калликреина (для которого С1inh служит ингибитором) и образовании вследствие этого
избыточных количеств кининов.
Большинство регуляторных факторов участвуют в контроле центрального звена активации комплемента, связанного с формированием и функционированием С3-конвертаз. Фактор I относят к нейтральным сериновым протеазам. Он обладает сродством к фрагментам C4b и C3b. Для проявления своей активности фактору I необходимо наличие кофакторов: сывороточных белков — фактора H и C4Bp (C4 binding protein), а также мембранных белков — С3-рецептора CR1 (Complement receptor 1) и кофакторного белка MCP (Membrane cofactor protein). C4Bp связывает сывороточный белок C4b. Затем C4b расщепляется фактором I. Факторы H, CR1 и MCP связывают C3b (как в растворимой фазе, так и на мембране) и облегчают взаимодействие с ним фактора I. Представленный почти на всех ядросодержащих клетках фактор DAF (Decay-activating factor, CD55) — мембранный ингибитор C3-конвертаз C4bC2b и C3bBb. DAF вызывает их распад и связывает фрагменты C3b или C4b. Факторы H и MCP отвечают преимущественно за контроль альтернативного, а C4Bp и DAF — классического пути активации комплемента.
На этапе литической атаки регулирующую роль выполняют витронектин, протектин и белок С8Вр (C8-binding protein). Адгезивный белок витронектин (S-протеин) связывается с комплексом C5bС6C7, препятствуя его взаимодействию с мембраной, и блокирует полимеризацию C9. C8Bp препятствует связыванию фактора С9 с С8, взаимодействуя с участком молекулы С8, к которому обладает сродством молекула С9.
Роль комплементзависимых процессов в иммунной защите и повреждении
[править]Комплементзависимый лизис бактериальных клеток — один из факторов противоинфекционной защиты, участвующий в повреждении микроорганизмов при инфекционном процессе. В то же время он обусловливает гемолиз при переливании несовместимой крови и анемии аутоиммунного генеза, участвует в повреждении ядросодержащих клеток при аутоиммунной патологии. Однако литическая функция комплемента в отношении ядросодержащих клеток, проявляется весьма слабо в связи с существованием на их поверхности белков, инактивирующих факторы комплемента. В настоящее время считают, что система комплемента вносит ограниченный вклад в защиту от патогенных микроорганизмов. В частности, комплемент эффективно уничтожает нессерий, поскольку, как уже отмечено, при наследственном дефекте компонентов литического комплекса снижается резистентность именно к этим возбудителям. При этом значимость С9 и, следовательно, комплементзависимого цитолиза, подвергается сомнению вследствие полной «безнаказанности» с клинической точки зрения инактивации его гена.
Роль системы комплемента в защите от патогенов заключается, по-видимому, в первую очередь в опсонизации клеток-мишеней, что делает их доступными для действия эффекторных клеток, имеющих рецепторы для компонентов комплемента, — прежде всего фагоцитов (макрофагов и нейтрофилов). Наиболее распространены рецепторы для C3b и его фрагментов C3d, C3bi, что свидетельствует об особой функциональной значимости избыточной фиксации С3b на поверхности клеток. Лимфоциты тоже имеют рецептор для фрагментов C3b (CR2, или CD21). Более того, CR2 в качестве корецептора входит в состав рецепторного комплекса В-лимфоцитов. Полагают, что распознавание опсонизированных клеток лимфоцитами (особенно В-клетками) является одним из механизмов, определяющих их активацию и участие в регуляции иммунных процессов. Иммунорегуляторная роль компонентов комплемента состоит и в солюбилизации (переводе в растворимую форму) иммунных комплексов.
Как уже упоминалось, освобождающиеся при активации комплемента фрагменты С4а, С3а и С5а — активные хемотаксические и сосудорасширяющие факторы, а С5а и С3а обладают анафилактогенной активностью и участвуют в реакциях воспаления и гиперчувствительности (отсюда их название — анафилатоксины). Рецепторы для этих фрагментов присутствуют на поверхности нейтрофилов и макрофагов, что обусловливает хемотаксический эффект названных фрагментов, а также на тучных клетках и
базофилах, что определяет их анафилактогенные функции. С4а, С3а и С5а играют особую роль в системе комплемента, поскольку факторы, ограничивающие их действие, отсутствуют (у всех остальных компонентов системы комплемента ингибиторы имеются).
Система комплемента взаимодействует с другими гуморальными системами, активируемыми при воспалительных процессах и способствует вовлечению этих систем в реакцию иммунного воспаления. Наконец, отложение компонентов комплемента в составе иммунных комплексов на биологических мембранах инициирует развитие иммунопатологии в результате привлечения в очаг поражения макрофагов и других эффекторов иммунного воспаления.
Белки острой фазы(С-реактивный протеин и маннансвязывающий лектин)
[править]Некоторые гуморальные реакции врожденного иммунитета по своему назначению аналогичны реакциям адаптивного иммунитета и могут
рассматриваться как их эволюционные предшественники. Такие реакции врожденного иммунитета имеют преимущество перед адаптивным иммунитетом в быстроте развития, однако недостаток их заключается в отсутствии специфичности в отношении антигенов. Пару сходных по результатам реакций врожденного и адаптивного иммунитета мы рассмотрели выше в разделе, посвященном комплементу (альтернативная и классическая активация комплемента). Другой пример будет рассмотрен в данном разделе: белки острой фазы в ускоренном и упрощенном варианте воспроизводят некоторые эффекты антител.
Белки (реактанты) острой фазы представляют группу протеинов, секретируемых гепатоцитами. При воспалении продукция белков острой фазы изменяется. При усилении синтеза белки называют положительными, а при понижении синтеза — отрицательными реактантнами острой фазы воспаления. Динамика и выраженность изменений сывороточной концентрации различных белков острой фазы при развитии воспаления неодинакова: концентарция С-реактивного белка и сывороточного амилоида Р возрастает очень сильно (в десятки тысяч раз) — быстро и кратковременно (практически нормализуется к концу 1-й недели); уровни гаптоглобина и фибриногена возрастают слабее (в сотни раз) соответственно на 2-й и 3-й неделях воспалительной реакции. В данной главе будут рассмотрены только положительные реактанты, участвующие в иммунных процессах.
Согласно выполняемым функциям выделяют несколько групп белков острой фазы. К транспортным белкам относят преальбумин, альбумин, орозомукоид, липокалины, гаптоглобин, трансферрин, маннозасвязывающий и ретинолсвязывающий белки и т. д. Они играют роль переносчиков метаболитов, ионов металлов, физиологически активных факторов. Роль факторов этой группы существенно возрастает и качественно изменяется при воспалении. Другую группу образуют протеазы (трипсиноген, эластаза, катепсины, гранзимы, триптазы, химазы, металлопротеиназы), активация которых необходима для формирования многих медиаторов воспаления, а также для осуществления эффекторных функций, в частности киллерной. Активация протеаз (трипсина, химотрипсина, эластазы, металлопротеиназ) уравновешивается накоплением их ингибиторов. α2-Макроглобулин участвует в подавлении активности протеаз разных групп. Помимо перечисленных, к белкам острой фазы относят факторы коагуляции и фибринолиза, а также белки межклеточного матрикса (например, коллагены, эластины, фибронектин) и даже белки системы комплемента.
Пентраксины
Наиболее полно проявляют свойства реактантов острой фазы белки семейства пентраксинов: в первые 2-3 сут развития воспаления их концентрация в крови повышается на 4 порядка.
Основа для выделения этого семейства белков — структурные особенности модуля, являющегося их обязательной составной частью. Пентраксиновый модуль представляет кольцевидный гомопентамер. Он состоит из 5 нековалентно связанных одинаковых субъединиц. Субъединица образована 206 аминокислотными остатками и имеет молекулярную массу около 20–23 кДа. Структура субъединицы стабилизируется дисульфидной связью, придающей ей форму глобулы, в которой преобладают β-слоистые структуры (примерно 50%), соединенные α-спирализированными участками (12%). Сердцевину каждого мономера образуют 2 антипараллельных β-слоя. Такие структуры обозначают термином «желатиновый рулет» ( jelly roll).
Выделяют 2 группы пентраксинов — короткие и длинные. К коротким, содержащим только пентраксиновые домены, относят 2 острофазых реактанта — С-реактивный белок и сывороточный амилоид Р. К длинным пентраксинам относят белки, содержащие С-концевой пентраксиновый домен и N-концевой домен (тоже пятичленный, но имеющий другую структуру). Наиболее изучен в этой группе белок РТХ3 (пентраксин 3).
С-реактивный белок и сывороточный амилоид Р образуются и секретируются гепатоцитами. Основной индуктор их синтеза — IL-6. Белок PTX3
вырабатывают миелоидные (макрофаги, дендритные клетки), эпителиальные клетки и фибробласты в ответ на стимуляцию через TLR, а также
под действием провоспалительных цитокинов (например, IL-1β, TNFα). Концентрация пентраксинов в сыворотке резко возрастает при воспалении: С-реактивного белка и сывороточного амилоида Р — с 1 мкг/мл до 1–2 мг/мл (т.е. в 1000 раз), РТХ3 — с 25 до 200–800 нг/мл. Пик концентрации достигается через 6–8 ч после индукции воспаления.
Для пентраксинов характерна способность связываться с самыми разнообразными молекулами. С-реактивный белок был впервые идентифицирован благодаря его способности связывать полисахарид С (Streptococcus рneumoniae), что и определило его название. Пентраксины взаимодействуют и с множеством других молекул: C1q, бактериальными полисахаридами, фосфорилхолином, гистонами, ДНК, полиэлектролитами, цитокинами, белками межклеточного матрикса, сывороточными липопротеинами, компонентами комплемента, друг с другом, а также с ионами Са
2+ и других металлов. Для всех рассматриваемых пентраксинов существуют высокоаффинные рецепторы на миелоидных, лимфоидных, эпителиальных и других клетках. Кроме того, эта группа белков острой фазы обладает достаточно высоким сродством к таким рецепторам, как FcγRI и FcγRII.
Многочисленность молекул, с которыми взаимодействуют пентраксины, определяет широкое разнообразие их функций. Распознавание и связывание
пентраксинами PAMP дает основание рассматривать их как вариант растворимых патогенраспознающих рецепторов. К наиболее важным функциям пентраксинов относят их участие в реакциях врожденного иммунитета в качестве факторов, запускающих активацию комплемента через C1q и участвующих в опсонизации микроорганизмов. Комплементактивирующая и опсонизирующая способность пентраксинов делает их своеобразными «протоантителами», частично выполняющими функции антител на начальном этапе иммунного ответа, когда истинные адаптивные антитела еще не успели выработаться. Роль пентраксинов во врожденном иммунитете заключается также в активации нейтрофилов и моноцитов/макрофагов, регуляции синтеза цитокинов и проявлении хемотаксической активности по отношению к нейтрофилам.
Помимо участия в реакциях врожденного иммунитета пентраксины регулируют функции межклеточного матрикса при воспалении, контроле апоптоза и элиминации апоптотических клеток.
К этой группе медиаторов относят гистамин и серотонин, содержащиеся в гранулах тучных клеток. Освобождаясь при дегрануляции, эти амины вызывают разнообразные эффекты, играющие ключевую роль в развитии ранних проявлений гиперчувствительности немедленного типа.
Гистамин (5-β-имидазолилэтиламин) — главный медиатор аллергии. Он образуется из гистидина под влиянием фермента гистидиндекарбоксилазы. Поскольку гистамин содержится в гранулах тучных клеток в готовом виде, а процесс дегрануляции происходит быстро, гистамин очень рано появляется в очаге аллергического поражения, причем сразу в большой концентрации, что определяет проявления немедленной гиперчувствительности. Гистамин-быстро метаболизируется (95% за 1 мин) с участием 2 ферментов — гистамин-N-метилтрансферазы и диаминооксидазы ( гистаминазы); при этом образуется (в соотношении примерно 2:1) соответственно N-метилгистамин и имидазолацетат .
Известно 4 разновидности рецепторов для гистамина Н1-Н4. При аллергических процессах гистамин действует преимущественно на гладкие мыщцы и эндотелий сосудов, связываясь с их Н1-рецепторами. Эти рецепторы поставляют активационный сигнал, опосредованный превращениями фосфоинозитидов с образованием диацилглицерола и мобилизацией Са2+. Этот процесс в различных клетках проявляется по-разному, однако конечный результат его — расширение сосудов с усилением локального кровотока и повышением проницаемости капилляров. Указанные эффекты частично обусловлены образованием в клетках (мишенях гистамина) оксида азота и простациклина. Действуя на нервные окончания, гистамин вызывает ощущение зуда, характерного для аллергических проявлений в коже.
У человека гистамин играет важную роль в развитии кожной гиперемии и аллергического ринита. Менее очевидно его участие в развитии общих аллергических реакций и бронхиальной астмы. В то же время через Н2-рецепторы гистамин и родственные вещества оказывают регуляторное действие, иногда уменьшающее проявления воспаления, ослабляя хемотаксис нейтрофилов и выброс ими лизосомных ферментов, а также высвобождение самого гистамина. Через Н2-рецепторы гистамин действует на сердце, секреторные клетки желудка, подавляет пролиферацию и цитотоксическую активность лимфоцитов, а также секрецию ими цитокинов. Большинство этих эффектов опосредовано активацией аденилатциклазы и повышением внутриклеточного уровня цАМФ. Данные об относительной роли различных рецепторов гистамина в реализации его действия очень
важны, поскольку многие антиаллергические препараты представляют собой блокаторы Н1 (но не Н2 и других) рецепторов гистамина.
Липидные медиаторы. Эйкозаноиды
[править]Важную роль в регуляции иммунных процессов, а также в развитии аллергических реакций играют гуморальные факторы липидной природы. Наиболее многочислены и важны из них эйкозаноиды.
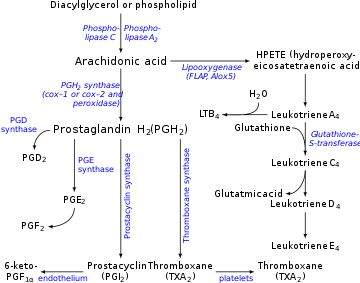 |
 |
Эйкозаноиды — продукты метаболизма арахидоновой кислоты — жирной полиненасыщенной кислоты, молекула которой содержит 20 атомов углерода и 4 ненасыщенные связи. Арахидоновая кислота образуется из мембранных фосфолипидов как прямой продукт действия фосфолипазы А (PLA) или косвенный продукт превращений, опосредованных PLC. Образование арахидоновой кислоты или эйкозаноидов происходит при активации различных типов клеток, особенно участвующих в развитии воспаления, в частности аллергического: эндотелиальных и тучных клеток, базофилов, моноцитов и макрофагов. Метаболизм арахидоновой кислоты может проходить по 2 путям — катализироваться циклооксигеназой или 5’-липоксигеназой. Циклооксигеназный путь приводит к образованию простагландинов и тромбоксанов из нестабильных промежуточных продуктов — эндоперекисных простагландинов G2 и H2, а липоксигеназный — к образованию лейкотриенов и 5-гидроксиэйкозатетраеноата через промежуточные продукты (5-гидроперокси-6,8,11,14-эйкозатетраеновую кислоту и лейкотриен А4), а также липоксинов — продуктов двойной липоксигенации (под действием двух липоксигеназ — см. далее).
Простагландины и лейкотриены во многих отношениях проявляют альтернативные физиологические эффекты, несмотря на то, что внутри этих групп существуют значительные различия в активности. Общее свойство этих групп факторов — преобладающее действие на стенку сосудов и гладкие мышцы, а также хемотаксический эффект. Эти эффекты реализуются при взаимодействии эйкозаноидов со специфическими рецепторами на поверхности клеток. Некоторые представители семейства эйкозаноидов усиливают действие других вазоактивных и хемотаксических факторов, например, анафилатоксинов (С3а, С5а).
Лейкотриены (LT) — С20 -жирные кислоты, молекула которых в положении 5 содержит ОН-группу, а в положении 6 — боковые серосодержащие цепи, например глутатион. Выделяют 2 группы лейкотриенов: одна из них включает лейкотриены С4, D4 и Е4, называемые цистеиниллей-котриенами (Cys-LT), во вторую входит один фактор — лейкотриен B4. Лейкотриены образуются и секретируются в течение 5–10 мин после активации тучных клеток или базофилов. Лейкотриен C4 присутствует в жидкой фазе в течение 3–5 мин, при этом он превращается в лейкотриен D4. Лейкотриен D4 существует в последующие 15 мин, медленно превращаясь в лейкотриен E4.
Лейкотриены оказывают свое действие через рецепторы, относящиеся к группе пуриновых рецепторов семейства родопсиноподобных рецепторов, 7-кратно пронизывающих мембрану и связанных с протеином G. Известны 2 группы рецепторов для лейкотриенов — CysLT-R и BLT-R соответственно для цистеиниллейкотриенов и лейкотриена B. В каждую группу входят по 2 разновидности рецепторов (CysLT-R1, Cys-LT-R2, BLT-R1 и BLT-R2). Сродство лейкотриена E к CysLT-R выше, чем лей-котриенов D и C. CysLT-R1 имеет максимальное сродство к лейкотриену D, тогда как CysLT-R2 с одинаковой эффективностью связывает лейкотриены D и C. Рецепторы лейкотриенов экспрессируются на клетках селезен-ки, лейкоцитах крови, кроме того, CysLT-R1 представлен на макрофагах, клетках кишечника, воздухоносного эпителия, а CysLT-R2 — на клетках надпочечников и головного мозга.
Цистеиниловые лейкотриены (особенно лейкотриен D4) вызывают спазм гладкой мускулатуры и регулируют локальный кровоток, снижая артериальное давление. Активность лейкотриена D4 в отношении гладких мышц в 100 раз выше, чем у гистамина, и в 2–4 раза выше, чем лейкотриенов C4 и E4. Лейкотриены С4 и Е4 также оказывают хемотаксическое действие, но более слабое, чем лейкотриен D4. Цистеиниловые лейкотриены — медиаторы аллергических реакций, в частности, медленной фазы бронхоспазма при
бронхиальной астме. Кроме того, они подавляют пролиферацию лимфоцитов и способствуют их дифференцировке. Ранее комплекс этих факторов (лейкотриены C4, D4 и E4) называли медленнореагирующей субстанцией А. Лейкотриен B4 (дигидроксиэйкозатетраеновая кислота) проявляет хемотаксическое и активирующее действие преимущественно в отношении
моноцитов, макрофагов, нейтрофилов, эозинофилов и даже Т-клеток. Еще один продукт липоксигеназного пути — 5-гидроксиэйкозатетраеноат — менее активен, чем лейкотриены, но может служить хемоаттрактантом и активатором нейтрофилов и тучных клеток.
Простагландины (PG) — С20 -жирные кислоты, молекула которых содержит циклопентановое кольцо. Варианты простагландинов, отличающиеся по типу и положению замещающих групп (окси-, гидрокси-), обозначаются различными буквами; цифры в названии означают число ненасыщенных связей в молекуле. Простагландины накапливаются в очаге воспаления позже кининов и гистамина, несколько позже лейкотриенов, но одновременно с монокинами (через 6–24 ч после запуска воспаления). Помимо вазоактивного и хемотаксического эффекта, достигаемого в кооперации с другими факторами, простагландины (особенно простагландин E2) оказывают регулирующее действие при воспалительных и иммунных процессах.
Экзогенный простагландин E2 вызывает некоторые проявления воспалительной реакции, но подавляет иммунный ответ и аллергические реакции. Так, простагландин E2 снижает цитотоксическую активность макрофагов, нейтрофилов и лимфоцитов, пролиферацию лимфоцитов, выработку этими клетками цитокинов. Он способствует дифференцировке незрелых лимфоцитов и клеток других кроветворных рядов. Некоторые эффекты простагландина Е2 связаны с повышением уровня внутриклеточного цАМФ. Простагландины E2 и D2 подавляют агрегацию тромбоцитов; простагландины F2 и D2 вызывают сокращение гладкой мускулатуры бронхов, тогда как простагландин E2 расслабляет ее.
Тромбоксан А2 (ТХА2) — С20 -жирная кислота; в его молекуле есть 6-членное кислородсодержащее кольцо. Это очень нестабильная молекула (время полужизни — 30 с), превращающаяся в неактивный тромбоксан В2.
Тромбоксан А2 вызывает сужение сосудов и бронхов, агрегацию тромбоцитов с высвобождением из них ферментов и других активных факторов, способствующих митогенезу лимфоцитов. Другой продукт циклоксигеназного пути — простагландин I2 (простациклин) — тоже нестабилен. Он проявляет свое действие через цАМФ, сильно расширяет сосуды, увеличивает их проницаемость, ингибирует агрегацию тромбоцитов. Наряду с пептидным фактором брадикинином простациклин вызывает ощущение
боли при воспалении.
Общая характеристика цитокинов
[править]Цитокины — самая многочисленная, наиболее важная и универсальная в функциональном отношении группа гуморальных факторов системы иммунитета, в равной степени важная для реализации врожденного и адаптивного иммунитета. Цитокины участвуют во многих процессах; их нельзя назвать факторами, относящимися исключительно к иммунной системе, поскольку они играют важную роль в кроветворении, тканевом гомеостазе,
межсистемной передаче сигналов.
Цитокины можно определить как белковые или полипептидные факторы, лишенные специфичности в отношении антигенов, продуцируемые преимущественно активированными к летками кроветворной и иммунной систем и опосредующие межк леточные взаимодействия при кроветворении, воспа лении, иммунных процессах и межсистемных коммуникациях.
Существует несколько классификаций цитокинов, основанных на разных принципах. Традиционная классификация отражает историю изучения
цитокинов. Идея о том, что цитокины играют роль факторов, опосредующих функциональную активность клеток иммунной системы, возникла после
открытия гетерогенности популяции лимфоцитов и осмысления факта, что только некоторые из них — В-лимфоциты — ответственны за образование
антител. Пытаясь выяснить, не играют ли гуморальные продукты Т-клеток роль в реализации их функций, начали изучать биологическую активность факторов, содержащихся в культуральной среде Т-лимфоцитов (особенно активированных). Решение этой задачи, а также возникшего вскоре вопроса о гуморальных продуктах моноцитов/макрофагов, привело к открытию цитокинов. Вначале их называли лимфокинами и монокинами, в зависимости от того, какие клетки их продуцировали — Т-лимфоциты или моноциты. Вскоре выяснилось, что четко разграничить лимфокины и монокины нельзя, и был введен общий термин — «цитокины». В 1979 г. на симпозиуме по лимфокинам в Интерлакене (Швейцария) установили правила идентификации факторов этой группы, которым присвоили групповое название «интерлейкины» (IL) (название не только отражает способность этих молекул опосредовать межлейкоцитарные взаимодействия, но и несет отзвук названия места, где родился этот термин). Тогда же свои названия получили два первых члена этой группы молекул — IL-1 и IL-2. С тех пор все новые цитокины (кроме хемокинов — см. далее) получали обозначение IL и порядковый номер.
Изучение биологической роли цитокинов показало, что некоторые цитокины и даже целые их группы уже давно открыты и получили другие
названия (которые за ними были сохранены). Это касается цитокинов с противовирусной активностью — интерферонов (IFN), колониестимулирующих факторов — CSF (цитокины с гемопоэтической активностью, поддерживающие рост кроветворных клеток) и факторов некроза опухоли — TNF (медиатор ЛПС, вызывающий некроз опухолевых клеток). Наконец, после введения термина «интерлейкин» была описана еще одна группа цитокинов — хемокины (хемотаксические цитокины). Общим для всех перечисленных групп признано название «цитокины». Первоначально к цитокинам относили только растворимые факторы. Однако со временем выяснилось, что некоторые из них (например IL-1αу человека) существуют в основном в связанной с мембранами форме. Затем оказалось, что целым семействам цитокинов (например, семейству TNF) больше свойственна мембранная, чем секретируемая форма.
В последние годы в связи с идентификацией большого числа новых цитокинов, иногда родственных ранее описанным, и образующих с ними единые группы, стали широко использовать классификацию, основанную на принадлежности цитокинов к структурно-функциональным семействам.
- Гемопоэтические факторы (CSF-G,-M,-GM, IL-3 и IL-7, эритропоэтин) – стимуляторы роста и созревания не-зрелых кроветворных клеток.
- Регуляторы естественного иммунитета – провоспалительные цитокины (IFNα, β, IL-1 и IL-6, TNFα, хемокины - IL-8, MCP-1, RANTES и др.). Они участвуют в неспецифической защите организма от бактериальных и вирусных инфекций. Их основными мишенями являются клетки-фагоциты – макрофаги и гранулоциты.
- Цитокины, регулирующие специфические иммунные реакции (IL-2 и IL-4, трансформирующий фактор роста (TGFβ) и др.). Эти белки участвуют в активации, росте и дифференцировке зрелых лимфоцитов.
- Цитокины, регулирующие воспалительные реакции, развивающиеся в процессе специфического иммунного ответа (INFγ, лимфотоксин,IL-5, IL-10 и др.). Их основная функция – активация неспецифических эффекторных клеток: цитотоксических макрофагов и естественных киллеров.
Еще одна классификация цитокинов (основана на структурных особенностях их рецепторов) будет приведена при описании цитокиновых рецепторов.
Гены цитокинов расположены в самых разных хромосомах, однако в некоторых случаях выявляется определенная закономерность. Так, 6 генов —
IL3, IL4, IL5, IL9, IL13, GMCSF— формируют кластер в длинном плече хромосомы 5 человека (сегмент 5q23–33). В длинном плече хромосомы 2
локализованы гены, кодирующие несколько представителей семейства IL-1. Полагают, что это отражает происхождение разнообразия этих генов за счет дупликаций. Гены цитокинов семейства фактора некроза опухоли (TNF, LTAи LТB) расположены в пределах MHC (короткое плечо хромосомы 6); формально их относят к молекулам МНС класса III.
Хотя разделение на монокины и лимфокины уже не применяют, необходимо признать, что существует 2 основных типа клеток-продуцентов цитокинов, отличающиеся кинетикой экспрессии генов и выработки белковых продуктов (цитокинов) — миелоидные и лимфоидные клетки. Наиболее
активные продуценты — соответственно моноциты/макрофаги и Т-лимфоциты хелперной (CD4+) субпопуляции. В миелоидных клетках процессы активации цитокиновых генов и секреции цитокинов происходят быст-рее, чем в лимфоидных. Однако даже в клетках одного типа различия в
кинетике экспрессии генов и синтеза различных цитокинов могут быть существенными. Так, экспрессия гена IL-1β(появление мРНК) в моноцитах
человека регистрируют через 15 мин после стимуляции ЛПС, она достигает максимума через 3–4 ч, в то время как экспрессия гена IL-1α в тех же условиях начинается через 3–4 ч и достигает максимума только через 11–12 ч. Преобладающее количество белка IL-1α синтезируется в мембраносвязанной форме. У Т-лимфоцитов экспрессию мРНК IL-2 регистрируют через 1 ч после стимуляции клеток митогеном, и она достигает максимума через 4–6 ч, а белковый продукт появляется в секрете через 6–10 ч, достигая максимальной концентрации к 24 ч, после чего секреция ослабевает. Экспрессия генов IFNG и IL4 и синтез соответствующих цитокинов происходит медленнее. Причины кратковременности экспрессии генов индуцибельных цитокинов — регуляторные механизмы, быстро ограничивающие экспрессию гена, а также короткий срок жизни мРНК.
Рецепторы для цитокинов
[править]| Тип | Примерами | Структура | Механизм |
|---|---|---|---|
| I тип рецепторов цитокинов | Некоторые консервативные мотивы в их внеклеточного аминокислоты домена. Подключен к Янус-киназы (JAK) семейство тирозинкиназы | JAK фосфорилируют и активировать вниз по течению белков, участвующих в их [трансдукции сигнала]] пути | |
| II типа рецепторов цитокинов | |||
| Многие члены "'иммуноглобулина надсемейство"' | Share структурных гомология с иммуноглобулинами (антитела), cell adhesion moleculeы, и даже некоторые Цитокины. | ||
| Рецепторы фактора некроза опухоли | цистеин-богатым общим внеклеточного привязки домена | ||
| Рецепторы хемокиновs | Семь трансмембранных спирали | G-белок-в сочетании | |
| TGF-бета-рецепторов |
Действие цитокинов осуществляется через рецепторы. По особенностям структуры полипептидных цепей выделяют несколько групп цитокиновых рецепторов. Приводимую классификацию применяют именно к полипептидным цепям. В состав одного рецептора могут входить цепи, относящиеся к разным семействам. Важность этой классификации обусловлена тем, что для разных типов полипептидных цепей рецепторов характерен определенный сигнальный аппарат, состоящий из тирозинкиназ, адапторных белков
и транскрипционных факторов.
В таблице представлено 6 структурных вариантов цитокиновых рецепторов, из которых 5 отображено на рисунке. Наиболее многочисленный тип — цитокиновые гемопоэтиновые рецепторы. Для их внеклеточных доменов характерно наличие 4 остатков цистеина и присутствие последовательности, содержащей остатки триптофана и серина — WSXWS. Домены семейства фибронектина, содержащие 4 остатка цистеина, составляют основу рецепторов интерферонов. Характерная черта доменов, образующих внеклеточную часть рецепторов семейства TNFR, — высокое содержание остатков цистеина («богатые цистеином домены»). Эти домены содержат 6 остатков цистеина. Группа рецепторов, внеклеточные домены которых относят к суперсемейству иммуноглобулинов, включает две группы — рецепторы для IL-1 и несколько рецепторов, цитоплазматическая часть которых обладает тирозинкиназной активностью. Тирозинкиназная активность свойственна цитоплазматической части практически всех ростовых факторов (EGF, PDGF, FGF и т.д.). Наконец, особую группу образуют родопсиноподобные рецепторы хемокинов, 7-кратно пронизывающие мембрану. Однако не все полипептидные цепи рецепторов соответствуют этой классификации. Так, ни α-, ни β-цепи рецептора IL-2 не относят к семействам, представленным в таблице (α-цепь содержит домены контроля комплемента). В основные группы также не входят рецепторы IL-12, общая β-цепь рецепторов IL-3, IL-5, GM-CSF и некоторые другие полипептидные цепи рецепторов.

Практически все цитокиновые рецепторы (кроме иммуноглобулиноподобных, обладающих киназной активностью) состоят из нескольких полипептидных цепей. Нередко разные рецепторы содержат общие цепи. Наиболее яркий пример — γ-цепь, общая для рецепторов IL-2, IL-4, IL-7, IL-9, IL-15, IL-21, обозначаемая как γ(с). Дефекты этой цепи играют важную роль в развитии иммунодефицитной патологии . Общая β-цепь входит в состав рецепторов GM-CSF, IL-3 и IL-5. Общие цепи имеют IL-7 и TSLP
(α-цепь), а также IL-2 и IL-15, IL-4 и IL-13 (в обоих случаях — β-цепь).

Роль субъединичного состава в формировании аффинности рецептора удобно иллюстрировать на примере рецептора для IL-2. Все полипептидные цепи, входящие в его состав, участвуют в формировании связывающего участка для IL-2 — 3 варианта этого рецептора с разным сродством к IL-2 (низким, промежуточным и высоким) различаются по «степени укомплектованности» полипептидными цепями (рис. 2.51). Так, отдельно экспрессируемая α-цепь способна связывать IL-2 с низким сродством (Кd=10-8 М), но не способна передавать сигнал в клетку. Димер βγ обладает промежуточным сродством к IL-2 (Kd=10-9 M); этот вариант рецептора присутствует на поко-ящихся клетках и естественных киллерах, причем на последних он передает сигнал. Активированные Т-клетки, а также регуляторные Т-клетки и некоторые естественные киллеры экспрессируют высокоаффинный тримерный рецептор состава αβγ с Kd=10-10 М.
Как правило, рецепторы представлены на поверхности покоящихся клеток в небольшом количестве и нередко в неполном субъединичном составе. Обычно в таком состоянии рецепторы обеспечивают адекватный ответ только при действии очень высоких доз цитокинов. При активации клеток число мембранных рецепторов цитокинов увеличивается на порядки, более того, эти рецепторы «доукомплектовываются» полипептидными цепями, как это было показано выше на примере рецептора для IL-2. Под влиянием активации число молекул этого рецептора значительно возрастает и в их составе появляется α-цепь, ген которой экспрессируется в процессе активации. Благодаря таким изменениям лимфоцит приобретает способность пролиферировать в ответ на действие IL-2.
Внутриклеточная передача сигнала при действии цитокинов
[править]В состав С-концевой цитоплазматической части некоторых цитокиновых рецепторов (относящихся к суперсемейству иммуноглобулинов) входит домен, обладающий активностью тирозинкиназы. Все эти киназы относятся к разряду протоонкогенов, т.е. при изменении генетического окружения становятся онкогенами, обеспечивая бесконтрольную пролиферацию клетки. Эти киназы имеют собственное название. Так, киназу, входящую в состав рецептора M-CSF, обозначают как c-Fms; киназу SCF — c-Kit; известна киназа гемопоэтического фактора — Flt-3 (Fms-like thyrosine kinase 3). Рецепторы, обладающие собственной киназной активностью, запускают передачу сигнала непосредственно, поскольку их киназа обусловливает фосфорилирование как самого рецептора, так и прилежащих к нему молекул.
Наиболее типичный вариант проявления активности характерен для рецепторов гемопоэтинового (цитокинового) типа, содержащих 4 α-спиральных домена. К цитоплазматической части таких рецепторов примыкают молекулы тирозинкиназ группы Jak-киназ (Janus-associated family kinases). В цитоплазматической части цепей рецепторов есть специальные участки для связывания этих киназ (проксимальный и дистальный боксы). Всего известно 5 Janus-киназ — Jak1, Jak2, Jak3, Tyk1 и Tyk2. Они в различных комбинациях кооперируются с разными цитокиновыми рецепторами, обладая сродством к конкретным полипептидным цепям. Так, киназа Jak3 взаимодействует с γ(с)-цепью; при дефектах гена, кодирующего эту киназу, развивается комплекс нарушений в иммунной системе сходный с наблюдаемым при дефектах гена полипептидной цепи рецептора.

При взаимодействии цитокина с рецептором происходит генерация сигнала, приводящего к формированию транскрипционных факторов и активации генов, определяющих реакцию клетки на действие цитокина. Одновременно происходит поглощение клеткой комплекса цитокина с рецептором и расщепление его в эндосомах. Сама по себе интернализация этого комплекса к передаче сигнала отношения не имеет. Она необходима для утилизации цитокина, предотвращающей его накопление в месте активации клеток-продуцентов. Большую роль в регуляции этих процессов играет сродство рецептора к цитокину. Только при достаточно высокой степени сродства (порядка 10-10 М) генерируется сигнал и происходит поглощение комплекса цитокина с рецептором.
Индукция сигнала начинается с аутокаталитического фосфорилирования связанных с рецептором Jak-киназ, запускаемого конформационными измененями рецептора, которые происходят в результате его взаимодействия с цитокином. Активированные Jak-киназы фосфорилируют цито-плазматические факторы STAT (Signal transducers and activators of transcription), присутствующие в цитоплазме в неактивной мономерной форме. Фосфорилированные мономеры приобретают сродство друг к другу и димеризуются. Димеры STAT перемещаются в ядро и выступают в качестве транскрипционных факторов, связываясь с промоторными участками генов-мишеней. При действии провоспалительных цитокинов активируются гены молекул адгезии, самих цитокинов, ферментов окислительного метаболизма и др. При действии факторов, вызывающих пролиферацию клеток, происходит индукция генов, ответственных за прохождение клеточного цикла и т.д.
Выделяют 6 разновидностей факторов STAT. В передаче сигналов от разных цитокинов принимают участие разные молекулы STAT. Так, в ответе на цитокины, рецепторы которых содержат γ(с)-цепь, связанную с киназой Jak3, участвуют факторы STAT5а и STAT5b. В передаче сигнала при действии цитокинов семейства IL-6 участвует фактор STAT3, IFNγ — STAT1, IL-12 — STАT4, IL-4 — STAT6 и т.д.
| Цитокины | Jak | STAT |
|---|---|---|
| IL-2 | Jak1, Jak3 | STAT1, STAT3, STAT5 |
| IL-4 | Jak1, Jak3 | STAT6 |
| IL-3, IL-5, GM-CSF | Jak2 | STAT5, STAT6 |
| IL-6, LIF, OSM | Jak1, Jak2, TYK2 | STAT1, STAT3, STAT5 |
| IL-7 | Jak1, Jak3 | STAT5 |
| IL-10 | Jak1, TYK2 | STAT1, STAT3, STAT5 |
| IL-11 | Jak1, Jak2 | STAT1, STAT3 |
| IL-12 | Jak2, TYK2 | STAT4 |
| IL-13 | Jak1, TYK2 | STAT6 |
| IL-15 | Jak1, Jak3 | STAT3, STAT5 |
| G-CSF | Jak1, Jak2 | STAT3 |
| IFNα, IFNβ | Jak1, TYK2 | STAT1, STAT2, STAT3, STAT4 |
| IFN-γ | Jak1, Jak2 | STAT1 |
Jak/STAT-опосредованный путь передачи сигналов от цитокинов — основной, но не единственный. С рецептором связаны не только
Jak-киназы, но и киназы семейства Src, а также PI3K. Их активация запускает дополнительные сигнальные пути, приводящие к активации АР-1 и других транскрипционных факторов. Активируемые транскрипционные факторы участвуют не только в передаче сигнала от цитокинов, но и в других сигнальных путях.
Существуют сигнальные пути, участвующие в контроле биологических эффектов цитокинов. Такие пути связаны с факторами группы SOCS (Suppressors of cytokine signaling), содержащей фактор SIC и 7 факторов SOCS (SOCS-1 — SOCS-7). Включение этих факторов происходит при активации цитокиновых сигнальных путей, что приводит к образованию петли отрицательной обратной связи. Факторы SOCS содержат домен SH2 , участвующий в реализации одного из следующих процессов:
- прямого ингибирования Jak-киназ в результате связывания с ними и индукции их дефосфорилирования;
- конкуренции с факторами STAT за связывание с цитоплазматической частью цитокиновых рецепторов;
- ускорения деградации сигнальных белков по убиквитиновому пути.
Выключение генов SOCS приводит к нарушению баланса цитокинов с преобладанием синтеза IFNγ и сопутствующей этому лимфопенией и усилением апоптоза.
Особенности функционирования системы цитокинов.
[править]Из сказанного выше следует, что при активации клеток чужеродными агентами (носителями PAMP при активации миелоидных клеток и антигенами при активации лимфоцитов) индуцируется (или усиливается до функционально значимого уровня) как синтез цитокинов, так и экспрессия их рецепторов. Это создает условия для локального проявления эффектов цитокинов. Действительно, если один и тот же фактор активирует и клетки-продуценты цитокинов, и клетки-мишени, создаются оптимальные
условия для локального проявления функций этих факторов.
Обычно цитокины связываются, подвергаются интернализации и расщеплению клеткой-мишенью, практически не диффундируя от секретируемых клеток-продуцентов. Нередко цитокины бывают трансмембранными молекулами (например, IL-1α и TNFα) или представляются клеткам-мишеням в связанном с пептидогликанами межклеточного матрикса состоянии (IL-7 и ряд других цитокинов), что также способствует локальному характеру их действия.
В норме цитокины если и содержатся в сыворотке крови, то в концентрациях, недостаточных для проявления их биологических эффектов. Далее на примере воспаления мы рассмотрим ситуации, в которых цитокины оказывают системное действие . Однако эти случаи всегда являются проявлением патологии, иногда очень серьезной. По-видимому, локальный характер действия цитокинов имеет для нормального функционирования организма принципиальное значение. Об этом свидетельствует высокая скорость их выведения через почки. Обычно кривая выведения цитокинов состоит из двух компонент — быстрой и медленной. Т1/2 быстрой компоненты для IL-1β составляет 1,9 мин, для IL-2 — 5 мин (Т1/2 медленной составляет 30–120 мин). Свойство близкодействия отличает цитокины от гормонов — дальнодействующих факторов (поэтому утверждение «цитокины — это гормоны иммунной системы» принципиально неверно).
Цитокиновая сеть
[править]Для системы цитокинов характерна избыточность. Это означает, что практически любую выполняемую конкретным цитокином функцию дублируют другие цитокины. Именно поэтому выключение отдельного цитокина, например, вследствие мутации его гена, не вызывает фатальных последствий для организма. Действительно, мутация гена конкретного цитокина практически никогда не приводит к развитию иммунодефицита. Например, IL-2 известен как фактор роста Т-клеток; при искусственном удалении (путем генетического нокаута) кодирующего его гена существенного нарушения пролиферации Т-клеток не выявляют, однако регистрируют изменения, обусловленные дефицитом регуляторных Т-клеток. Это связано с тем, что пролиферацию Т-клеток в отсутствие
IL-2 обеспечивают IL-15, IL-7, IL-4, а также комбинации нескольких цитокинов (IL-1β, IL-6, IL-12, TNFα). Точно так же дефект гена IL4 не приводит к значительным нарушениям в системе В-клеток и переключении изотипов иммуноглобулинов, поскольку сходные эффекты проявляет IL-13. В то же время некоторые цитокины не имеют функциональных аналогов. Наиболее
известный пример незаменимого цитокина — IL-7, лимфопоэтическое действие которого, по крайней мере на определенных этапах Т-лимфопоэза уникально, в связи с чем дефекты генов самого IL-7 или его рецептора приводят к развитию тяжелой комбинированной иммунной недостаточности (ТКИН).
Помимо избыточности, в системе цитокинов проявляется и другая закономерность: цитокины плейотропны (действуют на различные мишени) и полифункциональны (вызывают различные эффекты). Так, число клеток-мишеней IL-1β и TNFα с трудом поддается учету. Столь же разнообразны вызываемые ими эффекты, участвующие в формировании комплексных реакций: воспаления, некоторых этапов гемопоэза, нейротропных и других реакций.
Еще одна важная черта, свойственная системе цитокинов, — взаимосвязь и взаимодействие цитокинов. С одной стороны, это взаимодействие заключается в том, что одни цитокины, действуя на фоне индукторов или самостоятельно, вызывают или усиливают (реже подавляют) выработку других цитокинов. Наиболее яркие примеры усиливающего действия — активность
провоспалительных цитокинов IL-1β и TNFα, усиливающих собственную выработку и образование других провоспалительных цитокинов (IL-6, IL-8, других хемокинов). IL-12 и IL-18 являются индукторами IFNγ. TGFβ и IL-10, наоборот, подавляют выработку различных цитокинов. IL-6 проявляет ингибирующую активность в отношении провоспалительных цитокинов, а IFNγ и IL-4 взаимно подавляют выработку друг друга и цитокинов соответствующих (Th1 и Th2) групп. Эти взаимоотношения цитокинов
будут подробнее рассмотрены при описании субпопуляций Т-хелперных клеток . Взаимодействие между цитокинами проявляется
и на функциональном уровне: одни цитокины усиливают или подавляют действие других цитокинов. Описаны синергизм (например, внутри группы провоспалительных цитокинов) и антагонизм цитокинов (например, между Th1- и Th2-цитокинами).
Cуммируя полученные данные, можно заключить, что ни один из цитокинов не существует и не проявляет своей активности изолированно — на всех уровнях цитокины испытывают влияние других представителей этого класса молекул. Результат такого многообразного взаимодействия иногда может быть неожиданным. Так, при использовании в лечебных целях высоких доз IL-2 возникают опасные для жизни побочные эффекты, некоторые из которых (например, шок, подобный токсическому, без бактериемии)
удается снять антителами, направленными не против IL-2, а против TNFα. Наличие множественных перекрестных взаимодействий в системе цитокинов послужило причиной создания понятия «цитокиновая сеть», достаточно четко отражающего суть явления.

Для цитокиновой сети характерны следующие свойства:
- индуцибельность синтеза цитокинов и экспрессии их рецепторов;
- локальность действия, обусловленная скоординированной экспрессией цитокинов и их рецепторов под влиянием одного и того же индуктора;
- избыточность, объясняющаяся перекрыванием спектров действия разных цитокинов;
- взаимосвязи и взаимодействие, проявляющиеся на уровне синтеза и реализации функций цитокинов.
Провоспалительные цитокины
[править]Цитокины — ключевые гуморальные факторы воспаления, необходимые для реализации защитных функций врожденного иммунитета. В развитии воспаления участвуют три группы цитокинов — воспалительные, или провоспалительные цитокины, хемокины, колониестимулирующие факторы, а также функционально связанные факторы IL-12 и IFNγ. Цитокинам также принадлежит важная роль в подавлении и сдерживании воспалительной реакции. К противовоспалительным цитокинам относят трансформирующий фактор роста β (TGFβ), IL-10; часто роль противовоспалительного фактора играет IL-4.
Выделяют 3 основных представителя группы провоспалительных цитокинов — TNFα, IL-1 и IL-6; относительно недавно к ним были добавлены IL-17 и IL-18. Эти цитокины продуцируются в основном активированными моноцитами и макрофагами преимущественно в очаге воспаления. Провоспалительные цитокины могут вырабатываться также нейтрофилами, дендритными клетками, активированными В-, NK- и Т-лимфоцитами. В очаге проникновения патогенов цитокины первыми начинают синтезировать немногочисленные местные воспалительные макрофаги. Затем в про-ессе эмиграции лейкоцитов из кровотока численность клеток-продуцентов возрастает и их спектр расширяется. В частности, к синтезу провоспалительных цитокинов подключаются стимулированные продуктами микроорганизмов и факторами воспаления эпителиальные, эндотелиальные, синовиальные, глиальные клетки, фибробласты. Гены цитокинов относят к индуцибельным. Естественные индукторы их экспрессии — патогены и их продукты, действующие через ТLR и другие патогенраспознающие рецепторы. Классический индуктор — бактериальный ЛПС. В то же время некоторые провоспалительные цитокины (IL-1, TNFα) сами способны индуцировать синтез провоспалительных цитокинов.
Провоспалительные цитокины синтезируются и секретируются достаточно быстро, хотя кинетика синтеза различных цитокинов этой группы неодинакова. В типичных случаях (быстрый вариант) экспрессию их мРНК отмечают через 15–30 мин после индукции, появление белкового продукта в цитоплазме — через 30–60 мин, содержание его во внеклеточной среде достигает максимума через 3–4 ч. Синтез цитокинов конкретной клеткой продолжается довольно непродолжительное время — обычно немногим больше суток. Не весь синтезируемый материал секретируется. Некоторое количество цитокинов экспрессируется на поверхности клетки или содержится в цитоплазматических гранулах. Выброс гранул могут вызывать те же активирующие сигналы, что и продукция цитокинов. Это обеспечивает быстрое (в течение 20 мин) поступление цитокинов в очаг поражения.
Провоспалительные цитокины выполняют многие функции. Основная их роль — «организация» воспалительной реакции . Один из наиболее важных и ранних эффектов провоспалительных цитокинов — усиление экспрессии молекул адгезии на эндотелиальных клетках, а также на самих лейкоцитах, что приводит к миграции в очаг воспаления лейкоцитов из кровяного русла. Кроме того, цитокины индуцируют усиление кислородного метаболизма клеток, экспрессии ими рецепторов для цитокинов и других факторов воспаления, стимуляцию выработки цитокинов, бактерицидных пептидов и т.д. Провоспалительные цитокины оказывают преимущественно местное действие. Попадание избыточно секретируемых провоспалительных цитокинов в циркуляцию способствует проявлению системных эффектов воспаления, а также стимулирует выработку цитокинов клетками, отдаленными от очага воспаления. На системном уровне провоспалительные цитокины стимулируют продукцию белков острой фазы, вызывают повышение температуры тела, действуют на эндокринную и нервную системы, а в высоких дозах приводят к развитию патологических эффектов (плоть до шока, подобного септическому).
Семейство Интерлейкин 1
[править]Состав семейства ИЛ-1
IL-1 — собирательное обозначение семейства белков, включающего более 11 молекул. Функция большинства из них неизвестна, однако 5 молекул — IL-1α (по современной классификации — IL-1F1), IL-1β (IL-1F2), IL-1RA (IL-1F3), IL-18 (IL-1F4) и IL-33 (IL-1F11) — активные цитокины.
Особенности строения и активации членов семейства ИЛ-1
IL-1α и IL-1β традиционно называют IL-1, поскольку они взаимодействуют с одним и тем же рецептором и их эффекты неразличимы. Гены этих цитокинов локализованы в длинном плече хромосомы 2 человека. Гомология между ними на нуклеотидном уровне составляет 45%, на аминокислотном — 26%. Обе молекулы имеют β-складчатую структуру: они содержат 6 пар антипараллельных β-слоев и имеют форму трилистника. Клетки синтезируют молекулу-предшественник с молекулярной массой около 30 кДа, лишенную сигнальных пептидов, что свидетельствует о необычном пути процессинга молекулы IL-1. Молекулярная масса зрелых белков — около 18 кДа.
IL-1α существует в трех формах — внутриклеточной (растворимая молекула присутствует в цитозоле и выполняет регуляторные функции), мембранной (молекула доставляется на поверхность клетки за счет механизма, аналогичного рециклингу рецепторов и заякоривается в мембране) и секретиуремой (молекула секретируется в первоначальном виде, но подвергается процессингу — расщеплению внеклеточными протеазами с образованием активного цитокина массой 18 кДа). Основной вариант молекулы IL-1α у человека — мембранный. В такой форме действие цитокина более выражено, но проявляется только локально.
Процессинг IL-1β происходит внутри клетки с участием специализированного фермента — IL-1-конвертазы ( каспазы 1), находящегося в лизосомах. Активация этого фермента осуществляется в составе инфламмосомы — временной надмолекулярной структуры, включающей, кроме неактивной каспазы 1, внутриклеточные рецепторы семейства NLR — NOD1, NOD2, IPAF и др. Для активации каспазы 1 необходимо распознавание названными рецепторами PAMP, что вызывает развитие активационного сигнала. В результате происходит образование транскрипционного фактора NF-κB и индукция провоспалительных генов, а также активация инфламмосомы и содержащейся в ней каспазы 1. Активированный фермент расщепляет молекулу-предшественницу IL-1β, и образовавшийся зрелый цитокин с молекулярной массой 18 кДа секретируется клеткой.
IL-1α, IL-1β, а также рецепторный антагонист IL-1 имеют общие рецепторы, экспрессируемые спонтанно на многих типах клеток. При активации клеток на них возрастает число мембранных рецепторов для IL-1. Основной из них — IL-1RI — во внеклеточной части содержит 3 иммуноглобулиноподобных домена. Его внутриклеточная часть представляет TIR-домен, структурно сходный с аналогичными доменами TLR и запускающий те же сигнальные пути. Число этих рецепторов невелико (200–300 на клетку), но они обладают высоким сродством к IL-1 (Kd равен 10-11 М). Другой рецептор — IL-1RII — лишен сигнальной составляющей в цитоплазматической части, не передает сигнал и служит рецептором-ловушкой. В передаче сигнала от IL-1RI принимают участие те же факторы, что и для TLR (например, MyD88, IRAK и TRAF6), что приводит к аналогичным результатам — образованию транскрипционных факторов NF-κB и АР-1, вызывающих экспрессию одного и того же набора генов. Эти гены отвечают за синтез провоспалительных цитокинов, хемокинов, молекул адгезии, ферментов, обеспечивающих бактерицидность фагоцитов, и других генов, продукты которых участвуют в развитии воспалительной реакции. К продуктам, секрецию которых индуцируют IL-1, принадлежит и сам IL-1, т.е. в данном случае срабатывает петля положительной обратной связи.
Мишенями IL-1 потенциально могут быть любые клетки организма. В наибольшей степени его действие затрагивает эндотелиальные клетки, все виды лейкоцитов, клетки хрящевой и костной тканей, синовиальные и эпителиальные клетки, многие разновидности нервных клеток. Под влиянием IL-1 происходит индукция экспрессии больше 100 генов; с его участием реализуется больше 50 различных биологических реакций. Основные эффекты IL-1 вызывают эмиграцию лейкоцитов и активацию их фагоцитарной и бактерицидной активности. Они влияют также на свертывающую систему и сосудистый тонус, определяя особенности гемодинамики в очаге воспаления. IL-1 оказывает многоплановое действие на клетки не только врожденного, но и адаптивного иммунитета, обычно стимулируя проявления и того, и другого.
IL-1 обладает множеством системных эффектов:
- Обеспечение развития и протекания местной воспалительной реакции и ответа острой фазы воспаления на уровне всего организма. При этом IL-1 стимулирует развитие целого комплекса защитных реакций, направленных на ограничение распространения инфекции, элиминацию внедрившихся микроорганизмов и восстановление целостности поврежденных тканей.
- Начало продукции IL-1 в зоне первичного контакта клеток-продуцентов с микроорганизмами - в области повреждения (местно), в ткани регионарных лимфоузлов и других лимфоидных образований обеспечивает активацию местных защитных реакций в воспалительном очаге. Далее за счет конститутивной экспрессии своих рецепторов IL-1 очень быстро активирует практически все типы клеток, участвующих в формировании воспалительной реакции, включая фибробласты, эндотелиоциты, резидентные макрофаги и все типы лейкоцитов крови
- В регуляции острофазового ответа принимают участие многие цитокины, особенно IL-1, TNFα и IL-6, а также другие биологически активные вещества. Однако только IL-1 за счет избирательных эффектов, вызывает увеличение экспрессии генов одних белков в клетках ткани печени и подавление экспрессии генов других белков. При тяжелой патологии это необходимо для сохранения пластических и энергетических ресурсов организма.
- Регуляция функций эндотелия и системы свертывания крови – важнейший компонент системных эффектов IL-1. При сепсисе и септическом шоке это индуцирует запуск прокоагуляционных систем крови, а также интенсивный синтез эндотелиоцитами множества других «прововоспалительных» цитокинов и экспрессию эндотелием молекул, обеспечивающих прикрепление нейтрофилов и лимфоцитов к стенкам сосудов.
- Выраженный пирогенный эффект также является важнейшим системным эффектом IL-1. В течение многих лет именно эта функция считалась главной для данного цитокина. IL-1 способен воздействовать на нейроны особой зоны переднего гипоталамуса в области терморегуляторного центра. Кроме того, IL-1 вовлечен в нейрогуморальные связи гипофизарно-гипоталамического узла, и именно IL-1 повышает уровень адренокортикотропного гормона и кортикостерона в плазме крови, а также увеличивает синтез ряда нейромедиаторов.
- Стимуляция адаптивного звена иммунитета. Так, IL-1 увеличивает функциональную активность Т- и В-лимфоцитов, инфильтрирующих ткани и находящихся в регионарных лимфоидных образованиях. Проникновение IL-1 в лимфатические узлы, а далее и в центральные органы иммунной системы способно вызывать изменения дифференцировки и функциональной активности лимфоцитов. В экспериментальных условиях введение IL-1 приводит к стимуляции дифференцировки предшественников Т-лимфоцитов в костном мозге, усилению пролиферации изолированных лимфоцитов тимуса и селезенки, усилению продукции ими IL-2 и увеличению среди спленоцитов доли клеток с фенотипом Т-хелперов.
- Усиление пролиферации Т-лимфоцитов, антигензависимой активации В-лимфоцитов, а также стимулирование активности NK-клеток, нейтрофилов и макрофагов, активация продукции острофазовых белков, участие в индукции синтеза простагландинов, ряда гормонов и нейромедиаторов – важные варианты влияния IL-1 на иммунореактивность. Не менее важно также регуляторное воздействие IL-1 на эндотелиоциты, фибробласты, другие клетки и ткани организма.
- Важнейшее свойство IL-1 — это его способность стимулировать пролиферацию преактивированных антигеном зрелых Т-лимфоцитов. Причем IL-1 может усиливать пролиферацию обоих типов Т-хелперных клонов. Однако сам по себе IL-1 не является ростовым фактором Т-лимфоцитов и не способен поддерживать длительную пролиферацию Т-клеток в культуре. Его действие заключается в индукции специфических ростовых факторов, в первую очередь IL-2 и IL-4, и усилении экспрессии клетками рецепторов этих цитокинов.
- IL-1 способен активировать синтез целого ряда других цитокинов, прежде всего IL-2, IL-3, IL-4, IL-6, IL-8, TNFα, TNFβ, IFNγ. Кроме того, IL-1 может индуцировать собственный синтез и экспрессию рецепторов для IL-2. Многие эффекты в процессе воспалительной реакции, такие как индукция лихорадки, стимуляция гемопоэза, участие в неспецифической противоинфекционной защите IL-1 как цитокин реализует в синергизме с TNFα и IL-6.
- IL-1 активен по отношению к нейтрофильным гранулоцитам. IL-1 активирует важнейшие функции нейтрофилов и является праймирующим фактором для данного типа клеток, то есть обладает способностью усиливать их реакцию в ответ на стимуляцию. Кроме стимуляции выхода нейтрофилов в очаг воспаления, IL-1 усиливает их адгезию, агрегацию, хемотаксис, фагоцитоз и продукцию свободных форм кислорода. Воздействие IL-1 на нейтрофилы может быть как прямым, так и опосредованным — путем индукции синтеза макрофагами, эндотелиальными клетками и фибробластами других регуляторных цитокинов.
- Гемостимулирующий эффект IL-1 обусловлен индукцией выработки нескольких эндогенных колониестимулирующих факторов и синергичным с ними усилением пролиферации и дифференцировки клеток различных ростков кроветворения. IL-1 действует на кроветворные клетки на разных этапах их созревания, включая стадию полипотентных стволовых клеток. Поэтому применение IL-1 приводит к возрастанию не только количества гранулоцитов, но также тромбоцитов и лимфоцитов. IL-1 действует на широкий круг клеток-предшественников, что позволяет ему более эффективно восстанавливать нормальное кроветворение, а не действовать узко направленно по отношению только к гранулоцитам. В этой связи особенно важна стимуляция IL-1 мегакариоцитарного ростка кроветворения и быстрое увеличение числа зрелых тромбоцитов.
- Стимулирующее влияние IL-1 на метаболизм соединительной ткани – еще один важный компонент биологической активности IL-1. В частности, IL-1 стимулирует пролиферацию фибробластов и выработку ими простагландинов, ростовых факторов и ряда цитокинов, таких как колониестимулирующие факторы, интерлейкины и интерфероны. В клетках соединительной ткани увеличивается также синтез коллагена и, одновременно, коллагеназы, а также ряда других ферментов.
- IL-1 системно регулирует процесс остеогенеза. Так, IL-1 активирует костномозговую продукцию остеокластов и их функциональную активность, в частности стимулируются процессы остеокластической резорбции. С другой стороны, IL-1 способен стимулировать пролиферацию остеобластов и их дифференцировку в остеоциты, а возможно и изменять уровень продукции гликозоаминогликанов. IL-1 активно вмешивается в регуляцию состояния костной ткани, воздействуя на различные ее клеточные системы, такие как остеокласты и остеобласты.
Он стимулирует выработку гепатоцитами белков острой фазы, при действии на центр терморегуляции гипоталамуса вызывает развитие лихорадки, участвует в развитии системных проявлений воспалительного процесса (например, в недомогании, снижении аппетита, сонливости, адинамии), что связано с действием IL-1 на ЦНС. Усиливая экспрессию рецепторов для колониестимулирующих факторов, IL-1 способствует усилению гемопоэза, с чем связано его радиозащитное действие. IL-1 стимулирует выход из костного мозга лейкоцитов, в первую очередь нейтрофилов, в том числе незрелых, что приводит к появлению при воспалении лейкоцитоза и сдвигу лейкоцитарной формулы влево (накопление незрелых форм клеток). Эффекты IL-1 влияют на вегетативные функции и даже на высшую нервную деятельность (изменение поведенческих реакций и т.д.). Мишенями IL-1 могут быть также хондроциты и остеоциты, с чем связана способность IL-1 вызывать разрушение хряща и кости при их вовлечении в воспалительный процесс и наоборот, гиперплазия патологических тканей (паннус при ревматоидном артрите). Повреждающее действие IL-1 проявляется и при септическом шоке, повреждении суставов при ревматоидном артрите и ряде других патологических процессов.
Дублирование IL-1 эффектов бактериальных продуктов связано с потребностью в многократном воспроизведении активирующего эффекта патогенов без их диссеминации. Микроорганизмы стимулируют только клетки, находящиеся в непосредственной близости от места проникновения, прежде всего локальные макрофаги. Затем тот же эффект многократно воспроизводится молекулами IL-1β. Выполнение IL-1 указанной функции облегчается экспрессией их рецепторов почти всеми клетками организма при активации (происходит прежде всего в очаге воспаления).
Таким образом, можно утверждать, что интерлейкин-1 (IL-1) является одним из ключевых медиаторов защитных реакций организма, который регулирует процессы пролиферации, дифференцировки и функциональной активности клеток иммунной и гемопоэтической систем.
Рецепторный антагонист IL-1 (IL-1RA) гомологичен IL-1α и IL-1β (гомология составляет соответственно 26% и 19%). Он взаимодействует с рецепторами IL-1, но не способен передавать в клетку сигнал. В результате IL-1RA выступает в роле специфического антагониста IL-1. IL-1RA секретируют те же клетки, что и IL-1, этот процесс не требует участия каспазы 1. Выработку IL-1RA индуцируют те же факторы, что и синтез IL-1, однако некоторое его количество спонтанно продуцируют макрофаги и гепатоциты. В результате этот фактор постоянно присутствует в сыворотке крови. Вероятно, это необходимо для предотвращения негативных последствий системного действия IL-1, вырабатываемого в значительных количествах при остром воспалении. В настоящее время проводят испытания рекомбинантного IL-1RA в качестве лекарственного препарата при лечении хронических воспалительных заболеваний (ревматоидный артрит и т.д.)
IL-18 или фактор индукции у-интерферона— провоспалительный цитокин, родственный IL-1β: он также синтезируется в виде предшественника, конвертируемого с участием каспазы 1; взаимодействует с рецептором, цитоплазматическая часть которого содержит домен TIR и передает сигнал, приводящий к активации NF-κB. В результате происходит активация всех провоспалительных генов, однако она выражена слабее, чем при действии IL-1. Синтезируется макрофагами. Отдельное свойство IL-18 — индукция (особенно в сочетании с IL-12) синтеза клетками IFNγ. В отсутствие IL-12 IL-18 индуцирует синтез антагониста IFNγ — IL-4 и способствует развитию аллергических реакций. Действие IL-18 ограничивает растворимый антагонист, связывающий его в жидкой фазе.
Клетки-продуценты - активированные макрофаги и прежде купферовськи и дендритные клетки, в частности незрелые кератиноциты, Т-и В-лимфоциты. Моноциты и макрофаги продуцируют много различных видов ИЛ-18, многие из которых являются неактивными димера. ИЛ-18 типа 2 является фрагментом ИЛ-18, имеет незначительную способность индуцировать интерферон, в крови связывается с IgM и в значительной концентрации обнаруживается в 30% людей. ИЛ-18 экспрессируется на многих клетках - моноцитах, макрофагах, Т-и В-лимфоцитах, дендритных и эндотелиальных клетках, кератиноцитах, астроцитах, клетках микроглии. Его экспрессия возникает при активации фактора NFkB. Рецептор ИЛ-18 принадлежит к семейству Ig-подобных рецепторов. Основные клетки-мишени - Т-лимфоциты, НК.
ИЛ-18 относится к провоспалительных цитокинов и имеет широкий спектр биологической активности.
- Он индуцирует образование у-интерферона, регулирует рост и дифференцировку Тх1, развитие иммунного ответа по Tx1-типом, активирует НК, является частью комплекса, который вызывает апоптоз клеток.
- Он индуцирует выработку ИФН-в В-лимфоцитами, что приводит к торможению секреции IgE, увеличивает синтез интерферона в Т-лимфоцитами, а вместе с ИЛ-12 - НК, стимулирует продуцирование многих цитокинов - ФНО-а, ИЛ-ß, ИЛ-8, МИР-а, ИЛ-5, ИЛ-6, ГМ-КСФ, Г-КСФ. При отсутствии ИЛ-12 он вместе с ИЛ-2 и ИЛ-3 индуцирует выработку ИЛ-4, что способствует развитию иммунного ответа при Тх2-типом и формирования аллергических реакций.
- ИЛ-18 может обнаруживать нейромодуляторный активность, активно участвует в формировании защитных реакций против различных патогенов благодаря продуцированию ИФН-у, особенно против внутриклеточных патогенов (листерий, шигелл сальмонелл, микобактерий), а также обладает противоопухолевой активностью, обусловленную индукцией апоптоза вследствие усиления взаимодействия Fas / FasL через стимуляцию ИЛ-18 продуцирования мРНК Fas L.
- Введение гена ИЛ-18 в опухолевые клетки мышей тормозит их пролиферацию.
- Он способен отменять у мышей развитие хронической болезни «трансплантат против хозяина», поддерживать воспалительный процесс вследствие стимуляции синтеза у-интерферона, ФНО-а, ИЛ-Щ ИЛ-8, Мира.
- Вместе (но не отдельно) с ИЛ-12 он приводит токсические эффекты через зависимые и независимые от у-интерферона механизмы; нейтрализация ИЛ-18 при летальной эндотоксемии защищает мышей от летального исхода. По гиперпродукування ИЛ-18 возникают деструктивные воспалительные процессы, в частности аутоиммунные заболевания Т-клеточного типа.
IL-33 структурно очень близок IL-18. Процессинг IL-33 тоже происходит с участием каспазы 1. Однако этот цитокин отличается от других представителей семейства IL-1 выполняемыми функциями. Своеобразие действия IL-33 значительной степени обусловлено тем, что его рецептор экспрессируется избирательно на Th2-клетках. В связи с этим IL-33 способствует секреции Th2-цитокинов IL-4, IL-5, IL-13 и развитию аллергических процессов. Он не оказывает существенного провоспалительного действия.
В отличие от IL- 1β и IL-18 , которые находятся в цитозоле и выражены по патогенной стимуляции, IL -33 и IL- 1α, конститутивно экспрессируют и хранится в ядре клеток. Они немедленно освобождаютя в межклеточное пространство после повреждения клеток, когда клетки подвергаются некрозу. IL- 33 можно найти в супернатанте клеток после физической травмы, когда нарушается плазматическая мембрана, и когда теряется целостность клеток.
Суперсемейство TNF
[править]Фактор некроза опухоли α (ФНОαα или TNFα) — представитель другого семейства иммунологически значимых белков. Это провоспалительный цитокин с широким спектром активности. TNFα имеет β-складчатую структуру. Он синтезируется в виде функционально активной мембранной молекулы про-TNFα с молекулярной массой 27 кДа, представляющей трансмембранный белок II типа (т.е. его N-концевая часть направлена внутрь клетки). В результате протеолиза во внеклеточном домене формируется растворимый мономер с молекулярной массой 17 кДа. Мономеры TNFα спонтанно формируют тример с молекулярной массой 52 кДа, представляющий основную форму этого цитокина. Тример имеет колоколовидную форму, причем субъединицы соединяются своими С-концами, содержащими по 3 участка связывания с рецептором, тогда как N-концы друг с другом не связаны и не участвуют во взаимодействии с рецепторами (а следовательно, и в выполнении цитокином своих функций). При кислых значениях рН TNFα приобретает α-спиральную структуру, что обусловливает изменение некоторых его функций, в частности, усиление цитотоксичности. TNF — прототипический член большого семейства молекул суперсемейства TNF . К нему относят лимфотоксины α и β (в растворимой форме существует только первый), а также многие мембранные молекулы, участвующие в межклеточных взаимодействиях (CD154, FasL, BAFF, OX40-L, TRAIL, APRIL, LIGHT), которые будут упоминаться далее в различных контекстах. Согласно современной номенклатуре, название членов суперсемейства состоит из сокращения TNFSF и порядкового номера (для TNFα — TNFSF2, для лимфотоксина α — TNFSF1).
| Фактор (лиганд) | Хромосома | Молекулярная масса, кДа | Рецептор |
|---|---|---|---|
| TNFα (TNFSF2) | 6р | 17; тример — 52; гликозилированная форма — 25,6 | TNF-R1, TNF-R2 (TNFRSF1, TNFRSF2) |
| Лимфотоксинα (TNFSF1) | 6р | 22,3 | TNF-R1, TNF-R2 |
| Лимфотоксин β (TNFSF3) | 6р | 25,4 | LTβ-R (TNFRSF3) |
| OX-40L (TNFSF4) | 1q | 34,0 | OX-40 (TNFRSF4; CD134) |
| CD40L (TNFSF5; CD154) | ТXp | 39,0 | CD40 (TNFRSF5) |
| FasL (TNFSF6; CD178) | 1q | 31,5 | Fas/APO-1 (CD95) (TNFRSF6) |
| CD27L (TNFSF7, CD70) | Т19p | 50,0 | CD27 (TNFRSF7) |
| CD30L (TNFSF8) | 9q | 40,0 | CD30 (TNFRSF8) |
| 4-1BBL (TNFSF9) | 19p | 27,5 | 4-1BB (TNFRSF9; CD137) |
| TR AIL (TNFSF10) | 3q | 32,0 | ВК4б ВК5 |
| APRIL (TNFSF13) | 17p | 27,0 | BCMA, TACI |
| LIGHT (TNFSF14) | 16q | 26,0 | HVEM (TNFRSF14) |
| GITRL (TNFSF18) | 1p | 22,7 | GITR (TNFRSF18) |
| BAFF (TNFSF20) | 13 | 31,2 | BAFFR, TACI, BCMA |
Основные продуценты TNFα, как и IL-1, — моноциты и макрофаги. Его секретируют также нейтрофилы, эндотелиальные и эпителиальные клетки, эозинофилы, тучные клетки, В- и Т-лимфоциты при их вовлечении в воспалительный процесс. TNFα выявляют в кровотоке раньше других провоспалительных цитокинов — уже через 20–30 мин после индукции воспаления, что связано со «сбрасыванием» клетками мембранной формы молекулы, а возможно также с выбросом TNFα в составе содержимого гранул.
Есть 2 типа рецепторов TNF, общие для TNFα и лимфотоксина α — TNFRI (от tumor necrosis factor receptor I ) и TNFRII с молекулярной массой соответственно 55 и 75 кДа. TNFRI присутствует практически на всех клетках организма, кроме эритроцитов, а TNFRII — преимущественно на клетках иммунной системы. TNFR образуют большое семейство, в которое входят молекулы, участвующие во взаимодействии клеток и индукции клеточной гибели — апоптоза. Сродство TNFα к TNFRI ниже, чем к TNFRII (соответственно около 5×10-10 М и 55×10-11 М. При связывании TNFα-тримера происходит необходимая для передачи сигнала тримеризация его рецепторов.
Особенности передачи сигнала от этих рецепторов во многом определяются структурой их внутриклеточной части. Цитоплазматическая часть TNFRI представлена так называемым доменом смерти, от которого поступают сигналы, приводящие к включению механизма апоптоза; TNFRII лишен домена смерти. Передача сигнала от TNFRI происходит с участием адапторных белков TRADD (TNFR-associated death domain) и FADD (Fas-associated death domain), тоже содержащих домены смерти. Помимо пути, приводящего к развитию апоптоза (через активацию каспазы 8 или синтез церамида), выделяют еще несколько сигнальных путей, включаемых с участием факторов TRAF2/5 и RIP-1. Первый из названных факторов передает сигнал по пути, приводящему к активации фактора NF-κB, т.е. по классическому пути индукции провоспалительных генов. Сигнальный путь, активируемый фактором RIP-1, приводит к активации MAP-каскада с конечным продуктом — транскрипционным фактором АР-1. Этот фактор включает гены, обеспечивающие активацию клетки и предотвращающие развитие апоптоза. Судьбу клетки, таким образом, определяет баланс про- и антиапоптотических механизмов, запускаемых при связывании TNFα с TNFRI.
Реализация функций TNFα связана преимущественно с действием через TNFRI — выключение соответствующего гена приводит к развитию тяжелого иммунодефицита, тогда как последствия инактивации гена TNFRII незначительны. На пике воспалительной реакции рецепторы ФНОα могут «сбрасываться» с мембраны и выходить в межклеточное пространство, где они связывают ФНОα, оказывая противовоспалительное действие. В связи с этим растворимые формы TNFR используют при лечении хронических воспалительных заболеваний. При этом оказалось, что препарат на основе растворимого TNFRII оказался клинически наиболее эффективным.
Как и IL-1, TNFα усиливает экспрессию молекул адгезии, синтез провоспалительных цитокинов и хемокинов, белков острой фазы, ферментов фагоцитарных клеток и т.д. Наряду с IL-1, TNFα участвует в формировании всех основных местных, а также некоторых системных проявлений воспаления. Он активирует эндотелиальные клетки, стимулирует ангиогенез, усиливает миграцию и активирует лейкоциты. TNFα в большей степени, чем IL-1, влияет на активацию и пролиферацию лимфоцитов. В комбинации с IFNγ TNFα индуцирует активность NO-синтазы фагоцитов, что значительно усиливает их бактерицидный потенциал. TNFα стимулирует пролиферацию фибробластов, способствуя заживлению ран. При повышенной локальной выработке TNFα преобладают процессы повреждения тканей, проявляющиеся развитием геморрагического некроза. Помимо этого TNFα подавляет активность липопротеиновой липазы, что ослабляет липогенез и приводит к развитию кахексии (одно из первоначальных названий TNFα — кахексин). Повышенное высвобождение TNFα и его накопление в циркуляции, например при действии высоких доз бактериальных суперантигенов, вызывает развитие тяжелой патологии — септического шока. Таким образом, действие TNFα, направленное на выполнение защитной функции и поддержание гомеостаза, может сопровождаться тяжелыми токсическими эффектами (местными и системными), нередко служащими причиной смерти.
Семейство интерлейкина-6
[править]
Состав семейства интерлейкина- 6
ИЛ-6, ИЛ-11, ИЛ-31, Онкостатин-М, Кардиотропин-1, Leukemia inhibitory factor(LIF) , Ciliary neurotrophic factor (CNTF).
IL-6 — провоспалительный цитокин широкого действия. Он также служит прототипическим фактором семейства цитокинов, включающего, кроме собственно IL-6, онкостатин М (OSM), лейкемия-ингибирующий фактор (LIF), цилиарный нейротрофический фактор (CNTF), кардиотропин-1 (CT-1), а также IL-11 и IL-31.
Молекулярная масса IL-6 — 21 кДа. IL-6 вырабатывают моноциты и макрофаги, эндотелиальные, эпителиальные, глиальные, гладкомышечные клетки, фибробласты, Т-лимфоциты типа Th2, а также многие опухолевые клетки. Выработка IL-6 миелоидными клетками индуцируется при взаимодействии их TLR с микроорганизмами и их продуктами, а также под влиянием IL-1 и TNFα. При этом в течение 2 ч содержание IL-6 в плазме крови возрастает в 1000 раз.
Рецепторы всех факторов семейства IL-6 содержат общий компонент — цепь gp130, присутствующую практически на всех клетках организма. Второй компонент рецептора индивидуален для каждого цитокина. Специфическая цепь рецептора IL-6 (gp80) отвечает за связывание этого цитокина, тогда как gp130 участвует в передаче сигнала, поскольку связана с тирозинкиназами Jak1 и Jak2. При взаимодействии IL-6 с рецептором запускается следующая последовательность событий: IL-6-мономер взаимодействует с цепью gp80, происходит димеризация комплексов (2 молекулы цитокина — 2 цепи gp80), после чего к комплексу присоединяется 2 цепи gр130, что приводит к фосфорилированию Jak-киназ. Последние фосфорилируют факторы STAT1 и STAT3, которые димеризуются, перемещаются в ядро и связывают промоторы генов-мишеней. Цепь gp80 легко «смывается» с клетки; в свободной форме она взаимодействует с цитокином, инактивируя его, т.е. выступает в качестве специфического ингибитора IL-6.
L-6 участвует в индукции практически всего комплекса местных проявлений воспаления. Он влияет на миграцию фагоцитов, усиливая выработку СС-хемокинов, привлекающих моноциты и лимфоциты, и ослабляя продукцию СХС-хемокинов, привлекающих нейтрофилы. Провоспалительные эффекты IL-6 выражены слабее, чем у IL-1 и TNFα, в противоположность которым он не усиливает, а угнетает выработку провоспалительных цитокинов (IL-1, TNFα и IL-6) и хемокинов клетками, вовлеченными в воспалительный процесс. Таким образом, IL-6 сочетает свойства про- и противовоспалительных цитокинов и участвует не только в развитии, но и в ограничении воспалительной реакции.
IL-6 — основной фактор, индуцирующий в гепатоцитах экспрессию генов белков острой фазы. IL-6 влияет на различные этапы гемопоэза, в том числе на пролиферацию и дифференцировку стволовых клеток. Он служит ростовым фактором незрелых плазматических клеток, существенно усиливая гуморальный иммунный ответ. IL-6 влияет также на Т-лимфоциты, повышая активность цитотоксических Т-клеток.
Семейство интерлейкина 17
[править]IL-17 и связанные с ним цитокины. Группа цитокинов, включающая разновидности IL-17, привлекла всеобщее внимание в связи с открытием особой разновидности Т-хелперов — Th17, участвующей в развитии некоторых повреждающих форм воспалительных реакций, в частности, при аутоиммунных процессах. Роль этих цитокинов в реакциях адаптивного иммунного ответа будет рассмотрена далее. Здесь приведем только общую характеристику цитокинов и кратко рассмотрим их роль в реакциях врожденного иммунитета.
Семейство IL-17 включает 6 белков, обозначаемых буквами от А до F. Свойствами провоспалительных цитокинов из них обладают IL-17A и IL-17F. Они представляют собой гомодимеры, скрепленные дисульфидной связью; их молекулярная масса — 17,5 кДа. Эти цитокины продуцируются упомянутыми Th17, а также CD8+ Т-клетками, эозинофилами, нейтрофилами. IL-23 стимулирует развитие Тh17-клеток и выработку IL-17.
Рецепторы для IL-17 экспрессируются многоми клетками — эпителиальными, фибробластами, клетками иммунной системы, в частности, нейтрофилами. Основной результат взаимодействия IL-17 с рецептором состоит, как и при действии других провоспалительных цитокинов, в индукции фактора NF-κB и экспрессии многочисленных NF-κB-зависимых генов воспаления.
Один из важных биологических эффектов IL-17 (наряду с IL-23) — поддержание гомеостаза нейтрофилов. Эти цитокины усиливают образование нейтрофилов, стимулируя выработку G-CSF. При этом усиление или ослабление выработки IL-17 и IL-23 регулируется численностью нейтрофилов в периферических тканях: снижение числа этих клеток в результате апоптоза приводит к усилению выработки цитокинов.
Провоспалительное действие IL-17 реализуется главным образом через усиление выработки других цитокинов (IL-8, IL-6, γ-CSF, ряд хемокинов) и экспрессии молекул адгезии. У мышей, трансгенных по IL-17 или по IL-23, развивается системное хроническое воспаление, имеющее интерстициальный характер, с инфильтрацией нейтрофилами, эозинофилами, макрофагами и лимфоцитами различных органов. За этими цитокинами признают ведущую роль в развитии хронических аутоиммунных заболеваний.
Семейство IL-12
[править]-
Кристаллическая структура человеческого интерлейкина 12
-
Кристаллическая структура человеческого интерлейкина 12Б
IL-12 был идентифицирован по способности активировать NK-клетки, вызывать пролиферацию Т-лимфоцитов и индуцировать синтез IFNγ. IL-12 занимает особое место в ряду цитокинов, вырабатываемых клетками системы врожденного иммунитета, поскольку он (как и его главные продуценты —дендритные клетки) служит связующим звеном между врожденным и адаптивным иммунитетом. С другой стороны, IL-12 входит в тандем IL-12–IFNγ, которому принадлежит ключевая роль в осуществлении иммунной защиты от внутриклеточных патогенов.
IL-12 представляет димер, состоящий из субъединиц р40 и р35. Его суммарная молекулярная масса — 75 кДа. Функциональная активность IL-12 связана с его субъединицей р40. «Полномасштабный» IL-12 секретируют активированные моноциты, макрофаги, миелоидные дендритные клетки, нейтрофилы, эпителиальные клетки барьерных тканей (они продуцируют и IL-12р35 и IL-12p40 субъединицы цитокина). Большинство же клеток организма синтезирует только функционально неактивную субъединицу IL-12р35. Количество гетеродимера IL-12, секретируемого клеткой, ограничено субъединицей р35. IL-12p40 синтезируется в избытке и может димеризоваться с образованием гомодимера, выступающего в качестве антагониста IL-12, а также хемоаттрактанта. Индукторы выработки IL-12 — прежде всего патогены, распознаваемые TLR и другими паттернраспознающими рецепторами. Выработку IL-12 усиливают IL-1, IFNγ, а также межклеточные взаимодействия, опосредованные CD40-CD154 и другими парами молекул семейств — TNFR.
Рецептор IL-12 сильнее всего экспрессирован на NK-клетках, активированных Th1-клетках и цитотоксических Т-лимфоцитах и в меньшей степени — на дендритных клетках. Экспрессия рецептора IL-12 активированными Т-клетками усиливается под влиянием IL-12, IFNγ, IFNα, TNFα и при костимуляции через рецептор CD28. Рецептор для IL-12 представляет димер, образованный субъединицами IL-12Rβ1 (100 кДа), и IL-12Rβ2 (130 кДа, CD212), с которым ассоциирован белок с молекулярной массой 85 кДа. В связывании IL-12 участвуют и β1 и β2 цепи, тогда как в передаче сигнала задействована преимущественно субъединица IL-12Rβ2. Внутриклеточный домен β1-цепи ассоциирован с киназой JAK2, внутриклеточный домен β2-цепи — с киназой Tyk2. Киназы фосфорилируют транскрипционные факторы STAT1, STAT3, STAT4 и STAT5.
Главная функция IL-12, обусловленная его способностью стимулировать цитотоксические лимфоциты (NK и T) и индуцировать дифферен-цировку Th1-клеток, — запуск клеточных механизмов защиты от внутриклеточных патогенов. IL-12 действует на NK- и NKT-клетки уже на ранних стадиях иммунных процессов, усиливая пролиферацию и цитотоксическую активность NK-клеток, а позже — цитотокси-ческих Т-лимфоцитов и синтез всеми этими клетками IFNγ. Несколько позже IL-12 индуцирует дифференцировку Th1-клеток, тоже продуцирующих IFNγ. Условие индукции Th1-клеток — предварительная экспрессия активированными CD4+ Т-клетками субъединицы рецептора IL-12Rβ2. После этого клетки приобретают способность связывать IL-12, что приводит к активации фактора STAT4, регулирующего экспрессию генов, характерных для Th1-клеток (для экспрессии гена IFNG более важно действие транскрипицонного фактора T-bet). Одновременно IL-12 подавляет дифференцировку Th2-клеток и ослабляет выработку клетками В-ряда антител классов IgE и IgA. Действуя на дендритные и другие АПК IL-12 индуцирует экспрессию костимулирующих молекул (CD80/86, и др.), а также продуктов МНС-II АПК. Таким образом, IL-12 играет связующую роль между врожденным и адаптивным иммунитетом и усиливает иммунные механизмы, ответственные за защиту от внутриклеточных патогенов и опухолей.
К семейству IL-12 относят IL-23, IL-27 и IL-35. Эти цитокины представляют гетеродимеры: IL-23 образован двумя субъединицами — IL-23р19 и IL-12p40 (идентична соответствующей субъединице IL-12), IL-27 — субъединицами Ebi3 и IL-27p28, IL-35 — субъединицами Ebi3 и IL-12p35. Эти цитокины продуцируются преимущественно дендритными клетками. Выработку цитокинов семейства IL-12 запускают представленные на патогенах PAMP и цитокины, в особенности GM-CSF.
Рецепция IL-23 осуществляется двумя разными структурами: субъединицу IL-12p40 распознает β1-цепь рецептора для IL-12, а субъединицу IL-23р19 — особый рецептор — IL-23R. Основную роль в передаче сигнала от IL-23 играет STAT4. Рецептор для IL-27 активирует молекулы WSX-1 (гомолог β2-субъединицы IL-12R) и gp130 (полипептидная цепь, входящая
в состав рецепторов для цитокинов семейства IL-6).
Подобно IL-12, IL-23 и IL-27 действуют преимущественно на CD4+ Т-клетки, способствуя их дифференцировке по Th1-пути. Особенности IL-23 — преимущественное действие на Т-клетки памяти, а также способность поддерживать развитие Т-хелперов типа Th17. IL-27 отличается от двух других цитокинов семейства способностью вызывать пролиферацию не только активированных, но и покоящихся CD4+ Т-клеток. Недавно было показано, что IL-27 и IL-35 могут выступать в качестве регуляторных (супрессорных) факторов, поскольку их субъединица Ebi3 — мишень ключевого фактора регуляторных Т-клеток FOXP3.
Колониестимулирующие факторы (CSF) или гемопоэтины представлены тремя цитокинами — GM-CSF, G-CSF и M-CSF. К ним функционально близок IL-3 (Multi-CSF). Эти факторы называют колониестимулирующими, поскольку впервые были идентифицированы по способности поддерживать рост in vitro колоний гемопоэтических клеток соответствующего состава. IL-3 обладает наиболее широким спектром действия, поскольку поддерживает рост любых колоний гемопоэтических клеток, кроме лимфоидных. GM-CSF поддерживает рост как смешанных гранулоцитарно-моноцитарных колоний, так и отдельно колоний гранулоцитов и моноцитов/макрофагов. G-CSF и M-CSF специализируются на поддержании роста и дифференцировки соответствующих колоний. Эти факторы не только обеспечивают выживаемость и пролиферацию кроветворных клеток указанных типов, но и способны активировать уже зрелые дифференцированные клетки (M-CSF — макрофаги, G-CSF — нейтрофилы). M-CSF участвует в дифференцировке моноцитов в макрофаги и подавляет дифференцировку моноцитов в дендритные клетки. G-CSF, помимо действия на гранулоцитарный ветвь гемопоэза, вызывает мобилизацию кроветворных стволовых клеток из костного мозга в кровоток.
G-CSF, GM-CSF и IL-3 структурно характеризуются как гемопоэтины, содержащие 4 α-спиральных домена. Их рецепторы содержат по 2 полипептидные цепи, их относят к семейству гемопоэтиновых рецепторов. M-CSF отличается от остальных CSF. Он представляет собой димерную молекулу и существует как в растворимой, так и в мембраносвязанной формах. Его рецептор имеет внеклеточные Ig-подобные домены и внутриклеточный домен, обладающий активностью тирозинкиназы (наименование этой киназы-протоонкогена — с-Fms — иногда переносят на весь рецептор). При связывании М-CSF с рецепторами происходит их димеризация и активация киназы.
Колониестимулирующие факторы продуцируются эндотелиальными клетками и фибробластами а также моноцитами/макрофагами. GM-CSF и IL-3, кроме того, синтезируются Т-лимфоцитами. Под влиянием бактериальных продуктов (через паттернраспознающие рецеторы) и провоспалительных цитокинов синтез и секреция колониестимулирующих факторов значительно возрастает, что приводит к усилению миелопоэза. Особенно сильно стимулируется гранулоцитопоэз, что сопровождается ускоренной эмиграцией клеток, в том числе незрелых, на периферию. Это создает картину нейтрофильного лейкоцитоза со сдвигом формулы вправо, весьма характерным для воспаления. Препараты на основе GM- и G-CSF применяют в клинической практике для стимуляции гранулоцитопоэза, ослабленного цитотоксическими воздействиями (облучение, прием химиопрепаратов при лечении опухолевых заболеваний и т.д.). G-CSF применяют для мобилизации стволовых кроветворных клеток с последующим использованием индуцированной лейкомассы для восстановления нарушенного гемопоэза.
Фактор стволовых клеток (SCF— stem cell factor, c-kit ligand) cекретируют клетки стромы костного мозга (фибробласты, эндотелиальные клетки), а также разные типы клеток в период эмбрионального развития. SCF существует в виде трансмембранной и растворимой молекул (последняя образуется в результате протеолитического отщепления внеклеточной части). SCF выявляют в плазме крови. Его молекула имеет две дисульфидные связи. Рецептор SCF — с-Кit — обладает тирозинкиназной активностью и по своей структуре близок к Flt-3 и c-Fms (рецептор M-CSF). При связывании SCF происходят димеризация рецепторов и их фосфорилирование. Передача сигнала происходит с участием PI3
K и MAP-каскада.
Мутации гена SCF и его рецептора описаны давно (мутации steel); у мышей они проявляются изменением окраски шерсти и нарушением гемопоэза. Мутации, нарушающие синтез мембранной формы фактора, вызывают грубые дефекты развития эмбриона. Совместно с другими факторами
SCF участвует в поддержании жизнеспособности стволовых кроветворных клеток, обеспечивает их пролиферацию, поддерживает ранние этапы гемопоэза. SCF особенно важен для эритропоэза и развития тучных клеток, а также служит ростовым фактором для тимоцитов на стадиях DN1 и DN2.
По структуре и биологической активности сходными с SCF свойствами обладает фактор Flt-3L-(Fms-like thyrosinkinase 3-ligand), в сочетании с другими факторами поддерживающий ранние этапы миелопоэза и развитие В-лифмоцитов. SCF играет роль фактора роста лейкозных миелобластов.
Хемокины, представляющие важный гуморальный фактор воспаления и врожденного иммунитета, рассмотрены выше при описании хемотаксиса
лейкоцитов.
Интерфероны образуют автономную группу цитокинов. Общее свойство интерферонов — наличие у них противовирусной активности. В то же время, подобно другим цитокинам, они участвуют в регуляции иммунных процессов. Сочетание этих свойств делает интерфероны важными факторами врожденного (а в случае IFNγ еще и адаптивного) иммунитета и служит основанием для широкого применения интерферонов в качестве лечебных
препаратов.
Интерфероны были открыты в 1957 г А. Исааксом (A. Isaacs) и Дж. Линдеманном (J. Lindemann) как гуморальные факторы, опосредующие
интерференцию вирусов — индуцируемую вирусами неспецифическую резистентность, распространяющуюся не только на вирус-индуктор, но и на
другие вирусы. В 70-е годы были описаны варианты интерферонов — типы I и II, продуцируемые разными клетками под влиянием различных стимулов. Тогда же были обнаружены регуляторные функции интерферонов, что послужило основанием для причисления этой группы факторов к цитокинам. Клонирование генов интерферонов и получение рекомбинантных продуктов дало начало биотехнологическому производству этих молекул и значительно расширило возможности их использования в клинической практике. Интерфероны оказались первыми описанными цитокинами и первыми цитокинами, применяемыми в практике.
В настоящее время выделяют 12 (у человека — 9) видов интерферонов, обозначаемых греческими буквами. По способности взаимодействовать с 3 типами рецепторов их объединяют в 3 семейства. Больше всего видов принадлежит к интерферонам I типа: IFNα, IFNβ, IFNδ, IFNε, IFNκ, IFNτ, IFNω, а также лимитин (у человека IFNδ, IFNτи лимитин не обнаружены). Тип II, ранее обозначавшийся как иммунный интерферон, включает единственный член — IFNγ. Описанный недавно тип III содержит 3 представителя — λ1, λ2 и λ3, называемые также IL-29, IL-28А и IL-28В соответственно. IFNα имеет 13 разновидностей, обозначаемых цифрами (1, 2, 4–8, 10, 13, 14, 16, 17, 21) или латинскими буквами. Каждый вид и разновидность интерферонов кодируются отдельным геном. Некоторые гены существуют в нескольким аллельных вариантах, которым соответствуют изоформы IFNα(например, α2а, α2b, α2с). Таким образом, в настоящее время всего выделяют 49 вариантов молекул интерферонов. Интерфероны типов I и III различаются по локализации генов (у человека — соответственно в хромосомах 9р и 19q), наличию интронов в генах интерферонов III, но не I типа и, что особенно существенно, по действию на разные рецепторы. IFN II типа (IFNγ) отличается от других интерферонов по всем показателям; спектр его биологической активности коренным образом отличается от таковой интерферонов I и III типов.
Интерфероны типов I и III
[править]IFN I типа объединяет 24 изотипа IFN-α (лейкоцитарного IFN), IFN-β (фибробластный IFN), IFN-τ (трофобластный IFN), IFN-ω, IFN-σ, IFN-κ, IFN-ε. В ответ на индукцию патогенассоциированными молекулярными структурами инфекционных агентов (РАМР), особенно вирусными двуцепочечными РНК (дцРНК), все ядерные, в том числе и малодифференцированные клетки организма продуцируют IFN I типа . Однако разные представители группы IFN I типа продуцируются различными клетками. Так, IFN-α и IFN-ω продуцируются гемопоэтическими клетками; IFN-β — фибробластами, гемопоэтическими и эпителиальными клетками; IFN-τ — трофобластами; IFN-κ и IFN-ε — кератиноцитами и клетками плаценты.
Недавно были идентифицированы IFN III типа (IFN-λ1/IL-29, IFN-λ2/IL-28A, IFN-λ3/IL-28B), которые продуцируются эпителиоцитами респираторного тракта, DC, особенно плазмацитоидными дендритными клетками (pDC), моноцитами и макрофагами в ответ на их возбуждение РАМР инфекционных агентов. Так, продукция IFN III типа активируется вирусными одноцепочечной РНК (оцРНК), дцРНК и CpG ДНК (CpG ДНК — участок ДНК, состоящий из более чем 500 bp (пар оснований), который содержит более 55 % неметилированных цитозин-гуаниновых динуклеотидов), в частности, цитомегаловируса. Гены, кодирующие IFN III типа в отличие от генов IFN I типа содержат интроны. IFN III типа взаимодействуют со специфическим рецептором, состоящим из двух субъединиц, одна субъединица которого принадлежит семейству цитокиновых рецепторов II класса, другая идентична субъединице 2 рецептора IL-10. Уровень экспрессии рецептора IFN III типа существенно отличается в различных тканях организма.
В настоящее время идентифицировано 24 гена, кодирующих изотипы IFN-α, по одному гену для IFN-β, IFN-ω, IFN-τ, IFN-σ, IFN-κ, IFN-ε, IFN-γ, IFN-ζ/limitin и три гена для IFN-λ. Гены IFN-a представлены геном непосредственного раннего ответа (IFN-α4), который реагирует на стимул немедленно, и генами с отсроченной реакцией транскрипции (IFN-α2, IFN-α5, IFN-α6, IFN-α8 и др.
Каскад возбуждения системы интерферонов
Для людей в состоянии здоровья характерен очень низкий уровень концентрации IFN в сыворотке крови, который резко повышается при развитии инфекционного процесса или после стимуляции митогенами и антигенами. Появление IFN в сыворотке крови является маркером активации одной из первых линий защиты, направленной против внутриклеточных инфекционных агентов. Среди клеток, участвующих в интерфероновой системе, условно различают две функциональные группы. Первую группу составляют клетки, которые при индукции РАМР синтезируют IFN, вторую группу — клетки, активируемые IFN. Учитывая аутокринное действие интерферона, интерферонпродуцирующие клетки могут быть и интерферонактивируемыми клетками одновременно, но не все интерферонактивируемые клетки являются интерферонпродуцентами .
В основе регуляции интерфероногенеза лежат как положительная обратная связь, обусловленная индукцией синтеза интерферона интерфероном, так и отрицательная обратная связь, характеризующаяся способностью IFN индуцировать синтез супрессоров Jak/STAT пути. Разнонаправленность регулирующих векторов приводит к волнообразному характеру продукции IFN. Каскад активации системы интерферона, развивающийся в течение острой респираторной инфекции, может быть представлен в виде последовательности событий (рис. 1).
Интерферон γ
[править]Фагоцитоз
[править]
Под фагоцитозом понимают поглощение клеткой частиц размером более 0,5 мкм. Как уже отмечалось, явление фагоцитоза было открыто И.И. Мечниковым (1882). Он показал фундаментальную роль фагоцитоза как способа питания одноклеточных организмов, эволюционировавшую у многоклеточных в механизм защиты от чужеродных агентов. В настоящее время роль фагоцитоза в организме многоклеточных рассматривают еще шире: показано его участие в морфогенезе, элиминации клеток, погибающих по механизму апоптоза и т.д.
Традиционно выделяют 8 стадий фагоцитоза :
- приближение к объекту фагоцитоза в результате хемотаксиса;
- адгезия;
- активация мембраны;
- погружение;
- образование фагосомы;
- слияние фагосомы и лизосомы, образование фаголизосомы;
- киллинг и расщепление объектов фагоцитоза;
- выброс продуктов деградации.
Рассмотрим фагоцитоз с этапа адгезии, на котором клетки-участники фагоцитарного процесса взаимодействуют физически.
Адгезия фагоцитов к объектам фагоцитоза. Феномен опсонизации.
[править]Обязательным условием адгезии фагоцита служит распознавание объекта фагоцитоза. Механизмы распознавания разнообразны и принципиально различаются в случаях фагоцитоза опсонизированного и неопсонизированного объектов.
В отсутствие опсонизации молекулярное распознавание, необходимое для прилипания фагоцитов к клеткам-мишеням, существляется в основном двумя группами рецепторов. Одна из этих групп — scavenger-рецепторы («мусорщики»), физиологически предназначенные для элиминации липопротеинов низкой плотности и способные распознавать липидные компоненты бактерий. Вторая группа участвует в элиминации апоптотических клеток: αvβ3-интегрин, распознающий витронектин, и рецептор фосфатидилсерина (оба лиганда появляются на поверхности клеток при нарушении
асимметрии клеточной мембраны в процессе апоптоза). В качестве рецептора еще одной молекулы, экспрессируемой апоптотическими клетками, выступает тромбоспондин. Эта растворимая молекула кооперируется с
двумя упомянутыми мембранными рецепторами: она первой связывается со своим лигандом и облегчает распознавание других маркеров апоптоза мембранными рецепторами профессиональных (макрофаги) и факультативных (эндотелиальные клетки) фагоцитов.
Распознавание фагоцитом предварительно опсонизированных клеток более типично для инфекционных процессов. Под опсонизацией (от греч. οψονεο — подготавливать пищу) понимают обволакивание частицы молекулами, облегчающими ее распознавание и поглощение фагоцитом. Существует 2 основных варианта опсонизации: в одном случае опсонизирующие агенты — антитела класса IgG, а в другом — фрагмент С3-компонента комплемента iС3b. Часто оба фактора опсонизируют клетку совместно. Это
неудивительно, поскольку антитела в составе иммунных комплексов активируют комплемент, что приводит к отложению на клетке-мишени C3b, расщепляющегося до iC3b. Однако опсонизация компонентами комплемента более распространена, поскольку активация комплемента возможна без участия антител (альтернативный и лектиновый пути) или с участием антител, для которых на фагоцитах нет рецепторов (например, IgM-антител). Своеобразный вариант опсонизации инертных частиц (частиц металла, пластика и т.д.) — обволакивание их белками межклеточного матрикса, в результате чего они становятся доступными для распознавания мембранными β1-интегринами фагоцитов.
Лейкоциты, обладающие фагоцитарной активностью, несут на своей поверхности рецепторы для опсонинов, а также рецепторы-мусорщики и рецепторы, распознающие апоптотические клетки. Последний тип рецепторов широко распространен и свойственен не только «профессиональным» фагоцитам, но и ряду других клеток (эндотелиальные, эпителиальные и т.д.). Благодаря способности многих типов клеток элиминировать апоптотические клетки, не происходит «загрязнения» продуктами распада тканей, в которых в физиологических условиях происходит массовая гибель клеток путем апоптоза (например, при эмбриогенезе).
При распознавании рассмотренными рецепторами своих лигандов происходит сближение фагоцитов с их мишенями, обычно закрепляемое молекулами адгезии, в частности β1-интегрином VLA-4 и β2-интегрином LFA-1. На поверхности бактериальных клеток отсутствуют рецепторы интегринов (IСAM, VCAM, белки межклеточного матрикса), однако обычно присутствуют короткие аминокислотные последовательности, распознаваемые интегринами (например, последовательность RGD, распознаваемая некоторыми
интегринами). Распознавание неопсонизированных патогенов затруднено. Опсонизация облегчает этот процесс.
Рецепторы для распознавания опсонинов (Fc- и C3-рецепторы).
[править]Рассмотрим 2 типа рецепторов, играющих основную роль в распознавании опсонинов, фиксированных на поверхности фагоцитируемых клеток: рецепторы для Fc-части иммуноглобулинов/антител (FcR) и рецепторы для комплемента (CR).
Fc-рецепторы
Распознавание патогенов и других клеток, опсонизированных антителами класса IgG, осуществляется с помощью Fc-рецепторов (FcγR), экспрессированных на поверхности фагоцитов. Эти рецепторы распознают участки хвостовой части (Fc) молекул иммуноглобулинов IgG-класса (в наибольшей степени субклассов IgG1 и IgG3). Эти участки расположены в CН2- и СН3-доменах γ-цепей иммуноглобулинов. В молекулах свободных антител они скрыты и открываются только при связывании с антигеном, сопровождающимся изменением конфигурации молекулы IgG. Кроме Fcγ-рецепторов, известны Fc-рецепторы, распознающие связанные антитела классов IgA и IgE (FcαR и FcεR). Функциональная роль Fc-рецепторов значительно шире их участия в распознавании объектов фагоцитоза, поэтому они будут многократно упоминаться в дальнейшем.

У человека выделяют 3 типа Fcγ-рецепторов — FcγRI (CD64), FcγRII(CD32) и FcγRIII(CD16); 2 последних типа существуют в нескольких вариантах, различающихся устройством С-концевой части. Перечисленные рецепторы отличаются друг от друга сродством к Fc-части молекулы IgG. В порядке убывания аффинности они образуют ряд: FcγRI > FcγRII> FcγRIII.
Наиболее высокоаффинный рецептор FcγRI состоит из двух полипептидных цепей. Цепь, связывающаяcя c Fc-участком γ-цепи IgG (α-цепь), имеет 3 внеклеточных домена, относящихся к суперсемейству иммуноглобулинов. Ее цитоплазматический участок лишен последовательностей, позволяющих передавать сигнал внутрь клетки. Такая активационная сигнальная последовательность (участок ITAM — Immunoreceptor tyrosine-based activation motif ) есть в цитоплазматической части другой полипептидной цепи — γ-цепи, осуществляющей в связи с этим сигнальную функцию рецептора. FcγRI экспрессирован на покоящихся клетках только одного типа — макрофагах; нейтрофилы и эозинофилы начинают экспрессировать его после активации. Это единственный тип Fcγ-рецепторов, связывающий свободные антитела. Фиксация антител на FcγRI обусловливает формирование «армированных» макрофагов, несущих на поверхности антитела с активными центрами, направленными наружу.
Рецепторы FcγRII представлены более широко: они свойственны практически всем клеткам врожденного иммунитета, а также В-лимфоцитам. FcγRII тоже имеют одну α-цепь, содержащую 2 внеклеточных иммуноглобулинподобных домена. Внутриклеточный участок α-цепи FcγRII по протяженности превосходит аналогичные участки других Fc-рецепторов. Известно 2 варианта этих рецепторов — FcγRIIA и FcγRIIВ, различающися особенностями строения их цитоплазматической части. FcγRIIA содержит
в ней активационный мотив ITAM, а FcγRIIВ — ингибирующий мотив ITIM (Immunoreceptor tyrosine-based inhibition motif ). Фосфорилирование остатков тирозина в ITAM делает возможным взаимодействие его с тирозинкиназами семейства Syk, что служит основой для передачи активационного сигнала. Фосфорилирование тирозина в ITIM обеспечивает его взаимодействие с фосфатазами SHP1, SHP2 и SHIP, ослабляющими активационный сигнал и оказывающими ингибирующее действие . Рецепторы FcγRIIA присутствуют на поверхности фагоцитов различной природы и играют важную роль в распознавании опсонизирующих антител. Рецепторы FcγRIIB экспрессированы преимущественно на В-лимфоцитах и участвуют в регуляции их активности.
Низкоаффинные рецепторы FcγRIII имеют сложную структуру. Помимо основной α-цепи, имеющей 2 иммуноглобулинподобных внеклеточных домена, они содержат 2 дополнительные цепи, идентичные γ-цепям рецепторов FcγRI или FcεRI. Эти цепи несут участок ITAM. По особенностям структуры С-концевой части α-цепи эти рецепторы также неоднородны. Их основной вариант — FcγRIIIА — содержит α-цепь, имеющую полноценную трансмембранную и внутриклеточную части, причем последняя взаимодействует с γ-цепью, что позволяет рецептору передавать сигнал в клетку. Такой вариант рецептора характерен для естественных киллерных клеток, а также моноцитов, макрофагов и ряда других клеток. Альтернативный вариант — FcγRIIIВ, содержащий α-цепь, заякоренную в мембране через гликозилфосфатидилинозитол. Этот вариант рецептора экспрессируется на нейтрофилах.
С3-рецепторы
С3-рецепторы по своей структуре более гетерогенны, чем Fc-рецепторы. Известно 4 разновидности С3-рецепторов. CR1 (CD35) экспрессирован не только на классических фагоцитах (нейтрофилах, моноцитах), но и на ряде других клеток: В-лимфоцитах, эритроцитах, фолликулярных дендритных клетках. На последних CR1 участвует в связывании иммунных комплексов, т.е. выполняет важнейшую функцию, играющую ключевую роль в развитии гуморального иммунного ответа. Молекула CD35 связывает, помимо C3b, фрагмент C3d. Рецептор CR2(CD21) имеет наиболее широкий спектр лигандов. Он связывает фрагменты С3, находящиеся на разных стадиях деградации — С3b, iC3b, С3d. Кроме того, CR2 служит рецептором вируса Эпштейна–Барр. Этот рецептор экспрессирован на В-лимфоцитах и фолликулярных дендритных клетках, но не на фагоцитах. Он не имеет отношения к фагоцитозу, но играет важную роль в активации В-клеток и процессах гуморального ответа, происходящих в зародышевых центрах. Наконец CR3 и CR4 представляют уже охарактеризованные β2-интегины — Мас-1(СD11b/CD18) и p150/95(CD11c/CD18). Они связывают инактивированный фрагмент C3b — iC3b . Все С3-рецепторы играют важную роль в контроле активации комплемента, ингибируя связывание С3 с поверхностью собственных клеток и ускоряя отделение компонентов комплемента от иммунных комплексов.
Активация, обусловленная связыванием рецепторов фагоцитов. Формирование фагоцитарной чаши
[править]Распознавание мишеней фагоцитоза через различные мембранные рецепторы фагоцитов приводит к запуску процессов активации, отличающихся деталями, но приводящих к одинаковому результату — погружению и по-следующему разрушению частицы.
На начальных стадиях фагоцитоза основные события происходят на обращенном к мишени участке поляризованной клетки, где должна сформироваться временная структура, называемая фагоцитарной чашей (phagocytic cap). На поверхности патогена обычно фиксировано несколько молекул антител. Они обусловливают объединение Fc-рецепторов в кластеры в результате перекрестного сшивания. Это приводит (за счет конформационных изменений) к активации прилежащих к цитоплазматической части рецепторов
тирозинкиназ семейства Src. Эти киназы фосфорилируют цитоплазматические участки рецептора, в том числе остатки тирозина в мотиве ITAM, а также контактирующие с ними киназы семейства Syk. Фосфотирозины ITAM обеспечивают связывание этого мотива с SH2-доменами Syk-киназ. Далее активационная волна передается на ряд ферментов, определяющих дальнейший ход событий.
Следующий этап активации направлен на образование продуктов, участвующих в полимеризации актина — процесс, на котором основан фагоцитоз. Для реализации этого этапа необходимо участие ГТФаз — Rac-1, Cdc42 (их активность преобладает при FcγR-зависимом фагоцитозе) и Rho (задействована преимущественно в комплементзависимом поглощении частицы). Нити актина окружают основание формирующейся фагоци-тарной чаши. За их адгезию к мембране в этих участках отвечают белки семейства MARCKS (Myristoylated alanine-rich C kinase substrate), активируемые протеинкиназой С. Полимеризация актина в сочетании с погружением частиц составляет основу формирования фагоцитарной чаши — главного результата рассмотренных процессов и исходной позиции следующего этапа фагоцитоза.
Формирование и созревание фагосомы
[править]Существуют различия в феноменологии процесса погружения частицы в зависимости от того, какие рецепторы участвуют в ее распознавании. При FcγR-зависимом фагоцитозе в захвате объекта участвуют псевдоподии, тогда как при комплементзависимом фагоцитозе частица погружается в клетку без их формирования. Хотя в инициации фагоцитоза задействовано несколько миозинов, в формировании псевдоподий главная роль при-надлежит миозину Х, активация которого происходит при связывании с продуктами PI3K. Миозин Х рассматривается как основной «двигатель» при формировании фагосомы.
Погружение частицы обусловлено сокращением нитей актина, сконцентрированных вокруг фагоцитарной чаши. Погружение формирующейся фагосомы в клетку заверашется смыканием над ней мембраны, подобно застежке-молнии. Сразу после этого нити актина исчезают из окружения фагосомы. Процесс разборки актиновых нитей зависит от ионов Са2+. В то же время актиновые филаменты формируют нити, отходящие от фагосомы внутрь клетки, и их сокращение перемещает фагосому в глубь цитоплазмы.
Сразу после образования фагосома не несет бактерицидных веществ и ферментов, способных разрушить патоген. Перемещаясь внутрь клетки, фагосома проходит процесс созревания, основу которого составляют множественные акты слияния с фагосомой различных гранул, привносящих в
нее эффекторные молекулы. Показатель созревания — смена мембранных маркеров фагосом: сначала на ее мембране присутствуют маркеры ранних эндосом (Rab5, EEA1), затем они сменяются маркерами поздних эндосом (Rab7, Rab9, белки группы LAMP2). Другие показатели созревания —
закисление содержимого и изменение спектра ферментов, содержащихся в фаголизосомах. При созревании фагосомы претерпевают изменения, характерные для эндосом в целом. Слияние с эндосомами реализуется по механизму, сходному с механизмом доставки мембран к фагоцитарной чаше. Ключевую роль при этом играют белки семейства SNARE, входящие в состав мебран сливающихся гранул. Эти белки гомотипически взаимодействуют между собой. В большинстве случа-ев направление движения эндосом к фагосоме определют микротрубочки.
Слияние гранул стимулируется повышением уровня внутриклеточного Са2+.
Решающий вклад в созревание фагосом и обретение ими способности убивать и расщеплять поглощенные объекты вносят лизосомы. Слияние фагосомы и лизосомы рассматривают как момент формирования фаголизосомы. В нейтрофилах источник бактерицидных веществ и ферментов
для фагосомы — специализированные лизосомоподобные гранулы — специфические (нейтральные, раньше всего сливающиеся с фагосомами),
азурофильные (кислые, сливающиеся с фагосомами позже), желатиназные, а также секреторные гранулы. Наиболее важна при созревании доставка в фаголизосому комплексов NADPH-оксидазы при помощи специфических гранул. По мере последовательного вливания в фаголизосому содержимого различных гранул изменяется рН ее содержимого, возрастает ее бактрицидный потенциал и способность разрушать те или иные субстраты. Последовательность вовлечения различных гранул в формирование фаголизосомы зависит от порогового уровня их чувствительности к ионам Са2+: он выше для азурофильных гранул, чем для специфических, поэтому азурофильные гранулы позже сливаются с фагосомами.
Это придает процессу созревания фаголизосомы определенную «логику»: сначала проявляют свою активность ферменты с нейтральным оптимумом
действия, поступающие из специфических гранул, а по мере закисления среды мобилизуются ферменты азурофильных гранул, наиболее активные
при кислых значениях рН. Сенсорами для ионов Са2+ в гранулах служат белки семейства синаптостагминов. Процесс слияния гранул контролируют также киназы и ГТФазы семейства Rab (в частности белок Rab5).
Сформированная фаголизосома — клеточная органелла, специализированная для осуществления киллинга и расщепления фагоцитированных
корпускулярных объектов.
.
Бактерицидная функция фагоцитов
[править]Конечное назначение фагоцитоза состоит в создании оптимальных условий для киллинга и цитолиза патогенов, т.е. в осуществлении внутриклеточного цитолиза. Поэтому эффективность фагоцитоза обусловлена не столько поглощением патогена, сколько его разрушением внутри клетки. В зависимости от реализации бактерицидных свойств, различают завершенный и незавершенный фагоцитоз. Только первый отвечает своему биологическому предназначению и может рассматриваться как эффективная защитная реакция — проявление врожденного иммунитета. Киллинг происходит в фаголизосомах фагоцитов. Фаголизосомы содержат факторы, разрушающие микроорганизмы. Выделяют несколько групп таких факторов:
- кислородзависимые факторы:
- активные формы кислорода;
- галоидсодержащие соединения;
- азотистые метаболиты;
- кислород- и оксид азота-независимые факторы:
- факторы, обусловливающие локальное закисление;
- бактрицидные пептиды;
- катионные белки;
- ферменты;
- конкурентные ингибиторы метаболизма.
Все эти факторы проявляют свою бактерицидную и литическую активность преимущественно в фаголизосомах, в которые они поступают из лизосом (ферменты, пептиды) или генерируются de novo(активные формы кислорода и азота). Некоторые из бактерицидных факторов (NO и его метаболиты) могут формироваться и действовать вне гранулярного аппарата клеток. Все бактерицидные факторы могут проявлять свою активность также за пределами клетки, куда они попадают в результате дегрануляции или других форм секреции. Однако эти факторы следует отличать от бактерицидных факторов, не связанных с фагоцитозом, а участвующих в реализации внеклеточного цитолиза.
Кислородзависимые факторы бактерицидности
[править]В обеспечении киллинга фагоцитированных микроорганизмов наиболее важна роль производных кислорода. Главное событие в образовании
кислородзависимых бактерицидных факторов — кислородный взрыв — быстрое (реализуемое за секунды) и высокопродуктивное осуществление цепи
реакций, приводящих к образованию активных форм кислорода. Активные формы кислорода включают высокореактивные свободные радикалы, ионы кислорода и кислородсодержащих химических групп. Образование активных форм кислорода катализируется ферментом NADPH-оксидазой(NADPH — восстановленная форма никотинамиддинуклеотидфосфата), называемой также оксидазой фагоцитов (Phоx).
Сборка NADPH-оксидазы

Кислородный взрыв реализуется в мембране фаголизосом. Сборка NADPH-оксидазы — исходное событие в запуске кислородного взрыва и генерации активных форм кислорода. NADPH-оксидаза активируется под влиянием сигналов, возникающих при связывании лигандов с Fc-рецепторами, рецепторами-«мусорщиками», родопсиноподобными рецепторами. Сначала этот процесс происходит в участке клеточной мембраны, примыкающем к зоне действия хемотаксического агента или к зоне контакта с фагоцитируемым объектом. При формировании фагосомы сборка NADPH-оксидазы перемещается внутрь клетки.
Неактивная NADPH-оксидаза локализуется в мембране секреторных везикул и специфических гранул. Она представляет собой флавоцитохром b558,
состоящий из субъединиц α(p22phox) и β(gp91phox), а также белка Rap1а. При активации к NADPH-оксидазе подсоединяется 4 цитозольных белка: p47phox, p67phox, p40phox и ГТФаза Rac-2. При фагоцитозе гранулы и везикулы, содержащие NADPH-оксидазу, сливаются с фагосомой. Активация фермента происходит уже в составе мембраны фаголизосомы. В привлечении цитозольных компонентов важная роль принадлежит мембранным фосфоинозитидам, обеспечивающим связывание цитозольных компонентов Phox — фосфотидилинозитол-3,4-дифосфата (PI-3,4P2) и фосфотидилинозитол-3-монофосфата (PI-3P), а также фосфотидилинозитолкиназ, катализирующих их образование.
Под влиянием активационных сигналов, генерируемых при связывании родопсиноподобных рецепторов, происходят фосфорилирование p47phoxи активация двух его доменов: PX и SH3. При участии PX-домена p47phox прикрепляется к PI(3,4)P2 мембраны фаголизосомы, а с помощью SH3-домена — к С-концевой цитозольной части мембранного компонента цитохрома b558 — p22phox. Переместившись в мембрану, p47phox способствует внедрению в нее белка p67phox
, происходящему за счет взаимодействия С-концевого домена p47phox и С-концевого SH3-домена p67phox. Адапторный белок p40phox связан с p67phox исходно, а через PX-домен он присоединяется к PI-3P мембраны. Одновременно ГТФаза
Rac-2 освобождается от ингибитора, блокирующего ее при покоящемся состоянии клетки (отделение от ингибитора обусловлено осфорилированием Rac-2), и внедряется в мембрану фагосомы, где взаимодействует с молекулой p67phox. Таким образом, осуществляется полная сборка NADPH-оксидазы.
Образование активных форм кислорода
Конформационные изменения, происходящие при сборке NADPH-оксидазы, приводят к тому, что ее основной компонент gp91phox приобретает способность взаимодействовать с окисленной формой кофактора, образующегося при гликолизе, — NADPH. Это взаимодействие происходит при участии простетической группы FAD (флавин адениндинуклеотид) и двух молекул гема. FAD получает электрон (е-) от NADPH и передает его «наружной» молекуле гема, обращенной к цитозолю, от которой он переходит к «внутренней» молекуле гема, обращенной к содержимому фагосомы. Внутренняя молекула гема передает электрон молекуле кислорода, что приводит к образованию супероксида , объединяющего в себе свойства аниона и радикала, и потому называемого супероксидрадикалом, или супероксиданионом (*О2Ї). Супероксидрадикал — короткоживущий родоначальник активных форм кислорода. В начальную фазу фагоцитоза супероксиданион, образующийся на участке клеточной мембраны, находится во внутриклеточном пространстве; после формирования фагосомы и фаголизосомы он поступает внутрь этих гранул.
На следующем этапе реализуется цепь реакций, приводящих к образованию радикалов, ионов кислорода и содержащих их молекул, обладающих более высокой бактерицидной активностью чем супероксианион, — активных форм кислорода. Под действием фермента супероксиддисмутазы из двух молекул супероксидного аниона образуется перекись водорода. В присутствии ионов Fe2+ супероксид взаимодействует с перекисью водорода с образованием гидроксил-радикала (*ОН) — сильного окислителя. Перекись водорода и особенно гидрокисл-радикал обладают очень сильной бактерицидной активностью. При их совместном действии происходит перекисное окисление липидов, разрыв пептидных связей, окисление сульфгидрильных групп и другие глубокие химические изменения макромолекул в клеточных стенках патогенов, приводящие к их гибели. При мутациях генов, кодирующих субъединицы NADPH-оксидазы, нарушается активность этого фермента и, как следствие, развивается хроническая гранулематозная болезнь.
Кислородзависимые факторы бактерицидности, индуцируемые миелопероксидазой
Миелопероксидаза — маркерный фермент азурофильных гранул нейтрофилов. Она составляет 1–5% общего белка этих клеток. Зрелая молекула миелопероксидазы — гетеродимер, образованный тяжелой α- и легкой β-цепями. С α-цепью связана железосодержащая группа — гем. Миелопероксидазная микробицидная система включает, помимо собственно миелопероксидазы, перекись водорода и кофакторы, в том числе ионы галогенов (Cl-, I-, Br-).
Миелопероксидаза катализирует в фаголизосомах окислительные реакции. Превращение йодида (I-) в молекулярный йод (при участии миелопе-роксидазы и перекиси водорода) обеспечивает его связывание с сульфгидрильными группами белков, приводящее к нарушению жизнеспособности микроорганизмов. При катализируемом миелопероксидазой взаимодействии ионов Cl- с перекисью водорода образуется сильный микробицидный агент — хлорноватистая (гипохлорная) кислота HOCl. При ее взаимодействии с аминокислотами образуются хлорамины, обладающие бактерицидным действием. При окислении хлорноватистой кислоты супероксидом образуется гидроксильный радикал *ОН, а при ее оксилении перекисью водорода — синглетный кислород ‘О2
Эти метаболиты обладают сильной микробицидной активностью. Синглетный кислород особенно активно взаимодействует с полиненасыщенными жирными кислотами, вызывая их перекисное окисление, нарушающее целостность мембраны бактерий. Синглетный кислород участвует в образовании еще одного микробицидного вещества — озона (О3).
Нейтрофилы — наиболее эффективные продуценты активных форм кислорода. К этим агентам чувствительны разные типы микроорганизмов, в первую очередь — внеклеточные патогены.
Оксид азота и его производные
[править]Активные формы азота образуются при окислении аргинина с его превращением в цитруллин. Известно 2 пути превращения аргинина,
один из которых катализируется аргиназой и приводит к образованию орнитина. Продукты другого пути, катализируемого NO-синтазой, — цитруллин и оксид азота. Известно 3 изоформы NO-синтазы, из которых эпидермальная и нейрональная экспрессируются спонтанно в соответствующих клетках, а макрофагальная NO-синтаза является индуцибельной (iNOS). Именно макрофагальная изоформа ответственна за образование активных форм азота в фагоцитах. Основной индуктор iNOS —
IFNγ; этот фактор вносит важный вклад в усиление микробицидной активности макрофагов. Другой активатор iNOS — тетрагидроптерин — активируется TNFα. Оптимальное условие индукции iNOS — сочетанное
действие IFNγ и TNFα.
Оксид азота (NO) обладает микробицидной активностью. Особенно сильные бактерицидные свойства проявляет продукт взаимодействия оксида азота с супероксидным радикалом — пероксинитрит (OONOЇ), окисляющий сульфгидрильные группы белковых и небелковых молекул, нарушая при этом их функции. Из пероксинитрита образуются другие активные формы азота — радикалы NO2* и ОН*. В процессе превращения оксида азота происходит образование анионов и радикалов нитрита (NO2-, NO2*), а также нитратанионов (NO3-).
Основные продуценты активных форм азота — моноциты/макрофаги. Хотя нейтрофилы также способны синтезировать некоторое количество оксида азота, его роль в микробицидном эффекте для этих клеток не доказана. К активным формам азота наиболее чувствительны внутриклеточные патогены — микобактерии, грибы, простейшие. Поскольку образование оксида азота возможно вне фагосом в цитозоле, он действует не только на фагоцитируемые микроорганизмы, но и на вирусы, Mycobacterium tuberculosis, грибы и простейшие. Оксид азота обладает также тумороцидным эффектом.
Факторы бактерицидности, не зависящие от кислорода и оксида азота
[править]Микроорганизмы выработали способы нейтрализации факторов кислородзависимой бактерицидности, а также NO и связанных с ним азотсодержащих соединений, основанные на действии бактериальных супероксиддисмутаз, каталаз и др. Однако у фагоцитов сформировались альтернативные механизмы бактерицидности.
Закисление внутренней среды фаголизосомы
При эндоцитозе содержимое эндосом закисляется. Для ранних эндосом характерны слабокислые значения рН (6,0–6,5). В содержимом поздних эндосом рН составляет 5,5–6,0, а в лизосомах — <5,0. Аналогичные изменения рН происходят при созревании фагосом. Закисление содержимого гранул — необходимое условие их слияния с фагосомами. Последовательное закисление среды в эндосомах — результат активности V-АТФазы — сложного белка, перекачивающего протоны из цитозоля в гранулы. V-АТФаза состоит из нескольких субъединиц. V-АТФаза отсутствует в фагосомах, но доставляется в них с лизосомами. В нейтрофилах V-АТФаза содержится во всех разновидностях гранул, кроме специфических (отсюда нейтральная реакция их содержимого). В фаголизосомах рН составляет 4,5–5,0. В фаголизосомах нейтрофилов pH среды несколько выше, чем в аналогичных структурах макрофагов. Это связано с более активной работой в нейтрофилах NADPH-оксидазы, сопряженной с потреблением протонов для
формирования перекиси водорода. Кроме того, активные формы кислорода ослабляют активность V-АТФазы.
Закисление среды фаголизосомы оказывает бактериостатическое и бактерицидное действие, поскольку при значениях рН, близких к 4,5, снижается электростатический потенциал клеток микроорганизмов, что приводит к нарушению поступления в них питательных веществ. Кроме того, кислая среда способствует активации большинства ферментов (особенно из азурофильных гранул), обладающих бактерицидной и бактериолитической активностью. Продукты, выделяющиеся при разрушении микроорганизмов, усиливают закисление.
Ферменты
При описании азурофильных и специфических гранул нейтрофилов уже перечисляли содержащиеся в них ферменты (общее число ферментов, выявляемых в фаголизосомах — более 60). Как известно, сначала с фагосомами сливаются специфические гранулы, содержащие ферменты, активные при нейтральных и слабощелочных значениях рН (именно такой pH имеет среда фагосом на данном этапе): щелочную фосфатазу и лизоцим, входящие в группу катионных белков.
Азурофильные гранулы доставляют в фаголизосомы широкий набор кислых гидролаз и других ферментов, активных при кислых значениях рН: миелопероксидазу, 5’-нуклеотидазу, β-арилсульфатазу, β-глюкуронидазу, кислую глицерофосфатазу, а также гликозидазы. Азурофильные гранулы — дополнительный источник лизоцима и лактоферрина. Из азурофильных гранул в фаголизосому поступают также нейтральные протеазы, объединяемые в группу серпроцидинов, — еще одних представителей катионных белков.
Большинство сосредоточенных в фаголизосомах ферментов участвуют в расщеплении убитых микроорганизмов.
Катионные белки
В составе катионных белков преобладают щелочные аминокислотные остатки (что и определяет их катионность). Среди катионных белков есть как обладающие ферментативной активностью (лизоцим и серпроцидины), так и конкурентные белки, бактерицидное действие которых основано на связывании жизненно важных для патогенов веществ (лактоферрин, витамин В12-связывающий фактор).
Лизоцим — катионный белок. Его молекулярная масса 15 кДа, изоэлектрическая точка (pI) — 10. Лизоцим — фермент, обладающий активностью мурамидазы. Действуя на гликановый компонент молекул, лизоцим вызывает деполимеризацию пептидогликанов клеточной стенки микроорганизмов, тем самым нарушая ее целостность. Обычно субстрат лизоцима в интактной клетке маскирован поверхностными молекулами. В связи с этим активность лизоцима проявляется только при его комбинации с другими ферментами, например, в фаголизосоме.
Серпроцидины (от Serine protease cidin) — группа гомологичных белков, обладающих протеазной активностью, включающая катепсин G, эластазу, азурацидин и протеиназу-3. Молекулярная масса серпроцидинов варьирует от 25 до 29 кДа. Щелочной характер этих белков обсуловлен высоким содержанием аргинина и амидированных форм дикарбоновых аминокислот (глутамин, аспарагин). Некоторые серпроцидины присутствуют не только в нейтрофилах, но и в моноцитах. Эти белки обладают микробоцидной активностью, не коррелирующей с протеолитической активностью. In vitro серпорцидины действуют на грамположительные и грамотрицательные бактерии, простейших, патогенные грибы, а также на клетки эукариот. Наибольшей микробоцидностью обладает катепсин, наименьшей — эластаза и протеиназа-3. Однако выключение гена эластазы значительно снижает гибель фагоцитированных микроорганизмов. Часто серпроцидины действуют совместно и при этом оказываются более эффективны, чем по отдельности. Катепсин G сохраняет микробицидную активность даже во фрагментированном состоянии. Активность серпроцидинов вне клеток подавляется ингибиторами сериновых протеиназ серпинами. Серпроцидины структурно и функционально родственны гранзимам цитотоксических лимфоцитов.
Лактоферрин — катионный белок, служащий маркером специфических гранул. Для него характерна способность формировать прочный комплекс с двумя ионами Fe3+ или других металлов с переменной валентностью. Взаимодействие происходит с участием ионов бикарботата. При связывании ионов железа образуется вещество красного цвета, что определило первоначальное обозначение лактоферрина как «красного белка».
Способность лактоферрина связывать ионы железа — основа его бактерицидного действия. Лактоферрин образует хелаты с ионами Fe3+ и создает их дефицит. Ионы железа участвуют в разнообразных жизненно важных процессах микроорганизмов, включая размножение. Секвестрирование ионов железа некоторые авторы рассматривают как один из фундаментальных механизмов защиты макроорганизма не только от инвазии патогенов, но и от роста опухоли. Бактериостатическое действие лактоферрина, основанное на конкуренции за ионы железа, — реальный механизм врожденного иммунитета. Помимо этого показана возможность прямого микробоцидного действия лактоферрина на некоторые патогены, однако оно выражено достаточно слабо.
BPI-протеины (от Bаcteria permeability inducing) — белки, повышающие проницаемость бактериальной стенки — образуют еще одну группу катионных белков с бактерицидной активностью. Молекулярная масса BPI-протеинов составляет 59 кДа. Они представлены в нейтрофилах и эозинофилах. Как и другие катионные белки, BPI-протеины обогащены основными аминокислотными остатками, в частности лизином, и содержат гидрофобные участки. Их изоэлектрическая точка (рI) составляет около 9,5. Белки этой группы действуют на грамотрицательные бактерии, распознавая ЛПС (они гомологичны ЛПС-связывающим белкам). BPI-протеины связываются с поверхностью бактерий при помощи электростатических взаимодействий.
При проникновении в мембрану BPI-протеины проявляют сродство к ЛПС, блокируя его активность (это может быть основанием для их возможного клинического применения). Литическое действие BPI-протеинов коррелирует с повышением проницаемости бактериальной стенки для белков.
Бактерицидные пептиды
Бактерицидные, или антибиотические, пептиды — наиболее интенсивно изучаемые бактерицидные факторы многоклеточных. Выделяют несколько групп бактерицидных пептидов, из которых наиболее известны дефензины и кателицидины.
Дефензины — катионные пептиды молекулярной массой 3–5 кДа (обычно содержат около 30 аминокислотных остатков), с характерным высоким содержанием остатков аргинина и других основных аминокислот (лизина, гистидина), а также гидрофобных аминокислот (валина, лейцина, пролина и т.д.). Основные и гидрофобные аминокислоты пространственно разобщены, что придает молекуле пептида амфипатичность. Для дефензинов характерна β-складчатая структура. Важнейшее их свойство — наличие 6 остатков цистеина, формирующих 3 дисульфидные связи. В зависимости от расположения этих связей выделяют α-, β- и θ-дефензины. Для α-дефензинов характерно следующее распределение дисульфидных связей (указаны номера остатков цистеина, скрепляемых связью): 1–6, 2–4, 3–5. Связь между 1-м и последним (6-м) остатками цистеина делает молекулу циклической. Эта цикличность не характерна для β-дефензинов, тогда как θ-дефензины образуют цикл за счет пептидной связи между крайними, не цистеиновыми остатками.
У человека описано 6 разновидностей α-дефензинов. Дефензины группы α — важный компонент фаголизосом нейтрофилов: на их долю приходится 5–7% общего белка нейтрофилов. Нейтрофилы содержат 5 разновидностей α-дефензинов. Они представлены также в некоторых макрофагах (например, легочных). В эпителиальных клетках (в частности, в эпителии крипт слизистой оболочки кишечника) присутствуют 2 другие разновидности α-дефензинов. У человека известно 2 β-дефензина, локализованых в эпителии дыхательных путей, но не в лейкоцитах.
Кателицидины (пептиды, гомологичные кателину) — положительно заряженные амфипатические пептиды. В их структуре преобладают α-спирализованные участки. Кателицидины содержат функционально важный домен, гомологичный катепсину L (кателину). В нейтрофилах человека присутствует 1 вариант кателицидинов — LL-37.
Бактерицидные пептиды проявляют антибактериальную, антимикотическую и антивирусную активность. Их бактерицидность связана с особенностями их строения. Взаимодействие дефензинов с клетками микроорганизмов не зависит от рецепторов и обусловлено электростатическими взаимодействиями положительно заряженных остатков собственных аминокислот с отрицательно заряженными группами (в составе пептидогликанов, ЛПС и др.) на поверхности патогенов. В реализации следующей фазы взаимодействия дефензинов с патогеном решающая роль принадлежит амфипатичности структуры этих пептидов: положительно заряженные группы продолжают контактировать с анионными молекулами клеточной стенки, а гидрофобные участки способствуют внедрению молекулы в клеточную мембрану патогена, что приводит к нарушению ее целостности. Существует несколько моделей, описывающих летальное действие дефензинов. Согласно одной из них («сборка бочки»), мономер пептида встраивается в клеточную стенку микроорганизма, затем к этому мономеру последовательно присоединяются другие. В результате формируется трехмерная циклическая структура («бочка»), образующая канал, через который проходят ионы и более крупные молекулы (гидрофобные участки дефензинов при этом связаны с компонентами мембраны микроорганизма, а гидрофильные участки обращены внутрь микроба). Нарушение целостности мембраны и изоляции внутренней среды микроорганизма от окружения приводит к его гибели.
Дефензины локализованы и оказывают свое действие преимущественно внутри нейтрофилов, точнее, в их фаголизосомах. Однако в результате секреции дефензины могут поступать во внеклеточное пространство и проявлять там свои бактерицидные свойства. Однако эта возможность ограничена содержанием в плазме крови и межклеточной жидкости серпинов — ингибиторов сериновых протеаз, подавляющих действие дефензинов. Во внеклеточном пространстве дефензины проявляют хемокиноподобные и иммунорегуляторные свойства при более низких концентрациях, чем в фаголизосомах.
Секреторная и киллерная активность фагоцитов
[править]Секреторная активность фагоцитов реализуется двумя альтернативными путями, основанными на разных механизмах, — в форме дегрануляции и секреции, зависящей от аппарата Гольджи. Дегрануляция осуществляется при участии микротрубочек и прекращается при их деполимеризации (например, при обработке колхицином). В классический вариант секреции с участием аппарата Гольджи микротрубочки не вовлекаются, однако этот процесс можно нарушить действием цитохалазина и других ядов, повреждающих микрофиламенты.
Выброс фагоцитами продуктов деградации (дегрануляция)
[править]Дегрануляция — основная форма секреторной активности тучных клеток, базофилов и ключевое событие реакций гиперчувствительности немедленного типа. Для эозинофилов дегрануляция служит основным условием внеклеточного цитолиза — формы защиты от многоклеточных паразитов.
Для нейтрофилов дегрануляция — заключительный этап фагоцитоза. Ее следствия — попадание содержимого фаголизосом в межклеточное пространство — побочный эффект реакции. Однако в дегрануляцию вовлекаются не только фаголизосомы, но и свободные гранулы нейтрофилов. Дегрануляция лизосом моноцитов и макрофагов также происходит при фагоцитозе. В эффекторное действие моноцитов и макрофагов дегрануляция вносит меньший вклад, чем аппарат Гольджи-зависимая секреция.
Итак, заключительная фаза фагоцитоза — выброс содержимого фаголизосом путем дегрануляции. За счет сокращения нитей актомиозина фаголизосомы транспортируются по каркасу из микротрубочек к клеточной мембране и сливаются ней. Сигналом к секреции служит повышение уровня внутриклеточного Са2+. Секреция контрoлируются ГТФазами семейства Rab. При этом происходит превращение мембранных фосфоинозитидов, катализируемое PI-3P. Экзоцитоз гранул нейтрофилов может быть спровоцирован действием форболмиристат ацетата, активирующего протеинкиназу С и ряд других ферментов. Ключевую роль во взаимном распознавании мембран играют белки семейства SNARE: под влиянием форболмиристат ацетата на клеточной мембране появляются белки SNAP-23 и синтаксин-4, распознаваемые SNARE-белками мембран гранул синтаксином-6 и VAMP-2, соответственно. Такое распознавание — обязательное условие дегрануляции.
Выброс гранул и фаголизом, образованных с их участием, не совпадает по времени и контролируется не полностью идентичными механизмами. В дегрануляцию специфические гранулы и фаголизосомы, образованные с их участием, вовлекаются раньше азурофильных гранул. Содержимое гранул попадает в нейтральную внеклеточную среду, т.е. в благоприятные условия для проявления активности ферментов и других факторов, содержащихся в специфических гранулах. Азурофильные гранулы содержат ферменты с оптимумом действия в кислой среде, создающейся лишь на пике воспалительной реакции. На этом этапе в окружении нейтрофилов оказыва-ются лизоцим и щелочная фосфатаза. Однако по мере прогрессирования воспаления повышается вклад в дегрануляцию азурофильных гранул и в межклеточной среде воспалительного очага происходит накопление кислых гидролаз и активных форм кислорода.
Все перечисленные факторы задействованы в защите против микроорганизмов. Активные формы кислорода и галоидсодержащие соединения проявляют свой бактерицидный эффект во внеклеточной среде, несмотря на короткий срок существования. Лизоцим, катионные протеазы ( катепсин G, азуроцидин, эластаза), лактоферрин оказывают более сильное антипатогенное действие. Однако эффективность этой защиты во внеклеточном пространстве значительно ниже, чем внутри клетки, где факторы действуют в более высокой концентрации и в тесном контакте друг с другом. Важно отметить, что во внеклеточном пространстве большинство этих факторов проявляет цитотоксическое действие в отношении собственных клеток организма. Продукты дегрануляции и некротической гибели нейтрофилов вызывают «расплавление» тканей в очаге воспаления и образование гноя. В результате дегрануляцию можно рассматривать скорее как побочный эффект, чем как дополнение к внутриклеточному цитолизу.
В то же время ферменты, особенно протеазы, выделяемые из гранул нейтрофилов, вносят существенный вклад в формирование вазоактивных пептидов, играющих важную роль в развитии сосудистой реакции при воспалении. Так, кислые и нейтральные протеазы участвуют в образовании кининов, влияющих на сократимость и проницаемость мелких сосудов. Сериновая протеаза, производимая нейтрофилами, катализирует превращение ангиотензиногена в ангиотензин II, вызывающий сужение крупных
сосудов, что приводит к повышению кровяного давления. Катионные белки обусловливают высвобождение вазоактивных пептидов и гистами-на из тучных клеток и тромбоцитов и вызывают агрегацию последних. Некоторые протеазы способны расщеплять факторы комплемента С3 и С5 с образованием С3а и С5а, играющих важную роль в развитии воспаления. Некоторые вазоактивные пептиды уже содержатся в гранулах нейтрофилов, а при дегрануляции происходит их высвобождение.
Нейтрофилы, завершившие процесс фагоцитоза, погибают (чаще путем апоптоза). Тканевые нейтрофилы быстро подвергаются апоптозу и без осуществления фагоцитарной реакции; фагоцитоз только ускоряет этот процесс. Причина апоптоза в этом случае — повышение проницаемости митохондрий для цитохрома с и фактора Аро-1, формирующих апоптосому, в которой происходит активация каспазы 9. В процессе апоптоза на поверхности нейтрофилов появляется фосфатидилсерин и другие молекулы, распознаваемые мембранными рецеторами макрофагов, что приводит к фагоцитозу апоптотирующих нейтрофилов. Таким образом, макрофаги «очищают территорию» после фагоцитоза. При активации макрофагов в них происходит образование антиапоптотических факторов (Bcl-2 и др.), поэтому они не подвергаются апоптозу после завершения фагоцитоза.
Дегрануляция эозинофилов как основа внеклеточного цитолиза
[править]Принципиально иную функцию имеют факторы, выделяемые во внеклеточную среду при дегрануляции эозинофилов. Эти клетки играют
основную роль в защите от слишком крупных для фагоцитоза патогенов — прежде всего от многоклеточных паразитов.
В специфических (крупных) гранулах преобладают 4 главных белка: главный щелочной белок (MBP), присутствующий в сердцевине
гранулы в виде кристаллов, и 3 белка матрикса — эозинофильный катионный белок (ECP), эозинофильная пероксидаза (ЕРО) и нейротоксин, происходящий из эозинофилов (EDN). При дегрануляции кристаллический МВР переходит в растворимую форму. Все перечисленные белки участвуют в повреждении клеток макропаразитов. Белки ECP и EDN обладают также рибонуклеазной активностью и оказывают противовирусное действие. Определенный вклад в антипатогенный эффект эозинофилов вносят минорные составляющие гранул — ферменты (присутствующие в специфических гранулах — миелопероксидаза, коллагеназа, эластаза, β-глюкуронидаза, катепсин, РНКаза; присутствующие в мелких гранулах — кислая фосфатаза, арилсульфатаза, пероксидаза). В то же время белки MBP, ECP, EPO и ферменты гранул повреждают нормальные клетки организма.
Всем названным белкам в той или иной степени свойствена иммунорегуляторная активность, направленная на ограничение воспалительной реакции; она характерна и для эйкозаноидов, синтезируемых в липидных тельцах эозинофилов. Для многих цитокинов, выделяемых эозинофилами по механизму классической секреции (IL-4, IL-5, IL-10, TGFβ, отчасти IL-6), тоже характерно преобладание противовоспалительных эффектов.
Как уже отмечалось, внеклеточный цитолиз менее эффективен, чем внутриклеточный, прежде всего в связи с уменьшением концентрации выделяемых клетками факторов. В случае эозинофилов эта проблема решается благодаря их адгезии к поверхности паразитов, что позволяет обеспечить достаточно высокие концентрации выделяемых веществ. В результате внеклеточный цитолиз, обеспечиваемый факторами, секретируемыми эозинофилами, представляет главный и вполне адекватный механизм иммунной
защиты против многоклеточных паразитов.
Секреторная функция моноцитов и макрофагов
Секреторная активность моноцитов и макрофагов реализуется преимущественно через аппарат Гольджи-зависимый механизм и (в отличие от таковой активности нейтрофилов) играет очень важную роль. Однако дегрануляция фаголизосом тоже выполняет важные функции: таким путем из макрофагов выделяются продукты окислительного взрыва, галоидные производные, азотистые метаболиты, протеазы, кислые гидролазы, участвующие во внеклеточном цитолизе и переваривании убитых патогенов. Дегрануляция моноцитов и макрофагов не сопровождается «расплавлением» тканей, поскольку они выделяют значительно меньше перечисленных веществ, чем нейтрофилы. Дегрануляция макрофагов протекает не взрывообразно, а в значительной степени регулируемо; макрофаги существенно меньше нейтрофилов подвергаются апоптозу.
Цитокины — наиболее важная для реализации и регуляции иммунной защиты группа продуктов, выделяемая моноцитами/макрофагами. Эти клетки секретируют все провоспалительные цитокины — TNFα, IL-1, IL-6, IL-8, IL-12, IL-18, IL-23; все провоспалительные хемокины, интерфероны (в наибольшей степени IFNα, в наименьшей — IFNγ) и колониестимулирующие факторы. Таким образом, моноциты/макрофаги служат источником факторов, определяющих развитие воспалительной реакции и участвующих в большинстве реакций врожденного иммунитета. Кроме того, макрофаги, наряду с дендритными клетками, обеспечивают запуск адаптивного
иммунного ответа, эффекторами которого служат лимфоидные клетки.
Макрофаги секретируют компоненты комплемента (практически все) и эйкозаноиды (простагландины, лейкотриены). Эти клетки вырабатывают гомеостатические факторы, поддерживающие нормальное регулируемое функционирование многих основных систем организма: молекулы межклеточного матрикса (фибрионоген, тромбоспондин, протеогликаны), факторы свертывания крови, значительную часть белков сыворотки крови, в частности, транспортные белки (трансферрин, α2-макроглобулин). Макрофаги
выделяют активные пептиды — провоспалительные (вазоактивные пептиды и т. д.) и регуляторные (гормоны). Факторы, секретируемые макрофага-ми, участвуют в иммунопатогенезе атеросклероза. Эти клетки секретируют липопротеиновую липазу (способствует образованию из липопротеинов низкомолекулярных липидных метаболитов, способных проникать в стенки артерий) и аполипопротеин А. Макрофаги могут участвовать в транспорте поглощенных ими липидных соединений в стенку сосуда.
Макрофаги спонтанно секретируют белки межклеточного матрикса, компоненты комплемента, различные сывороточные белки, факторы липидного метаболизма. При активации макрофагов включаются гены большинства вырабатываемых ими продуктов, а также усиливается продукция некоторых конститутивно синтезируемых веществ (С2, С4, фибронектина). Однако образование макрофагами некоторых веществ (например, липопротеиновой липазы) при активации, наоборот, ослабляется. Моноцитам/макрофагам не свойственно ни характерное для нейтрофилов взрывообразное выделение продуктов, ни характерное для лимфоцитов медленное развертывание секреции. Для экспрессии индуцибельных генов обычно требуется 20-30 мин, а синтез белковых продуктов начинается в пределах 1 часа. Продолжительность экспрессии генов и секреции продуктов макрофагами, как правило, не превышает 1 суток.
Таким образом, секреторная активность свойствена всем миелоидным клеткам, участвующим во врожденном иммунитете. Для гранулоцитов характерна быстрая дегрануляция, обычно сопряженная с внеклеточной микробоцидностью. Для моноцитов/макрофагов характерен регулируемый секреторный процесс, зависящий от аппарата Гольджи; при этом они выделяют множество факторов, обладающих иммунорегуляторной и гомеостатической функцией.
Контактная киллерная активность миелоидных клеток
[править]Реализация миелоидными клетками 2 из 3 основных типов цитотоксичности (внутри- и внеклеточного) описана выше. Нейтрофилы и моноциты/макрофаги относят к «профессиональным» фагоцитам. Фагоцитарная активность в умеренной степени свойствена также эозинофилам, базофилам и тучным клеткам. Внеклеточный цитолиз задействован в антипаразитарной и, возможно, противоопухолевой защите, осуществляемой эозинофилами и нейтрофилами. Для миелоидных клеток также характерен 3-й тип цитотоксичности — контактный цитолиз. Мишенью при этом выступают не столько сами патогены, сколько инфицированные ими клетки.
Обязательное условие контактного цитолиза (как отражено в названии) — установление контакта между клетками, включающего две составляющие: неспецифическую адгезию и рецепторное распознавание. В адгезии участвуют молекулы интегринов, прежде всего β2-интегрин LFA-1 (αLβ2), экспрессируемый на миелоидных клетках. Рецепторами αLβ2 на клетке-мишени служат молекулы суперсемейства иммуноглобулинов — ICAM-1 и ICAM-2. Взаимодействие этих молекул обеспечивает прочное взаимное прилипание клеток. Более специфичное рецепторное взаимодействие основано на распознавании мембранными рецепторами миелоидных клеток молекул опсонинов, представленных на поверхности клетки-мишени. Наиболее характерные лиганды для рецепторов миелоидных клеток — Fс-участки IgG-антител и фрагменты компонентов комплемента (iC3b и др.). В распознавании участвуют в первом случае Fc-, а во втором — СR-рецепторы, широко представленные на поверхности миелоидных клеток (особенно активированных). FcγRI экспрессирован на макрофагах и активированных клетках других типов; FcγRIIA и FcγRIII — на всех разновидностях миелоидных клеток. В результате таких взаимодействий устанавливается прочный контакт между клеткой-эффектором и мишенью.
После формирования контакта в клетку-мишень передается летальный сигнал, приводящий к ее апоптозу. Механизмы киллинга, осуществляемого миелоидными клетками, не выяснены. Очевидно выделение цитотоксических веществ происходит за счет экзоцитоза фаголизосом. Эффективность секретируемых факторов повышается благодаря тесному контакту клеток. Апоптоз могут индуцировать цитокины, секретируемые лейкоцитами (например, TNFα, действующий через рецептор TNFRI на клетке-мишени). В индукции апоптоза участвуют также сигналы, поставляемые в клетку-мишень мембранными индукторами апоптоза (Fas-лигандом, TRAIL) через специализированные рецепторы (Fas-рецептор, DR3, DR4). Контактный цитолиз, осуществляемый доставкой в клетки-мишени цитотоксических веществ типа гранзимов, наименее вероятен, поскольку требует высокой специализации клеток, свойственной естественным киллерам и цитотоксическим Т-лимфоцитам, но не миелоидным клеткам.
Следует, однако, отметить, что контактный цитолиз не служит основным эффекторным механизмом миелоидных клеток при осуществлении ими защитных реакций. Вероятно, это связано с функциональными особенностями этих клеток. Объективная потребность в контактном цитолизе в рамках врожденного иммунитета обусловливает привлечение в эту систему лимфоидных клеток — естественных киллеров.
Эндогенные пептиды-антибиотики
[править]Эндогенные антимикробные пептиды (АМП) представляют собой небольшие молекулы, построенные из аминокислот. Они являются важной составляющей врожденной иммунной системы эукариот, которая обеспечивает защиту против патогенов. АМП эффективны против широкого спектра бактерий,грибов и вирусов.
Действие небольших АМП главным образом приводит к нарушению структуры и функций цитоплазматической мембраны микроорганизмов, что, в свою очередь, ведет к гибели последних. АМП выступают не только в качестве эндогенных антибиотиков, они также играют важную роль в развитии процессов воспаления, поддержании и регуляции адаптивной иммунной системы.
Фагоцитирующие лейкоциты являются центральным клеточным элементом врожденного иммунитета у млекопитающих. В дополнение к образованию токсических свободных радикалов кислорода и окиси азота, лейкоциты используют широкий спектр АМП и белков. Большинство АМП представлено катионными, гранулы-ассоциированными (поли)пептидами с аффинностью к компонентам отрицательно заряженной микробной клеточной стенки. Последние исследования в этой области, включая открытие двух новых семейств АМП (пептидогликан распознающие пептиды и желатиназа-ассоциированный липокалин нейтрофилов), выявили тесную взаимосвязь между кислород-зависимой и кислород-независимой системами и взаимодействие АМП с системой Toll-подобных рецепторов.
На сегодняшний день у человека обнаружено три семейства пептидов-антибиотиков – дефензины, кателицидины и гистатины
Лактоферрин (Lf )
[править]Лактоферрин Lf представляет собой белок трансферринового семейства железосвязывающих белков с м.м 80 kDа.
Этот гликопротеин в основном локализован во вторичных (специфических) гранулах полиморфноядерных нейтрофилов (ПМЯЛ). Кроме того, Lf можно обнаружить в эпителии, разнообразных биологических жидкостях и секретах. Впервые Lf был изолирован из грудного молока. Этот белок является важной составляющей иммунной системы. Lf связывает железо и способен влиять на активность ферментов: ДНКазы, РНКазы, АТФазы, фосфатазы, и гидролизмальто-олигосахаридов. Кроме того, что Lf является естественным антибактериальным, антигрибковым и антивирусным белком, обладает антиоксидантными и иммуномодулирующими свойствами, поддерживает микробаланс в гастро-интестинальной системе.
Lf секретируется нейтрофилами в норме и при воспалении. Концентрация Lf в плазме коррелирует с общим количеством нейтрофилов и уровнем оборота этих клеток. В связи с этим определение данного белка в жидкостях организма может быть использовано в качестве показателя активации нейтрофилов.
В дополнение к антимикробной активности, Lf модулирует функциональную активность некоторых клеток организма. Так, Lf через N-терминальный домен, усиливает фагоцитарную активность нейтрофилов, вероятно, с использованием опсонического и стимулирующего нейтрофилы механизмов. На поверхности ряда клеток выявлены специфические рецепторы для Lf, через которые может реализовываться его иммуномодулирующая активность. В
частности, Lf способен усиливать высвобождение IL-6 и TNF-α из мононуклеарных клеток периферической крови, но при этом ингибирует высвобождение IL-1 и IL-2. Lf модулирует цитотоксичность натуральных киллеров и снижает синтез цитокинов в дерме. Недавно было показано, что Lf способен стимулировать рост костной ткани (в физиологических концентрациях Lf усиливает пролиферацию и дифференцировку первичных остеобластов, и ингибирует остеокластогенез).
Бактерицидный белок, повышающий проницаемость клеток (BPI)
[править]B/PI (САР57, ВР55)— белок (м. м. = 58 kDa) азурофильных гранул. Обладает бактерицидной активностью в отношении грамотрицательных бактерий. Причиной потери жизнеспособности бактерий является повышение проницаемости их внешней мембраны путем деградации пептидогликанов и фосфолипидов. Его избирательность по отношению к грамотрицательным бактериям определяется взаимодействием с ЛПС. LBP и B/PI имеют высокое структурное сходство, благодаря чему, так же как LBP, B/PI связывается с ЛПС, но результат является диаметрально противоположным. LBP повышает чувствительность клеток к ЛПС, a B/PI угнетает распознавание ЛПС . Сходство с B/PI имеет антимикробный катионный белок САР-57 (cationic antimicrobial protein-57). Описана его активность в отношении S. typhimurium, Е. coli, N. gonorrhoeae. Также известен ВР55, который высоко активен в отношении P. aeruginosa. Его активность угнетается ЛПС.
Кальпротектин (MRP8/14 и S100A8/A9)
[править]Кальпротектин (КП) представляет собой гетерокомплекс кальций-зависимых белков. КП высвобождается из нейтрофилов и макрофагов во время
их активации или гибели и вовлекается в активный воспалительный процесс. КП составляет до 60 % цитоплазматических белков циркулирующих ПМЯЛ,
кроме того, он также обнаружен в моноцитах, макрофагах и в илеальных эозинофилах. В моноцитах периферической крови этот белок локализован
экстра- и внутриклеточно, в нейтрофилах — только внутриклеточно. КП высвобождается из клеток в очаге воспаления в результате гибели и разрушения ПМЯЛ, что является примером «голокринной секреции». При воспалении КП экспрессируется сквамозным эпителием (от кожи до кишечного эпителия).
КП имеет антибактериальный, антигрибковый, а также иммуномодулирующий и антипролиферативный эффект. Показано, что этот белок ингибирует
рост фибробластов и может индуцировать апоптоз различных типов клеток. Кроме того, он является потенциальным хемотаксическим фактором для
нейтрофилов. Концентрация этого белка в плазме возрастает при заболеваниях, ассоциированных с повышением активности нейтрофилов. При воспалении ЖКТ гранулоциты мигрируют в стенку кишечника.
Дефензины
[править]Дефензины (англ. defensin, от англ. defense — защита) Данные АМП представляют собой небольшие катионные пептиды, которые воздействуют на микроорганизмы путем нарушения проницаемости мембран, образуя ионные каналы. Среди дефензинов (ДН) млекопитающих выделяют две основные группы: альфа- и бета-дефензины. Альфа-ДН (HNP 1-4)
содержатся в азурофильных гранулах нейтрофилов.
Три основных ДН человечека (HNP 1-3) составляют приблизительно 99 % всех АМП данного типа. Они синтезируются только нейтрофилами, что позволяет считать их специфическими клеточными маркерами этих клеток. Активация нейтрофилов при инфекционных и воспалительных процессах приводит к быстрому высвобождению ДН, которые затем обнаруживаются в плазме и других жидкостях организма.
В нормальной плазме обнаруживаетя очень низкийуровень ДН (от неопределяемых величин до 50-100нг/мл), однако в условиях сепсиса одержание ДН может возрасти до 10 мг/мл и даже выше. При определении ДН очень важна осторожность в отборе проб плазмы, так как активация нейтрофилов во время свертывания крови, также как и долгое хранение крови с антикоагулянтом приводит к высвобождению ДН. В дополнение к микробицидному действию альфа-ДН проявляют также хемотаксическую, иммуномодулирующую и цитотоксическую активность, вносят вклад в общую защиту организма и развитие процессов воспаления. Совсем недавно была открыта антивирусная активность некоторых ДН. Считается, что альфа-ДН вносят серьезный вклад в антиВИЧ-1 активность антивирусного фактора CD8. Это обстоятельство открывает новые возможности в исследовании ВИЧ. Показано, что пациенты у которых отсутствуют альфа-ДН (синдромом недостаточности специфических гранул) страдают частыми и тяжелыми бактериальными инфекциями.
Бета-ДН изначально были открыты в эпителиальных клетках дыхательного тракта. Всего у человека выявлено 9 видов эпителиальных ДН, три из которых относятся к бета-ДН (HBD 1-3). Бета-ДН 1 (hBD-1) экспрессируется у человека конститутивно, в то время как бета-ДН 2 (hBD-2) и 3 (hBD-3) являются индуцибельными пептидами, которые можно рассматривать как одну из неотъемлемых частей врожденного иммунитета и антимикробного иммунного барьера слизистых оболочек. Экспрессия бета-ДН в кишечнике индуцируется провоспалительными цитокинами, а также микроорганизмами (например,E. coli, H. pylori или P. aeruginosa).
Кателицидины
[править]Кателицидины - это катионные амфипатические пептиды разнообразной линейной, α-спиральной или β-шпилькообразной структуры в пероксидаза-отрицательных гранулах нейтрофилов. Появляются кателицидины как результат протеолиза C-конца предшественника белка, содержащего кателиновый домен . У человека имеется только один предшественник кателицидинов, hCAP18, который производится, в основном, в лейкоцитах и эпителиальных клетках. Он расщепляется с образованием пептида LL-37 и целого набора более коротких пептидов с измененными свойствами. Помимо нейтрофилов hCAP18 выявлен в лимфоцитах и моноцитах, в сквамозном эпителии (рта, языка, пищевода, шейки матки и вагины), эпителии легочной ткани, кератиноцитах при воспалительных заболеваниях и эпидидимите. Антибактериальный С-концевой фрагмент hCAP18 - LL37 (37 аминокислот) проявляет антимикробную активность как против грамотрицательных, так и против грамположительных бактерий, грибов, некоторых вирусов и простейших. Этот пептид оказывает синергический антибактериальный эффект с дефензинами. LL37 может связывать липополисахарид и нейтрализовать его способность индуцировать эндотоксический шок. LL37 является важным фактором реэпителизации ран, также была показана его ангиогенная активность invivo и invitro. Более того, LL37 функционирует в качестве хемотаксического агента для нейтрофилов, моноцитов и Т-клеток. У человека кателицидин LL-37/hСАР-18 обнаружен в верхней части крипт толстой кишки. Усиление его экспрессии наблюдается при кишечных инфекциях, он обладает бактерицидным действием.
Секреторный ингибитор протеиназы лейкоцитов (SLPI)
[править]SLPI также известный как антилейкопротеаза (ALP), представляет собой катионный ингибитор эластазы нейтрофилов и, в меньшей степени, катепсина G. Этот белок синтезируется эпителиальными клетками легких, кожи и других органов, а также ПМЯЛ и макрофагами (у мышей). В дополнение к своим ингибиторным свойствам SLPI может участвовать в защите от протеолитических повреждений. Не так давно было показано, что SLPI может проявлять антимикробную и антивоспалительную активность, что, скорее всего, не связано с его способностью ингибировать сериновые протеиназы ПМЯЛ. Было установлено, что SLPI проявляет антибактериальную и антигрибковую активность в тех концентрациях, в которых этот АМП присутствует в мукозных секретах, синтезируемых, в частности, легкими. Предполагается, что SLPI играет важную роль в ингибировании протеин-дисульфидной изомеразы, что очень существенно при инфицировании клеток ВИЧ.
Элафин/SKALP
[править]Элафин относится к эпителиальным ингибиторам протеиназ. Это соединение также известно под рядом других названий, таких как SKALP и эластаза-специфический ингибитор (ESI). Предполагается, что он играет важную роль в регуляции процессов воспаления и в защите от тканевых повреждений в многослойном эпителии. Элафин ингибирует лейкоцитарную эластазу и протеиназу-3 и в дополнение к этому служит субстратом для трансглутаминаз. SKALP конститутивно синтезируется в различных видах эпителия. Элафин также обладает антимикробной активностью против грамположительных и грамотрицательных бактерий. У человека в нормальных клетках кожи элафин отсутствует, однако он быстро индуцируется во время воспалительных процессов, таких, как псориаз и заживление ран. Пре-элафин или Trappin-2 представляет собой 12,3 кДа белок.
Белок, связывающий липополисахариды (LBP)
[править]
Элементы врожденной иммунной системы, распознаю- щие бактериальные ЛПС
LBP представляет собой белок острой фазы с м.м. 58 kDa, который продуцируют гепатоциты и энтероциты. Этот белок прочно связывается с ЛПС и, как было показано, играет важную роль в отношениях между ЛПС и организмом. Известно, что LBP выполняет целый ряд функций. Так, LBP переносит ЛПС на CD14-рецептор мононуклеарных фагоцитов, увеличивая чувствительности этих клеток к данному фактору патогенности в 100-1000 раз. Более того, LBP способен усиливать ответ CD14-негативных клеток путем акселерации связывания ЛПС с растворимым CD14. Образующийся при этом комплекс стимулирует клетки. И, наконец, LBP катализирует взаимодействие ЛПС и липопротеинов, что позволяет эффективно нейтрализовать их биологическую активность. Так, было показано, что LBP предотвращает развитие у мышей септического шока, вызванного ЛПС грам(–) бактерий. Содержание LBP в сыворотке значительно возрастает при травмах, системном воспалительном синдроме, сепсисе. LBP может быть полезным маркером при диагностике и мониторинге острофазных состояний, сепсиса
Гепсидин
[править]Этот АМП, синтезируемый в печени в форме препропептида из 84 аминокислот, секретируется в циркуляцию в форме структурированного пептида из 25 аминокислот. Это соединение участвует в регуляции метаболизма железа в организме. Антимикробный эффект гепсидина обусловлен как воздействием на бактериальную мембрану, так и лишением микроорганизмов доступного железа. Определение концентрации про-гепсидина (гепсидин прогормон) в сыворотке используется для диагностики тяжелых нарушений метаболизма железа.
Эластаза нейтрофилов
[править]Эластаза нейтрофилов(медуллазин) (ген ELA2) — сериновая протеаза, в большом количестве содержащаяся совместно с азуроцидином и протеиназой 3 в азурофильных гранулах. Кроме азурофильных гранул, эластаза также может иметь мембранную локализацию. Эластаза осуществляет протеолиз коллагена типа IV, эластина и других белков внеклеточного матрикса, что происходит при дегенеративных и воспалительных заболеваниях. Эластаза разрушает наружный мембранный белок A (OmpA) поверхности грамотрицательных бактерий, модифицирует функции моноцитов,гранулоцитов, NK–клеток.
Антитела. В-лимфоциты
[править]Основой для понимания природы адаптивного иммунитета являются знания о молекулах, специфически распознающих чужеродные субстанции. Существует три разновидности антигенраспознающих молекул: иммуноглобулины/антитела и TCR двух типов — αβи γδ. Все они существуют в форме мембранных рецепторов лимфоцитов, а антитела — также в виде свободных растворимых молекул.
Антитела
[править]Первыми из антигенраспознающих молекул были открыты антитела, которые к настоящему времени изучены полнее других молекул этой группы. Свойствами антител обладают белковые молекулы, называемые иммуноглобулинами. Таким образом, термин «иммуноглоубин» отражает химическую структуру молекулы без учета ее специфичности к конкретному антигену, а термин «антитело» определяет функциональные свойства молекулы и учитывает специфичность конкретного иммуноглобулина в отношении антигенов (обычно уточняют, к какому антигену направлены антитела, например антитела к бычьему сывороточному альбумину). Как уже отмечалось в главе 1, иммуноглоублины/антитела существуют в 2 формах: мембранной (в составе BCR) и растворимой (собственно антитела).
Антитела были открыты в 1890 г., когда Э. Беринг (E. Behring) и С. Китасато (C. Kitasato) установили, что сыворотки кроликов, которым вводили дифтерийный токсин, приобретали способность нейтрализовать этот токсин и оказывать лечебное действие при дифтерийной инфекции. Иммуноглобулины как разновидность белков были первоначально выявлены методом электрофореза во фракциях сывороточных γ- и β-глобулинов [А. Тизелиус (A. Tiselius), 1937]. Позже они были очищены методами хроматографии и подвергнуты структурному изучению с помощью ограниченного протеолиза [Р. Поттер (R. Potter)] и восстановления дисульфидных связей [Дж. Эдельман (G. Edelman)]. Большой вклад в изучение антител внесли исследования гомогенных опухолевых (миеломных) иммуноглобулинов [С. Мильштейн (C. Milstein)], которые в конечном счете привели к созданию гибридомной технологии [Г. Кехлер (G. Kohler), С. Мильштейн, 1975], позволившей получать моноклональные антитела заданной специфичности. При помощи гибридом можно получать моноклональные антитела необходимой специфичности. Наконец, в конце 1970-х годов С. Тонегава (S. Tonegawa) открыл молекулярные основы формирования разнообразия антигенраспознающей способности антител и описал явление соматической перестройки иммуноглобулиновых генов.
Структура молекул иммуноглобулинов
[править]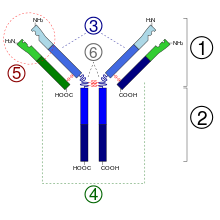
Растворимые антитела и мембранные иммуноглобулиновые рецепторы различаются только строением своей С-концевой части. В этой главе
рассмотрим общие структурные особенности мембранных и растворимых молекул иммуноглобулинов.
Молекулы иммуноглобулинов состоят из двух типов полипептидных цепей — тяжелых(H— heavy) и легких(L— light). Так называемый мономерный иммуноглобулин содержит две Н- и две L-цепи, расположенные симметрично и соединенные дисульфидными связями. Единственная дисульфидная связь, соединяющая Н- и L-цепи, локализуется недалеко от С-конца легкой цепи. Н-цепи скрепляются различным числом дисульфидных связей, о чем будет сказано ниже. Молекулу иммуноглобулина можно разрушить до отдельных полипептидных цепей восстановлением дисульфидных связей дитиотреитолом или меркаптопурином. Легкие цепи содержат 2, а тяжелые — 4-5 гомологичных сегмента — домена. Эти сегменты образованы примерно 110 аминокислотными остатками и имеют сходную пространственную организацию, стабилизированную одной дисульфидной связью, но различные функции. Молекулярная масса L-цепей — 50-60 кДа, Н-цепей — 100—120 кДа, мономера иммуноглобулина — 150—170 кДа.
Во всех цепях N-концевой домен участвует в распознавании антигена. Главную роль при этом играет пространственное соответствие, или комплементарность, антигенраспознающей части молекулы иммуноглобулина с распознаваемым эпитопом. Специфичность иммуноглобулинов определяется первичной структурой антигенраспознающих доменов, называемых вариабельными, или V-доменами (от variable). V-домены тяжелых и легких цепей (VHи VL) участвуют в формировании антигенсвязывающего участка, или активного центра антител.
Структура остальных доменов молекулы иммуноглобулина постоянна. Поэтому их называют константными, или С-доменами (от constant). В состав
L-цепи входит 1 С-домен (СL), Н-цепей — 3 или 4 С-домена (CH1, CH2 и т. д.). С-домены определяют эффекторные функции иммуноглобулинов, не связанные с распознаванием антигена, а предназначенные для взаимодействия с рецепторами клеток, активации комплемента и т. д., что необходимо для реализации эффекторных функций антител.
Протеазы расщепляют молекулы иммуноглобулинов на фрагменты, при этом под воздействием разных протеаз можно получить различные продукты . Так, папаин расщепляет молекулы иммуноглобулинов на 2 типа фрагментов— Fab (Fragment antigen binding) и Fc (Fragment cristallizable). Из молекулы выщепляется два Fab-фрагмента и один Fc-фрагмент. Как следует из названия, Fab-фрагмент сохраняет способность связывать антиген, поскольку содержит активный центр антител (V-домены обеих цепей, CL- и CH1-домены). Fc-фрагмент включает остальные СH-домены, скрепленные дисульфидными связями. Название Fc-фрагмента определило обозначение рецепторов, распознающих «хвостовую» часть антител — Fc-рецепторы. Другой протеолитический фермент — пепсин — расщепляет молекулу ближе к С-концу Н-цепей, чем папаин, — «ниже» дисульфидных связей, скрепляющих Н-цепи. В результате при действии пепсина образуется двухвалентный антигенсвязывающий F(ab’)2-фрагмент и укороченный Fc’-фрагмент.

Выделяют два типа L-цепей — κ и λ, различающиеся строением CL-домена. Строение СН-доменов обусловливает разделение Н-цепей и молекул иммуноглобулинов на изотипы, или классы, первоначально идентифицированные серологически (то есть с помощью сывороточных антител к различным изотипам). Выделяют 5 основных изотипов Н-цепей — μ, γ, α, δ и ε. Каждая молекула иммуноглобулина может содержать Н-цепи только одного изотипа. В зависимости от структуры Н-цепей выделяют 5 классов молекул иммуноглобулинов — IgM, IgG, IgA, IgD и IgE (латинские буквы в названии иммуноглоублинов соответствуют греческим в обозначении изотипов Н-цепей). Иммуноглобулины классов IgG и IgA разделяют на подклассы (субтипы), также в зависимости от особенностей Н-цепей. У человека выделяют 4 подкласса IgG — IgG1, IgG2, IgG3, IgG4 (у мышей — IgG1, IgG2a, IgG2b, IgG3) и 2 подкласса IgA — IgA1 и IgA2. Н-цепи этих подклассов иммуноглобулинов обозначают соответствующими греческими буквами с цифрой (γ1, γ2, γ3, γ4, α1, α2). Иммуноглобулины всех классов могут принадлежать к К- и L-типам в зависимости от присутствия в их составе L-цепей κ- или λ-типов соответственно. У человека соотношение K- и L-типов составляет 3:2.
| Свойство | IgM | IgG | IgA | IgD | IgE |
|---|---|---|---|---|---|
| Молекулярная масса, кДа | 950 | 150; IgG3 — 165 | 150; димер — 300 | 185 | 190 |
| Число мономеров | 5 | 1 | 1 или 2 | 1 | 1 |
| Валентность | 5 | 2 | 2 или 4 | 2 | 2 |
| Изотип Н-цепи | μ | γ | α | δ | ε |
| Число С-доменов в Н-цепи | 5 | 4 | 4 | 4 | 5 |
| Число S-S связей между Н-цепями | 4 | 3–12* | 4 или 5 | 1 | 3 |
| Содержание углеводов, % | 12 | 3 | 8 | 13 | 12 |
| Содержание в сыворотке, мг/мл | 1,5 | 13–14** | 3,5*** | 0,03 | 0,00002 – 0,0005 |
| Срок полужизни, сут | 5–10 | 23; IgG3 — 7 | 6 | 3 | 2 |
| Скорость синтеза, мг/кг в сутки | 7,9 | 34 | 66 | 0,4 | 0,0016 |
| Активация комплемента | Классический путь | Классический путь (кроме IgG4) | - | - | - |
| Клетки, связывающие иммуноглобулин через FcR | - | Макрофаги/ моноциты, нейтрофилы | Макрофаги/ моноциты, нейтрофилы (слабо) | - | Тучные клетки, базофилы |
| Функции | Мембранный рецептор. Первичный иммунный ответ | Вторичный иммунный ответ; защита от бактерий и вирусов | Преобладающий класс в секретах слизистых оболочек | Мембранный рецептор | Реагины; защита от паразитов |
* — IgG1 — 3; IgG2 — 5; IgG3 — 13; IgG4 — 3.
** — IgG1 — 9; IgG2 — 3; IgG3 — 1; IgG4 — 0,5.
*** — IgA1 — 3; IgA2 — 0,5.
Домены иммуноглобулинов представляют собой глобулы, образованные двумя слоями, содержащими несколько β-складок. В С-домене β-слои содержат 4 и 3 β-складки, в V-домене — оба слоя состоят из 4 β-складок. Схема взаимного расположения β-складок отражена на рис.

Между слоями есть дисульфидная связь, соединяющая складки В и F и стабилизирующая структуру домена. Аналогичные домены парных полипептидных цепей повернуты на 180° относительно друг друга. Противоположную ориентацию имеют также соответствующие домены Н- и L-цепей. Домены контактируют друг с другом при помощи гидрофобных взаимодействий.
Суперсемейство иммуноглобулинов
Схема строения доменов (два параллельных организованных определенным образом β-слоя, соединенных дисульфидной связью) очень широко распространена в структуре молекул, функционально значимых для иммунной системы, — молекул суперсемейства иммуноглобулинов (IgSF).
По числу и взаиморасположению слоев выделяют домены C- и V-типов. V-тип подразумевает определенный способ взаиморасположения β-складок, а не вариабельность молекулы (свойственная этим доменам только в составе антигенраспознающих структур — иммуноглобулинов и TCR).
Наиболее древний и простой представитель этого семейства — молекула Thy-1, экспрессируемая у человека в основном на нервных клетках, а у мышей — также на кроветворных клетках и Т-лимфоцитах. Эта молекула содержит единственный домен V-типа. По-видимому, суперсемейство иммуноглобулинов возникло до зарождения адаптивной иммунной системы (об этом свидетельствует наличие молекул с такой структурой у беспозвоночных), но широко использовалось при ее формировании. Наблюдаемое у позвоночных разнообразие членов этого семейства возникло в результате сочетания дупликаций генов с точечным мутационным процессом.
V-домены и антигенсвязывающие участки иммуноглобулинов
V-домены Н- и L-цепей содержат 4 участка с относительно постоянным составом, называемые каркасными участками, и 3 высоковариабельных участка, называемые гипервариабельными. Положение гипервариабельных участков варьирует в различных цепях; оно примерно соответствует расположению 25–35, 50–60 и 93–102 аминокислотных остатков. Поскольку эти участки играют ключевую роль в распознавании и связывании антигена, их еще называют участками, определяющими комплементарность — CDR (Сomplementarity determining regions).
V-домены могут быть одинаково передставлены в иммуноглобулинах всех классов. По строению каркаса выделяют 3 подгруппы Н-цепей, 3 подгруппы κ-цепей и 5 подгрупп λ-цепей. Каркасная последовательность V-доменов весьма консервативна. Их гомология внутри подгруппы составляет 85–90%.
В пространственной структуре V-доменов вариабельные последовательности расположены в зоне изгибов полипептидной цепи, направленной навстречу соответствующим участкам V-домена другой цепи (т.е. CDR H- и L-цепей направлены навстречу друг другу). В результате формируется гидрофильный канал, образующий антигенсвязывающий участок (активный центр) иммуноглобулинов. Он представляет собой полость длиной 6 нм и шириной 1,2–1,5 нм (по данным электронной микроскопии). Площадь поверхности, предназначенной для контакта с антигеном, составляет 7,2 нм2. Пространственная структура этой полости, обусловленная строением гипервариабельных участков, определяет специфичность антител, т.е. их способность распознавать и связывать конкретные молекулы на основе пространственного соответствия. Сверхвысокая вариабельность CDR и
активных центров обеспечивает уникальность молекул иммуноглобулинов, синтезируемых В-лимфоцитами одного клона, не только по структуре, но и по способности связывать различные антигены.
В формирование активного центра вносят вклад пространственно разделенные участки Н- и L-цепей. Гипервариабельные участки V-доменов входят в состав активного центра не полностью — поверхность антигенсвязывающего участка захватывает только около 30% CDR. Структура активного центра была первоначально установлена методом мечения по сродству, основанным на регистрации места связывания меченых низкомолекулярных лигандов. Позже многие детали структуры активных центров антител и их взаимодействия с антигеном были установлены с помощью рентгеноструктурного анализа кристаллов молекул антител.
Антигенсвязывающая способность V-доменов Н- и L-цепей по отдельности выражена значительно слабее, чем в составе активного центра. Поскольку мономерные иммуноглобулины содержат по две пары Н- и L-цепей, молекула содержит два антигенсвязывающих участка, что наглядно демонстрируется с помощью электронной микроскопии: при связывании антителами бифункционального лиганда образуются видимые кольцевые структуры.
С-домены, изотипы и антигенные варианты иммуноглобулинов
Как уже говорилось, принадлежность иммуноглобулинов к различным классам и подклассам определяется строением и числом их С-доменов. В состав γ-, α- и δ-цепей входит по 3, а в состав μ- и ε-цепей — по 4 С-домена.
В С-доменах локализовано большинство участков, распознаваемых рецепторами клеток (Fc-рецепторами, С-рецепторами для компонентов комплемента). Так, в домене Сγ2 расположены участки связывания с компонентом комплемента С4b, а также с рецепторами FcγRI и FcγRII. В домене Сγ3 локализован участок связывания с FcγRIII. В связывании C1q участвуют и Сγ2, и Сγ3. Особенности строения домена СH2 определяют скорость метаболизма молекул иммуноглобулинов, т.е. продолжительность их пребывания в циркуляции.
Между доменами СН1 и СН2 располагается участок, различный по протяженности в Н-цепях разных изотипов и не входящий в состав доменов. В связи высоким содержанием остатков пролина этот участок обладает высокой гибкостью, что и определило его название — шарнирный. Именно в этом участке располагаются сайты расщепления иммуноглобулинов протеазами. В нем сосредоточены все дисульфидные связи, соединяющие Н-цепи. Число этих связей варьирует от 1 в молекуле IgD до 13 в молекуле IgG3. Молекула IgG1 содержит 3 дисульфидные связи.
Важный элемент молекул иммуноглобулинов — их углеводная компонента. L-цепи лишены стабильных участков гликозилирования. В Н-цепях они представлены во всех доменах, кроме вариабельного (больше всего в СН2). Число сайтов гликозилирования в иммуноглобулинах разных изотипов различно. Сайты N-гликозилирования (через остатки аргинина) преобладают над сайтами О-гликозилирования (через остатки серина или треонина). Молекулы IgG гликозилированы значительно слабее (углеводы составляют 2–3% массы молекулы), чем иммуноглобулины других классов (12–14%). Молекулярная масса углеводной цепи в составе IgG составляет около 2 кДа. Обычно углеводные цепи имеют основу, образованную остатками маннозы и хитобиозы, и могут содержать две или более «антенн». Хотя углеводный компонент иммуноглобулина не влияет на его специфичность, он стабилизирует функционально важные детерминанты молекулы, обеспечивает взаимодействие с лектинами, определяет особенности катаболизма и т.д. Гликозилирование может существенно влиять на биологические свойства антител. Так, негликозилированные молекулы IgG обладают меньшим сродством к FcγRI, FcγRII и С1q, чем гликозилированные. Дефекты гликозилирования молекул иммуноглобулинов играют важную роль в иммунопатологии.
IgG всех субклассов, а также IgD и IgE представляют собой мономерные молекулы, т.е. содержат по две пары Н- и L-цепей. Растворимые молекулы IgA и IgM формируют полимеры — димер IgA и пентамер IgM. В их состав, помимо классических полипептидных цепей, входит соединительная J-цепь (от joining) массой 15 кДа, связанная с Н-цепью дисульфидной связью.
J-цепь отвечает за стабилизацию полимера. Эта цепь не гомологична Н- и L-цепям (не относится к суперсемейству иммуноглобулинов). Мономерные единицы в IgA и IgM соединяются дисульфидными связями в С-концевой части Н-цепей. Эти связи особенно чувствительны к действию восстановителей. Так, под действием 2-меркаптоэтанола пентамер IgM (константа
седиментации 19S, масса 900 кДа) распадается на мономеры (7S, 150 кДа). В составе присутствующих в секретах молекул IgA (секреторный IgA, sIgA) содержится еще одна цепь — секреторный компонент (SC). Его молекулярная масса — 60 кДа. Традиционно роль секреторного компонента связывают с защитой молекулы IgA от действия протеаз, содержащихся в высоких
концентрациях в пищеварительных и иных секретах. В настоящее время появились данные, свидетельствующие о более разнообразных функциях этого компонента. Секреторный компонент представляет собой часть поли-Ig-рецептора, участвующего в транспортировке молекулы IgA через эпителиальный пласт в слизистых оболочках. Процесс секреции IgA будет подробнее рассмотрен при описании иммунной защиты барьерных тканей.
Роль иммуноглобулинов различных классов в иммунной защите организ-ма различна. Поскольку первыми экспрессируются μ-цепи, в ходе иммунного ответа ранее других начинает секретироваться IgM. Большинство антител при первичном иммунном ответе принадлежит к IgM- классу. IgM-антитела обладают высокой способностью связывать комплемент, агглютинировать и лизировать клетки-мишени. В то же время они обладают относительно низким сродством к антигену, причем оно не возрастает в процессе иммунного ответа (отсутствует созревание аффинитета). Недостаточная функциональная эффективность IgM-антител обусловлена
также отсутствием на эффекторных клетках иммунной системы рецепторов для Fc-части молекулы IgM. Тем не менее роль IgМ-антител в экстренной защите организма на ранних этапах иммунного ответа достаточно велика.
IgG-антитела, на долю которых приходится основная часть антител на поздних этапах первичного и при вторичном иммунном ответе, обладают рядом преимуществ перед IgM-антителами. В то же время субтипы IgG различаются по эффекторным свойствам. Так, IgG1 и IgG3 весьма эффективны в привлечении фагоцитов и киллерных клеток (эти иммуноглобулины распознаются
Fcγ-рецепторами различных типов), а также в активации комплемента. IgG1 составляют более половины всех антител, образующихся при иммунном ответе. Защитная активность IgG2- и IgG4-антител выражена незначительно в связи со слабым взаимодействием с Fcγ- и рецепторами комплемента. Их роль состоит преимущественно в прямой нейтрализации патогенов.
IgG2-антитела чаще всего специфичны к углеводным детерминантам.
IgA — основной иммуноглобулин секретов слизистых оболочек и главный фактор их специфической защиты. Секреторный IgA связывается с поверхностью патогенов, блокируя их адгезию на слизистых оболочках и подвижность. Таким образом, секреторный
IgA участвует в формировании иммунной защиты слизистых оболочек. Назначение сывороточного IgA менее понятно, особенно если учитывать его слабую способность взаимодействовать с Fc-рецепторами и активировать комплемент. Содержание IgD и IgE в сыворотке крови очень низко. IgD экспрессируется в составе BCR; роль IgD в сыворотке крови не установлена. Несмотря на то, что IgE является минорным компонентом сывороточных иммуноглобулинов, он обладает значительной активностью в защите от паразитов. IgE играет ключевую роль при аллергии немедленного типа.
Биохимические свойства иммуноглобулинов
[править]Иммуноглобулины человека по структуре тяжёлых цепей делятся на пять классов. Различия между IgA (с двумя подклассами), IgD, IgE, IgG (с четырьмя подклассами) и IgM определяются Н-цепями, которые обозначаются греческими буквами — для IgA-α, для IgD-δ, для IgE-ε, для IgG-γ и для IgM-μ. L-Цепи имеют только две разновидности (κ и λ). IgM могут существовать в различных формах. Секретируемые IgM состоят из пяти взаимосвязанных димеров, IgA могут быть образованы из одного, двух или трёх димеров. Олигомерные IgM и IgA удерживаются вместе благодаря связывающему J-пептиду (от англ. joining).
Иммуноrлобулин М (IgM)
[править]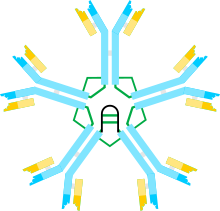
Иммуноrлобулин М (IgM). Белки, представляющие класс антител М. Они первыми, вырабатываются в ответ на острую инфекцию и появляются в кровяном русле обеспечивая первичный иммунитет. Снижение их содержания свидетельствует о дефиците гуморального иммунитета. Увеличение концентрации наблюдается при остром инфекционном процессе различного генеза (вирусные, бактериальные, паразитарные, грибковые заболевания), при острых вирусных гепатитах, аутоиммунных заболеваниях, системной красной волчанке, миеломной болезни, пиелонефрите.
Из всех иммуноглобулинов IgM организован наиболее сложно и имеет наибольший мол. вес — 970 кД. Он состоит из пяти мономеров, каждый из которых включает две тяжелые цепи (мю-цепи) и две легкие цепи (каппа-цепи или лямбда-цепи). Мономеры объединены в единую пентамерную молекулу дисульфидными связями (-S-S-) и J-цепью . Пять мономерных субъединиц расположены радиально. При этом Fc-фрагменты направлены в центр круга, а Fab-фрагменты — наружу. В состав μ цепи входят четыре C-домена (Cμl, Cμ2, Cμ3 и Cμ4), но при этом в структуре тяжелой цепи отсутствует шарнирный участок. В какой-то степени ero функцию выполняет Сμ2 домен, имеющий ocтатки пролина. Предполаraется, что именно этот домен явился эволюционным предшественником шарнирной области γ и α цепей IgG и IgA соответственно. Предпоследний остаток цистеина в хвостовом C-концевом отрезке, содержащем 18 аминокислотных остатков, очевидно, необходим для полимеризации мономеров в пентамер с помощью J-цепи. Каждая молекула IgM содержит только одну J-цепь.
Иммуноглобулин А (IgA)
[править]
1. домены H
2. домены L
3. J-цепь
4. секреторный компонент
Иммуноглобулин А (IgA) является преобладающим изотипом иммуноглобулинов в большинстве секретов слизистых оболочек. Тяжелая цепь IgA1, состоящая из 472 аминокислотных остатка, формирует четыре глобулярных домена: вариабельный VH и константные CНαl (Cαl), СНα2(Cα2), СНαЗ(Cα3), первые два из которых совместно с легкой κ- или λ-цепью формируют антигенсвязывающий Fab-домен, а два последних — константный Fc-супердомен. С-конец α-цепи IgA обоих изотипов, подобно μ-цепи у IgM. Предпоследний остаток Cys471 в составе С-концевого мини-домена любой из двух α-цепей мономера IgA способен ковалентно связываться с J-цепью, что приводит к формированию димерной формы IgA. Разнообразие IgA обусловлено и наличием двух подклассов: IgA1 представлен в основном в мономерной форме, в то время как IgA2 — преимущественно в димерной. Существуют три основные формы IgA:
- мембранный IgA, представленный всегда в мономерной форме и являющийся составной частью антигенраспознающего рецепторного комплекса B-клеток памяти;
- сывороточный IgA, продуцируемый плазматическими клетками в системный кровоток в виде мономеров (monoIgA) и полимеров (pIgA);
- секреторный IgA (SIgA), представленный в секретах слизистых покровов в основном в виде димеров, связанных с секреторным компонентом, являющимся продуктом протеолиза полииммуноглобулинового рецептора эпителия слизистых.
Структурными особенностями SIgA являются наличие в молекуле J цепи и ceкpeтоpнoro компонента. J цепь, как и у IgM, служит для полимеризации молекулы. Молекулярная масса цепи незначительна и составляет около 15 кДа. Данный полипептид не имеет rомолоrии с иммуноrлобулинами, а кодирующий ero reн локализован в хpомосоме, не содержащей reнoв иммуноrлобулинов. На заключительном этапе синтеза J-цепь взаимодействует с COOH-концевым участком тяжелой цепи через сульфидные связи. В результате образуются полимерные формы IgА, представляющие собой в основном димеры, хотя в незначительном количестве имеются и мультимерные молекулы, включающие три мономера и более.
Для IgА, представленноrо в секретах, характерно наличие ceкpeтopнoro компонента. ОН состоит из нескольких родственных в антиrенном отношении полипептидов и экспрессируется на поверхности эпителиальных клеток.
При специфическом взаимодействии димера (IgA)2-J с секреторным компонентом на клеточной поверхности образуется комплекс, который после эндоцитоза перемещается в цитоплазме к апикальной части клетки. Здесь комплекс подверraется действию протеолитических ферментов, что позволяет ему высвобождаться в секреты субэпителиальноrо пространства.
Функционально IgA выступает в качестве первой линии защиты на слизистых поверхностях, препятствуя проникновению вирусов в орraнизм. Хотя IgA не связывает комплемент и в силу этоrо не обладает бактериuидной активностью, он иrрает важную роль в нейтрализации бактериальных токсинов. Кроме тогo, у млекопитающих, включая человека, секреторный IgA хорошо представлен в молозиве и обеспечивает таким образом специфический иммунитет новорожденных.
Иммуноглобулин G (IgG)
[править]
1. FаЬ фрагмент
2. Fc фрагмент
3. легкая цепь (сост. из VH, CH1, шарнир, CH2 и CH3 домены: от N-конца)
4. легкая цепь (сост. из VL и CL домены: из N-конца)
5. рецептор антигена
6. шарнирная область
Иммуноглобулин G (IgG). Среди всех классов иммуноrлобулинов в количественном отношении доминирует IgG. В сыворотке млекопитающих он составляет около 75 % от общеro количества этих белков. Отдельная молекула включает две тяжелые γ цепи и две леrкие: κ или λ типов. Молекулярная масса IgG составляет приблизительно 150 кДа. У человека и мыши описаны по четыре подкласса [gG, которые впервые были обнаружены серолоrическими методами. Тяжелые цепи этих подклассов обозначаются как γl, γ2, γЗ и γ4. Порядковый номер указывает на количественное содержание каждоrо подкласса в сыворотке: в наибольшем количестве представлен IgGγl, в наименьшем — IgGγ4. Степень гомолоrии между разными подклассами человека высока и составляет 90 — 95 %. Различия связаны в основном с шарнирной областью, хотя в C-доменах также встречаются отдельные аминокислотные замены.
Шарнирная область характеризуется значительным числом остатков пролина и цистеина, что определяет ее rибкость. Количество дисульфидных связей этой части молекулы варьирует от одноrо подкласса к друroму. Так, в γl и γ4 цепях таких связей две, в γ2-цепях четыре, а в γ3-цепях одиннадцать. Именно связи S - S обеспечивают взаимодействие двух тяжелых цепей. В γl цепи шарнирная область начинается с 216-ro остатка и заканчивается 231-м. В то же время шарнирная область γ3-цепи на 47 остатков больше по сравнению с γl-цепью. Изучение аминокислотной последовательности позволяет предположить, что это увеличение ocтатков связано с тандемной дупликацией участка 216 −231 γl цепи. Существенной особенностью шарнирной области является возникающая в результате взаимодействия двух тяжелых цепей жесткая, циклическая октапептидная структура:
-Cys - Pro - Pro - Cys - | | -Cys - Pro - Pro - Cys -
Она служит осью вращения всей rибкой шарнирной области, а следовательно, и FаЬ — фраrментов, что необходимо, вероятно, для взаимодействия с антиrеном.
Гомолоrия между γ цепями мыши, относящимися, как и у человека, к четырем подклассам, меньше и составляет 60 — 70 %.
Биолоrическая роль IgG разнообразна. Это и антибактериальная зашита через механизм комплементзависимоrо лизиса микробной клетки, и проникновение через плаценту с той же защитной для развивающеroся зародыша функцией, и «армирование» макрофаroв (цитофильность к макрофаrам), в результате чеrо они становятся цитотоксическими для трансплантатов и опухолей, и участие в повышенной реактивности аллерrическоro типа.
Иммуноrлобулин D (IgD)
[править]Иммуноглобулины D – это мономеры; их содержание в крови составляет 0,03-0,04 г/л или 1% от общего количества иммуноглобулинов; в сутки их синтезируется от 1 до 5 мг/кг, а период полураспада колеблется в пределах 2-8 дней. IgD участвуют в развитии местного иммунитета, обладают антивирусной активностью, в редких случаях активируют комплемент. Плазматические клетки, секретирующие IgD, локализуются преимущественно в миндалинах и аденоидной ткани. IgD выявляются на В-клетках и отсутствуют на моноцитах, нейтрофилах и Т-лимфоцитах. Полагают, что IgD участвуют в дифференцировке В-клеток, способствуют развитию антиидиотипического ответа, участвуют в аутоиммунных процессах.
Тяжелая цепь IgD представлена δ-цепью . У человека δ-цепь включает три C-домена ( Cδ1 , Cδ2 и Cδ3 ) в отличие от IgD мышей, содержащего только два С-домена: Сδ1 и Сδ3. Приводит ли делеция домена Сδ2 к изменению функции IgD мыши, неизвестно. Шарнирная область иммуноглобулинов класса D отличается особой протяженностью (64 аминокислотных остатка - содержащую множество O-гликозидных цепей), и, хотя она в некоторой степени защищена углеводами, возможно, именно благодаря ей IgD по сравнению с другими классами иммуноглобулинов обладает повышенной чувствительностью к протеолитическому расщеплению, а период его полураспада в плазме крови очень невелик (2,8 сут.). Неожиданным оказался тот факт, что почти весь IgD вместе с IgM находится на поверхности лимфоцитов крови . Похоже, они служат антигенсвязывающими рецепторами B-лимфоцитов, и, возможно, что эти антигенные рецепторы могут взаимодействовать между собой, осуществляя контроль за активацией лимфоцитов и супрессией лимфоцитов. Возрастающая чувствительность IgD к протеолизу после связывания с антигеном может объясняться этими функциями.
Иммуноrлобулин E (IgE)
[править]Молекулы IgE ( ε- класс тяжелых цепей) состоят из одной субъединицы. Так же как и в IgM , тяжелая цепь IgE имеет 4 константных домена. IgE представляет собой мономер с мол. весом около 190 кД, включающий две тяжелые цепи ( ε-цепи ) и две легкие цепи ( κ-цепи или λ-цепи ). ε-цепь , как и μ-цепь , содержит пять доменов : один Vε- и четыре Сε-домена : Cε1 , Cε2 , Cε3 и Cε4 . Подклассов IgЕ человека пока не обнаружено.
Концентрация IgE в сыворотке крови невелика, и лишь небольшая часть плазматических клеток слизистых оболочек и дренирующих их лимфоузлов синтезирует иммуноглобулины этого класса. Поэтому неудивительно, что на сегодняшний день обнаружено всего 6 вариантов миеломных IgE, в то время как для IgG известны десятки тысяч случаев парапротеинемии . При подкожной инъекции человеку IgE задерживается в коже на длительное время, вероятно, связываясь с тучными клетками . Взаимодействие с антигеном приводит к дегрануляции тучных клеток и сопровождается высвобождением вазоактивных аминов. Этот процесс обусловливает симптомы сенной лихорадки и бронхиальной астмы при контакте с аллергеном у людей, страдающих аллергией .
Концентрация IgE в сыворотке возрастает при аллергических реакциях немедленного типа. Высокоаффинные рецепторы к Fc-фрагменту IgE находятся на тучных клетках и базофилах . При связывании IgE, фиксированных на мембранах тучных клеток или базофилов, с антигеном происходит высвобождение медиаторов воспаления (сероборан , гистамин). Именно этот механизм лежит в основе патогенеза анафилактических реакций .
Основная физиологическая функция IgE, очевидно, защита внешних слизистых оболочек организма путем локальной активации факторов плазмы и эффекторных клеток благодаря индукции острой воспалительной реакции. Инфекционные агенты, способные прорвать линию обороны, образованную IgA , будут связываться со специфическими IgE на поверхности тучных клеток, в результате чего последние получат сигнал к высвобождению вазоактивных аминов и хемотаксических факторов, а это, в свою очередь, вызовет приток циркулирующих в крови IgG, комплемента, нейтрофилов и эозинофилов. В этих условиях способность эозинофилов повреждать гельминтов, нагруженных IgG, и усиленная продукция IgE в ответ на проникновение этих паразитов в организм будут обеспечивать эффективную защиту. Активность IgE проявляется в развитии аллергических реакций. Данный иммуноглобулин способен взаимодействовать с тучными клетками и базофилами посредством Fc-области и соответствующего рецептора на этих клетках. После образования связи IgE с антигеном (аллергеном) тучные клетки получают сигнал к секреции вазоактивных аминов и других фармакологически значимых соединений, что, собственно, и приводит к развитию аллергической реакции.
Содержание иммуноглобулина E в сыворотке исчезающе мало, но он выявляется на поверхностной мембране базофилов и тучных клеток. Удельный вес этих иммуноглобулинов в аллергических реакциях является доминирующим (например, при бронхиальной астме и сенной лихорадке).
Гены иммуноглобулинов
[править]
Зародышевые гены иммуноглобулинов. У здорового человека В-лимфоциты в течение жизни создают несколько миллионов вариантов антител, связывающих разные антигены (потенциально 1016 антгенов). Никакой геном физически не несёт столько различных структурных генов. Количество наследуемого от родителей генетического материала (ДНК), определяющего биосинтез антител, не так уж и велико — немногим более 120 структурных генов. Это наследуемое множество генов — зародышевые гены Ig (зародышевая конфигурация генов).
С позиций существовавшего в начале 60-х годов постулата — «один ген — одна полипептидная цепь» невозможно было представить, как закодировано такое множество белков. Во всем геноме для этого попросту нехватало генов. В 1965 г. У. Дрейером и Дж. Беннетом была выдвинута гипотеза о том, что вариабельные и константные домены тяжелых и легких цепей иммуноглобулинов кодируются разными генами, то есть для кодирования одной полипептидной цепи используется не один, а два гена. В то время эта гипотеза казалась безумной и недоказуемой. Новые методы исследования ДНК открыли возможность выделять один ген из множества генов, клонировать его, чтобы иметь достаточное количество для анализа, и определять его структуру. В 1976 г. в Базельском институте иммунологии С. Тонегава с сотрудниками исследовали гены иммуноглобулинов, секретируемых миеломой МОРС 321. Тонегава установил, что в генах иммуноглобулинов экзоны соответствуют доменам полипептидных цепей. В ДНК зрелых клеток V- и С-генные сегменты более сближены, чем в эмбриональных. Следовательно, при тканеспецифической дифференцировке В-лимфоцитов происходит перестройка генного материала, в результате которой в разных клетках оказывается разный генетический материал. За это открытие в 1980 г. С. Тонегава был награжден Нобелевской премией.
В незрелых В-клетках или в любых друrих клетках V и C-гены той или иной группы сцепления, находясь на одной и той же хромосоме, удалены друг от друга на значительное расстояние. Подобная нативная локализация генов для иммуноrлобулинов определяется как состояние зародышевой линии (анrл. germline). Oднако по мере созревания В-клеток от некоммитированных предшественников к зрелым формам происходит реоргaнизация генома, так что пространственно yдaленные генные сегменты оказываются в непосредственной близости друг от другa, образуя единый информационный участок. Этот процесс перестройки генетическоrо материала получил название соматической рекомбинации. Он связан только с соматическими клетками (в случае с иммуноrлобулиновыми генами только с В-клетками), не наследуется и, следовательно, не затрагивает половые клетки.
Гены к-цепи
Генный сегмент Vκ включает в себя группу из 250 Vκ-генов, каждый из которых кодирует первые 94-95 аминокиcлотных остатков Vκ-области; при этом часть Vκ-генов потенциально способны функционировать, остальные имеют минорные дефекты или представляют собой псевдогены (функционально неактивные).
Jκ-сегмент кодирует остальную часть V-домена Ig и включает в себя 5 соединительных J-мини-генов, один из которых является псевдогеном. Каждый из работающих J-генов кодирует последовательность из 12-14 аминокислотных остатков и тем самым обеспечивает достройку V-гена до того количества нуклеотидных остатков, которое контролирует синтез полноценной Vκ-области.
Cκ-ген кодирует константный регион легкой κ-цепи . (В геноме человека обнаружен лишь один ген константной области κ-цепи).
В результате рекомбинации ДНК в процессе дифференцировки лимфоидных клеток один из Vк-генов соединяется с одним из J-мини- генов. Объединение этих сегментов ДНК происходит за счет делеции (удаления) последовательности нуклеотидов, входящих в интронную (некодирующую) последовательность между V- и J-генами. Место рекомбинации V-J не является жестко фиксированным: в процессе рекомбинации объединение может происходить как между собственно основаниями V- и J-генов, так и между основаниями, соседствующими с этими сегментами. Подобные "ошибки" вносят дополнительную изменчивость в 3-й гипервариабельный участок V-домена .
Прошедшая (первичная) рекомбинация обеспечивает формирование к-локуса, который состоит из трех экзонов (кодирующих участков):
- L-сегмента, кодирующего короткий сигнальный ( лидерный ) пептид, который состоит из 20-25 аминокислотных остатков;
- рекомбинантного V-J гена и
- С-гена константной области.
Такая рекомбинантная ДНК в коммитированных клетках обеспечивает образование первичного транскрипта - ядерной пре-мРНК . Далее в результате процессинга (созревания пре-мРНК) интронные участки между J- и С-, а также между L- и V-сегментами вырезаются. Таким образом кодирующие последовательности зрелой мРНК (связанной с полирибосомами ) оказываются слитыми в единый информационный участок.
мРНК транслирует полипептид с дополнителным лидерным участком (L) аминокислотных остатков. Предполагается, что лидерный участок, включающий в основном гидрофобные аминокислоты, служит "опознавательным знаком" синтезируемой к-цепи для направления ее в эндоплазматический ретикулум . После прохождения через мембрану эндоплазматического ретикулума он отщепляется, и зрелая к-цепь приобретает, наконец, тот аминокислотный состав, который характерен для секретируемого иммуноглобулина. Далее начинается внутриклеточный процессинг молекулы иммуноглобулина с образованием его секретируемой формы и ее движение по пути выделения из клетки.
Гены λ-цепи
Общая схема рекомбинации генов, кодирующих лямбда-цепи Ig , аналогична рекомбинации генов, кодирующих каппа-цепи . Локус генов легких цепей лямбда-типа также содержит набор V-генов и C-генов, но в отличие от каппа-цепей, каждый C-ген лямбда-типа сопровождается расположенным рядом с ним J-геном. Несмотря на это отличие от локуса каппа-цепей, процесс рекомбинации V-J в локусе лямбда-цепей в общем весьма сходен с аналогичным процессом в локусе к-цепей.
После рекомбинации сегментов V и J между перестроенными VJ-генами и C-геном еще сохраняется интрон (некодирующая промежуточная последовательность). Весь этот отрезок ДНК (от лидерной последовательности до 3'-конца C-гена, включая интроны) полностью транскрибируется в ядерную пре-мРНК (предшественник мРНК), из которой после удаления интронов и соединения экзонов образуется молекула мРНК , способная транслироваться в белок.
Изотипы, аллотипы и идиотипы иммуноглобулинов
[править]Изотипы – это варианты классов и подклассов иммуноглобулинов по тяжелым цепям (у человека 9 изотипов: M, G1, G2, G3, G4, A1, A2, E, D), отражают разнообразие антител на уровне биологического вида
Аллотипы– это варианты иммуноглобулинов в пределах одноименного изотипа, обусловлены генетическим разнообразием внутри вида (аллотипы IgG1, IgG2, IgG3, IgG4).
Идиотип (idious – уникальный) - это вариант уникального антигенсвязывающего участка молекулы иммуноглобулина, который является антигенной детерминантой. Антитела против таких антигенных детерминант называются антиидиотипическими.
B-система иммунитета: общие сведения
[править]Гуморальный ответ в виде продукции антител зависит от функционирования В-системы специфической иммунной защиты.
Центральным органом системы является костный мозг - основное место генерации B-клеток. Клеточный состав представлен B-лимфоцитами различной степени зрелости вплоть до заключительной формы в гистогенезе этих клеток - плазмоцитов , активно синтезирующих и секретирующих специфические иммуноглобулины.
В процессе развития B-лимфоцитов в костном мозге происходит реорганизация генов для синтеза тяжелой и легкой цепей иммуноглобулинов. В результате такой реорганизации одна клетка синтезирует только одну по специфичности тяжелую цепь и одну легкую цепь из множества возможных. Образующийся из такой клетки клон несет иммуноглобулиновый рецептор, способный реагировать только на один антигенный эпитоп.
При этом клоны, экспрессирующие иммуноглобулиновые рецепторы к своим собственным антигенам, уничтожаются и не принимают участия в дальнейшем становлении системы. Создание толерантности к собственным антигенам осуществляется на территории костного мозга. В результате на периферии оказываются клетки, рецепторы которых реагируют только на чужеродные антигены.
Дифференцировка В-лимфоцитов
[править]Весь путь развития В-лимфоцитов от стволовой кроветворной клетки до плазмоцита включает несколько этапов, каждый из которых характеризуется своим клеточным типом. Всего вычленено 7 таких типов:
1) стволовая кроветворная (гемопоэтическая) клетка - общий предшественник для всех ростков дифференцировки лимфомиелопоэза;
2) общий лимфоидный предшественник B-клеток и T-клеток для B- и T-клеточного пути развития - наиболее ранняя лимфоидная клетка, для которой еще не определилось одно из двух направлений развития;
3а) ранняя про-В-клетка - ближайший потомок предыдущего клеточного типа и предшественник последующих, продвинутых в дифференцировке клеточных типов (приставка "про" от англ. progenitor);
3б) поздняя про-В-клетка ;
4) пре-В-клетка - клеточный тип, окончательно вышедший на В-клеточный путь развития (приставка "пре" от англ. precursor);
5) незрелая В-клетка - завершающая костномозговое развитие клеточная форма, которая активно экспрессирует поверхностный иммуноглобулин и находится в стадии отбора на способность взаимодействовать с собственными антигенами;
6) зрелая В-клетка - клеточный тип периферии, способный взаимодействовать только с чужеродными антигенами;
7) плазматическая клетка (плазмоцит) - эффекторная, антителопродуцирующая клеточная форма, которая образуется из зрелой В-клетки после ее контакта с антигеном.
Роль стромы костного мозга Стадии развития от стволовой кроветворной клетки до незрелого В-лимфоцита происходят на территории костного мозга под прямым воздействием стромального микроокружения. Простым доказательством подобного утверждения являются опыты in vitro. Удаление из клеточной культуры стромальных элементов прерывает формирование В-лимфоцитов из стволовых клеток костного мозга. Реконструкция культуры восстанавливает процесс накопления В-клеток.
Участие клеток стромы в дифференцировке В-лимфоцитов проявляется в двух формах. Ранние этапы развития В-лимфоцитов зависят от прямого контактного взаимодействия со стромальными элементами. На более поздних этапах В-лимфоциты испытывают воздействие гуморальных факторов.
Взаимодействие наиболее ранних предшественников В-клеток со стромальными клеточными элементами осуществляется с помощью поверхностных адгезивных молекул.
Первые контактные отношения возникают на уровне стволовой кроветворной клетки и общего лимфоидного предшественника лимфоцитов через взаимодействие между гиалуроновой кислотой клеточной поверхности стромальных клеток и CD44. Это типичный адгезивный белок с относительно небольшим мол. весом 80-95 кД, хорошо представленный на поверхности различных типов лейкоцитов и эритроцитов. Помимо участия в установлении физического контакта между клетками стромы и ранними предшественниками В-клеток, он принимает участие в других формах межклеточных взаимодействий, а также в процессах клеточной миграции и метастазирования. Вероятно, связывание CD44 с лигандом не несет какой- либо прямой сигнальной функции, но стимулирует взаимодействие рецептора c-kit ранних про-В-клеток с другим рецептором стромальных клеток - SCF (англ. stem-cell factor).
Молекула c-kit обладает свойствами тирозинкиназ. В результате связывания этих поверхностных молекул происходит активация c-kit, что влечет за собой усиление пролиферации и переход В-клеточных предшественников на более продвинутый уровень дифференцировки - стадию поздних про-В-клеток.
Этот этап дифференцировки характеризуется появлением на поверхности поздних про-В-клеток рецептора к интерлейкину-7 и включением в процесс этого цитокина , секретируемого стромальными клетками. Активность интерлейкина-7 в качестве ростового фактора вполне достаточна для поддержания пролиферации и выживания развивающихся клеток. В результате их зависимость от SCF снижается и на стадии пре-В-клеток полностью прекращается. Контакт пре-В-клеток со стромой осуществляют адгезины ICAM .
Процесс В-клеточного развития в костном мозге завершается формированием незрелой В-клетки , экспрессирующей поверхностный IgM и подготовленной к миграции на периферию.
Кроме отмеченных, имеется еще целый ряд рецепторов ( СD45R , СD19 , СD38 , CD40 , CD20 , CD21 ), позволяющих следить за развитием В-клеток. Функция этих поверхностных структур не является прерогативой только развивающихся В-клеток. Они включены в процессы клеточного взаимодействия, представления антигена в иммуногенной форме и др.
Дифференцировка, реорганизация генов цепей Ig
Параллельно изменению экспрессии рецепторов в процессе созревания В-клеток в костном мозге происходит реорганизация генов, контролирующих тяжелые и легкие цепи IgМ.
Первыми в процесс реорганизации вступают гены тяжелых цепей Ig. На этапе ранних про-В-клеток начинается слияние D-сегмента и J-сегмента тяжелых цепей иммуноглобулина М . На следующем этапе развития - этапе поздних про-В-клеток - реорганизованный DJ-сегмент вступает в процесс объединения с V-генами. Реорганизация генов тяжелых цепей завершается на этапе пре-В-клеток.
Этот же этап характеризуется синтезом μ-цепей и их экспрессией на поверхности клетки. В ситуации, когда имеется мутация гена μ-цепи иммуноглобулина, препятствующая выходу тяжелой цепи на клеточную поверхность, развитие заканчивается на этапе пре-В-клеток. Вероятно, сам факт присутствия μ-цепи на клеточной поверхности является сигналом к началу синтеза легких цепей .
Таким образом реорганизация генов легких цепей начинается позднее по сравнению с генами тяжелых цепей и происходит только на этапе пре-В-клеток и завершается на заключительном этапе развития в костном мозге - этапе незрелых В-клеток. В результате создаются условия для полноценного синтеза иммуноглобулина М и его экспрессии на клеточной поверхности.
Поскольку реорганизация генных сегментов носит случайный характер, сформировавшиеся иммуноглобулиновые молекулы будут иметь широкую вариабельность по специфичности антигенсвязывающего участка. Причем в процессе такой реорганизации у отдельно взятой клетки будут синтезироваться моноспецифические иммуноглобулины одной, случайно сформированной специфичности.
Интродукция в геном клетки уже реорганизованного гена для тяжелых цепей прерывает процесс собственной рекомбинации генов для этого типа цепей. Все В-клетки таких трансгенных мышей будут синтезировать тяжелую цепь, соответствующую использованному трансгену.
При этом гены легких цепей реорганизуются по заданной программе, обеспечивая широкий набор L-цепей .
Аналогично у мыши, в геном которых интродуцирован реорганизованный ген легких цепей, прерывается процесс реорганизации собственных L-генов. Эти данные лишний раз демонстрируют способность В-клетки производить иммуноглобулины только одной специфичности. Случайность рекомбинационных процессов, обеспечивающих образование реорганизованного гена определенной специфичности, закрывает все прочие потенциально возможные сочетания генных сегментов.
Дифференцировка и селекция в костном мозге
Для завершения дифференцировки В-клеток на последнем этапе их развития в костном мозге , т.е. для трансформации незрелых В-клеток с поверхностным IgМ в зрелые В-клетки периферии, экспрессирующих два иммуноглобулина - IgM и IgD , требуется несколько дней. За это время происходит одно из главных событий в становлении В-системы иммунитета - отбор клеток, реагирующих только на чужеродные антигены .
B-клетки, иммуноглобулиновые рецепторы которых способны взаимодействоать с собственными антигенами, либо погибают в результате апоптоза , либо приходят в состояние ареактивности ( анергии ).
Апоптоз развивается обычно в тех случаях, когда распознавание антигена как "своего" происходит на поверхности клетки.
Распознавание свободного (гуморального) антигена приводит к анергии.
Наиболее четкая информация о реальности такого отбора пришла из опытов с трансгенными мышами. Интродукция в геном мышей реорганизованных генов для тяжелых и легких цепей иммуноглобулинов приводит к тому, что все зрелые В-клетки имеют поверхностный IgM одной специфичности, соответствующей введенным генам.
В тех случаях, когда трансгены, контролирующие синтез антител , специфичных к молекулам I класса MHC определенного генотипа (например, к Н-2Ка ), вводятся мышам иного генотипа ( Н-2Кb ), формирование зрелых В-клеток происходит нормально. Напротив, введение трансгенов той же специфичности сингенным мышам (генотип Н-2Ка ) приводит к нормальному образованию пре-В-клеток , но полностью блокирует формирование незрелых В-клеток , имеющих поверхностные анти-Н-2Ка IgM. Эти эксперименты ясно показывают, что формирование поверхностного IgM , специфичного к собственным клеточным антигенам, является запрещенным событием. Клоны В-клеток, несущих подобные иммуноглобулины, элиминируются посредством апоптоза .
Ситуация несколько меняется, когда незрелые В-клетки распознают растворимые формы антигена. У мышей, которым одновременно интродуцировали гены, контролирующие синтез лизоцима кур, и реорганизованные гены, ответственне за синтез иммуноглобулинов, специфичных к лизоциму, происходит нормальное образование IgM+ В-клеток. Несмотря на присутствие антигенраспознающего рецептора на клеточной поверхности такие В-клетки оказываются арективными к антигену, с которым они познакомились в процессе своего развития.
Фенотипические изменения при дифференцировке
Предшественники B-лимфоцитов обнаружены в островках гемопоэтической ткани эмбриональной печени на 8 -9-й неделе беременности у человека и на 14-й день у мыши. Затем образование B-клеток в печени постепенно прекращается и всю оставшуюся жизнь происходит только в костном мозге . В ходе дальнейшей дифференцировки B-клетки проходят через стадии пре-B- клеток и незрелых B-клеток .
В цитоплазме ранних, быстро размножающихся пре-B-клеток содержатся мю-цепи IgM , но легкие цепи отсутствуют. Боксы показывают время возникновения поверхностных маркеров"). Затем начинают экспрессироваться легкие цепи, и еще не созревшие B-клетки уже имеют рецепторы запрограммированной специфичности в виде встроенных в плазматическую мембрану молекул IgM.
На следующей стадии дифференцировки происходит ориентация клеток на синтез антител определенного класса. Они несут либо поверхностные IgM, либо IgM в комплексе с IgA или IgG . Последующая экспрессия поверхностного IgD означает, что клетка готова к стимуляции антигеном . Некоторые клетки, таким образом, несут поверхностные Ig трех различных классов: M, G и D или M, A и D, но все молекулы Ig на одной клетке имеют одинаковый идиотип и, следовательно, кодируются одними и теми же генами V(H) и V(L) .
После стимуляции антигеном поверхностный IgD утрачивается и у клеток памяти не обнаруживается. На конечной стадии существования полностью зрелой плазматической клетки поверхностные Ig утрачиваются практически полностью.
Способность T-хелперов переключать изотип известна, но могут быть случаи переключения определенных изотипов, не зависящие от антигена и происходящие под действием факторов микроокружения.
На рис. перечислены и другие поверхностные маркеры дифференцировки, в том числе и антигены MHC класса II , экспрессия которых на иммунокомпетентных B-клетках не должна вызывать удивления, если учесть их роль в кооперации с T-клетками.
Существует небольшая популяция B-клеток, экспрессирующая кроме поверхностных Ig и T-клеточные маркеры CD5 ( T1 ) у человека или Ly1 у мыши. Предшественники этой субпопуляции на очень ранних этапах жизни мигрируют из костного мозга в брюшинную полость .
Таким образом, частичное переключение классов синтезируемых иммуноглобулинов происходит под воздействием факторов микроокружения до контакта с антигеном.
Рецептор В-лимфоцитов для антигена(BCR)
[править]
В-лимфоциты, как иммунокомпетентные клетки, с помощью BCR с высокой эффективностью распознают чужеродные антигены и после взаимодействия с Т-хелперами дифференцируются в плазматические клетки, синтезирующие антитела, которые совпадают по специфичности с BCR. Гены BCR и антител организованы сходно с генами TCR, однако существуют различия в формировании их репертуара.
В-лимфоциты, в отличие от Т-лимфоцитов, распознают антигены в нативной форме с помощью клоноспецифичного антигенраспознающего рецептора иммуноглобулиновой природы. Антигены, распознаваемые В-клетками, презентируются высокоспециализированными ФДК, фиксирующими антиген чаще в форме иммунного комплекса. Важная роль в этом процессе отводится рецепторам комплемента, через которые иммунный комплекс фиксируется на соответствующих структурах ФДК. Молекулы HLA в презентации антигена В-лимфоцитам не участвуют.
BCR-комплекс отличается от TCR-комплекса по структуре и числу формирующих его субъединиц. Рецептор образован мономерной формой иммуноглобулинов с коротким цитоплазматическим концом и корецепторными молекулами, участвующими в трансдукции сигнала: Iga (CD79a) и IgP (CD79b). Цитоплазматические концы Iga и IgP содержат мотивы ITAM. Перекрестное связывание поверхностных BCR (антигеном или антителами против иммуноглобулинов) приводит к активации киназ (Fyn, Lyn, Btk и др.), участвующих в проведении активационного сигнала. Киназа Lck соединяется с мотивами ITAM Iga и Igp и передает активационный сигнал в ядро.

Цитоплазматические активирующие последовательности. В цитоплазматических участках Igα и Igβ присутствуют характерные последовательности аминокислотных остатков, называемые иммунорецепторными тирозинсодержащими активирующими последовательностями (ITAM - Immunoreceptor Tyrosine-based Activation Motif); такие же последовательности присутствуют в проводящих сигнал компонентах антигенраспознающего рецептора T-клеток.
Активация B-лимфоцита. Пролиферация и дифференцировка В-лимфоцита может запускаться непосредственно связыванием антигена с BCR. Однако для эффективной активации только через BCR необходима перекрёстная «сшивка» антигеном нескольких BCR. Для этого молекула антигена должна иметь повторяющиеся эпитопы на своей поверхности. В большинстве же случаев для активации В-клетки недостаточно сигнала, поступающего только от BCR, - требуется так называемый второй сигнал, поставляемый активированным Т-хелпером через корецепторы.
Корецепторный комплекс
В дополнительный корецепторный комплекс мембранных молекул, связанных с внутриклеточными системами проведения сигналов, входят, по крайней мере, 3 мембранные молекулы: CD19, CR2 (CD21) и TAPA-1 (CD81).
• CR2 - рецептор для компонентов комплемента. Связывание CR2 с продуктами деградации компонентов комплемента (C3b, C3dg и C3bi), опсонизировавших антиген, вызывает фосфорилирование молекулы CD19, которая в активированном состоянии ассоциирована с Src киназой Lyn.
• CD19. Фосфорилированная молекула CD19 активирует фосфатидилинозит-3-киназу (PI3K) и молекулу Vav (многофункциональная молекула проведения внутриклеточных сигналов), которые усиливают активационные реакции, инициированные BCR .
• TAPA-1 (Target of Antiproliferative Antibody - мишень для антипролиферативных антител) принадлежит к семейству тетраспанинов и в мембране физически примыкает к CD19 и CR2, однако детально роль этой молекулы еще не изучена.
Активация BCR запускает целый ряд каскадов, потенциирование которых зависит от получения дополнительных сигналов с рецепторов цитокинов, TLR и др. Первым шагом является активация тирозин-киназ Lyn, Fyn и Blk (принадлежат к семейству Src-киназ, Fyn и Blk на рисунке не показаны, поскольку они дублируют функции Lyn), а также тирозинкиназ Syk и Btk.
Дальнейшие события проведения сигнала с BCR показаны на рис.. Сигнальные каскады, идущие от антигенраспознающих рецепторов, более подробно описаны на примере TCR.
Молекулы CD79A (Igα) и CD79B (Igβ) образуют соединенный дисульфидными связями гетеродимер, субъединицы которого нековалентно связаны с молекулой иммуноглобулина. Функция гетеродимера состоит в
1) обеспечении экспрессии BCR на мембране,
2) передаче сигнала внутрь клетки и
3) интернализации рецептора (рис.).
До сих пор нет ясности в том, как именно инициируется передача сигнала через BCR. Существует несколько моделей, но наиболее обоснованная из них заключается в том, что активация BCR происходит при их агрегации. Связывание с лигандом двух и более рецепторов приводит к их физическому сближению на мембране. При этом их цитоплазменные концы, связанные с ферментами, оказываются в непосредственной близости. Происходит их фосфорилирование, что дает возможность присоединяться к ним другим молекулам и в итоге приводит к активации внутриклеточного каскада. В отличие от цитокинов и ростовых факторов антигены, активирующие В-лимфоциты, обычно не би-/три-/те- травалентны, а поливалентны. Так, одна бактерия может иметь множество повторяющихся антигенных детерминант на поверхности, с которыми связывается множество BCR, что проводит к сближению и группировке в одном участке цитоплазмы В-лимфоцита большого числа BCR (олигомеризация BCR).
Молекулы CD79A и CD79B передают сигнал одинаково — посредством содержащихся в их цитоплазменных участках иммунорецепторных доменов ITAM. Каждый домен ITAM имеет два тирозиновых остатка. Агрегация BCR после связывания с антигеном приводит к фосфорилированию тирозинов в составе ITAM. Это фосфорилирование осуществляется тремя тирозинкиназами семейства SRC (Src — сокращение от sarcoma): LYN, FYN и BLK . В В-лимфоцитах преимущественно функционирует тирозинкиназа LYN. SRC-киназы прикреплены ко внутренней поверхности мембраны. Они широко распределены и перемещаются по внутренней поверхности мембраны. Сближение цитоплазменных хвостов Igα и Igβ влечет за собой сближение SRC-киназ и фосфорилирование. На этом же этапе происходит и усиление сигнала: SRC-киназы могут связываться с образованными фосфотирозиновыми сайтами, что усиливает их активность.
Итогом этого этапа становится формирование в составе ITAM фосфотирозиновых сайтов, с которыми может связываться ряд других белков, и прежде всего тирозинкиназа SYK. Тирозинкиназа SYK активируется за счет содержащихся в ее составе тандемных (т. е. прилежащих друг к другу) доменов гомологии SRC 2 (SH2). Для ее активации необходимо, чтобы оба тирозина в составе ITAM были фосфорилированы. Это имеет большое значение в механизме анергии. Будучи прикрепленной к ITAM, она фосфорилируется киназами семейства SRC, а также аутофосфорилированием.
SYK передает сигнал через группу белков, связанных с адаптерным белком BLNK. BLNK связан с CD79, но не по ITAM, а в другой области этих молекул. При активации он фосфорилируется и образует каркас для комплекса белков, куда входят SRC-киназы, SYK, BTK, VAV1 и фосфолипаза Cγ2. Этот комплекс обозначается как сигналосома. Вся группа удерживается прикрепленной к внутреннему листку цитоплазматической мембраны, поскольку в составе каждого из этих белков имеется домен плекстриновой гомологии, который связывается преимущественно с фосфоинозитол-3-фосфатом мембраны. SYK в сигналосоме фосфорилирует и активирует тирозинкиназу Брутона (BTK). Активная BTK фосфорилирует фосфолипазу Cγ2 (PLCγ2). Фосфолипаза Cγ2 катализирует гидролиз фосфатидилинозитола, содержащегося во внутреннем листке цитоплазматической мембраны, до двух молекул, являющихся вторичными мессенджерами: диацилглицерола (DAG) и инозитолтрифосфата(IP3). IP3 водорастворим. Он поступает в цитоплазму и взаимодействует со своими рецепторами
на эндоплазматическом ретикулуме, что приводит к высвобождению в цитоплазму ионов Са2+. DAG, напротив, гидрофобен и остается у мембраны. DAG связывается с протеинкиназой Сβ (PKCβ), которая активируется в присутствии кальция. Таким образом, оба сигнала (появление DAG и повышение концентрации внутриклеточного кальция) приводят к одному последствию — активации PKСβ. PKCβ фосфорилирует множество субстратов, включая белок CARD11. CARD11 — ключевой сигнальный адаптер, который координирует комплекс, активирующий сигнальный путь NFκB .
Кроме того, DAG активирует белок Ras GPR, и это приводит к активации MAPK-киназного пути (RAS-RAF- MEC), что обусловливает поступление в ядро транскрипционного фактора ERK.
Повышение внутриклеточного кальция приводит к откреплению кальмодулина от кальциневрина. Кальциневрин фосфорилирует NFAT, поступающий в ядро и запускающий свою транскрипционную программу.
Таким образом, сигнальный путь от BCR обусловливает перемещение в ядро ключевых транскрипционных факторов: NFκB, NFAT, Erk, AP-1, которые обеспечивают пролиферацию и выживаемость нормальных и злокачественных B-клеток.
Возвращаясь к проксимальной передаче сигнала через BCR, важным компонентом ее является активация пути PI3K/AKT. SRC-киназы, главным образом тирозинкиназа LYN, фосфорилирует не только CD79A/B, но и молекулы CD19, CD28 и BCAP. Цитоплазменные участки молекул CD19, CD28 и BCAP содержат мотивы YXXM (где Х — любая аминокислота). Эти мотивы и становятся мишенью для LYN. Их фосфорилирование создает сайты для связывания фосфоинозитол-3-киназы (PI3K). В свою очередь, PI3K, оказавшись около мембраны, катализирует реакцию превращения фосфатидилинозитол-бифосфата (PIP2) в фосфатидилинозитол-трифосфат (PIP3). Количество продуцируемого PIP3 и продолжительность этой продукции определяют активацию эффекторов PI3K. Как уже отмечалось, с PIP3 связываются белки, образующие сигналосому. Кроме того, с ним связываются эффекторные белки пути PI3K, к которым относятся PDK1, BTK и AKT. Все они соединяются с PIP3 через свой домен плекстриновой гомологии и оказываются у внутреннего листка плазматической мембраны. Связанный с мембраной AKT фосфорилируется белком PDK1 и запускает множество сигнальных путей, определяющих рост, пролиферацию и жизнеспособность клеток]. Из них большое значение имеет путь AKT/mTOR, повышающий синтез белков и липидов и обеспечивающий клетку энергией. Также важно, что AKT связывает BAX и, следовательно, делает клетку устойчивой к апоптозу. Как уже отмечалось, BTK передает сигнал по оси PLCγ–PKCβ–CBM–NFκB.
Негативными регуляторами передачи сигнала через BCR являются трансмембранные рецепторные молекулы CD22, CD5, CD72 и FcγRIIB. Цитоплазменные участки этих молекул содержат мотивы ITIM, которые фосфорилируются тирозинкиназой LYN во время стимуляции BCR. C фосфорилированными ITIM связываются и активируются фосфатазы SHP-1 и SHIP-1. SHP-1 дефосфорилирует множество белков, в т. ч. мотивы ITAM CD79. SHIP-1, а также активируемый другим механизмом белок PTEN служат антагонистами PI3K: они дефосфорилируют PIP3 в разных положениях (PTEN-3-фосфатазы; SHIP-1-5-фосфатаза). Дефосфорилирование различных белков и PIP3 прекращает сигнал. Выключение генов, кодирующих эти белки, приводит к разрушению механизмов толерантности и развитию аутоиммунных болезней. Негативными регуляторами бывают и некоторые липидные фосфатазы. С. Liu и соавт. получены данные о том, что главным негативным регулятором пути BCR может быть N-WASP. Оба пути (и активирующий, и ингибирующий) запускаются тирозинкиназой LYN. Поэтому передача сигнала через BCR — результат не вполне изученного баланса между активирующими и ингибирующими молекулами.
Тоническая передача сигнала через BCR
В отличие от активной антигензависимой формы передачи сигнала через BCR, который инициируется в герминативном центре, зрелые B-клетки используют его особым образом, известным как тоническая или базальная передача сигнала BCR. Этот процесс определяет жизнеспособность B-клеток, когда они не связаны с антигеном. Незрелые В-лимфоциты, покидающие костный мозг, завершают свое созревание в периферических лимфоидных органах, где дифференцировка в разные субпопуляции В-клеток определяется различным микроокружением (селезенка, лимфатический узел, плевральная и перитонеальная полости). Большинство В-клеток, покидающих костный мозг, не встречает антиген и рециркулирует между кровью и фолликулами. Их жизнеспособность определяется именно тонической стимуляцией BCR. Если они контактируют с антигеном, то получают дополнительные сигналы через цитокиновые и костимуляторные рецепторы, что ведет к активации и клональной экспансии.
Доказательства существования тонической передачи сигнала через BCR были получены в экспериментах с кондициональной инактивацией IgM или CD79A в зрелых мышиных B-клетках. В эксперименте, проведенном группой K. Rajewsky, можно было выключить экспрессию BCR в В-лимфоцитах трансгенных мышей в желаемое время с помощью сайт-специфической рекомбинации (рекомбинации Cre-Lox), которая активировалась интерфероном. При удалении из генома мыши любого компонента BCR В-лимфоциты не будут образовываться вообще, поскольку на каждом этапе созревания В-лимфоцитов тестируется функциональность BCR. Эксперимент позволял выключить экспрессию BCR у взрослых мышей, когда имелся уже большой пул сформированных В-клеток. Таким образом, можно было увидеть, какое значение имеет постоянная передача сигнала в зрелых В-клетках. Выключение BCR приводило к полному исчезновению периферических В-клеток у мышей в течение нескольких недель. Это доказывало, что подобно тому, как созревание В-лимфоцитов зависит от BCR, так и зрелые В-лимфоциты нуждаются в постоянной передаче сигнала через BCR даже в отсутствие контакта с антигеном. В 1997 г. это опровергало один из ключевых постулатов иммунологии, состоявшего в том, что В-лимфоциты постоянно отбираются на функциональность BCR, а нефункциональные клетки удаляются из иммунной системы. Тоническая передача сигнала не зависит от антигенов, поскольку она влияет на все B-лимфоциты независимо от специфичности экспрессируемых ими антител.
Ключевым посредником тонической передачи является PI3K. Трансгенная экспрессия конститутивно активной формы каталитической субъединицы PI3K позволяла зрелым B-лимфоцитам пережить кондициональное удаление BCR. Трансгенная экспрессия других посредников передачи сигнала — IKKβ (ингибитор NFκB киназы β), MAPKK1, RAC1 — ничего не меняла. Прекращение экспрессии BCR приводило к исчезновению В-клеток . Таким образом, ключевым посредником тонической передачи сигнала через BCR является именно PI3K.
Биофизические механизмы тонической передачи неясны. Они могут быть опосредованы белками SYK16 и TC21, которые связаны с ITAM и могут передавать сигнал в отсутствие антигена. PI3K активируется после фосфорилирования CD19, запускаемого BCR. Но следует вспомнить, что она также служит посредником сигналов, поступающих от CD40, TNF и BAFF. Таким образом, существует два варианта передачи сигнала через BCR: активная, возникающая после контакта с антигеном, и тоническая (или базальная), которая происходит вне антигена. Лимфоидные опухоли используют те же механизмы для обеспечения пролиферации и жизнеспособности, что и нормальные лимфоциты.
Стадии лимфопоэза В-лимфоцитов
[править]Дифференцировка B-лимфоцитов из общей лимфоидной клеткипредшественника (потомка СКК) включает несколько этапов и процессов: перестройку генов иммуноглобулинов и интеграцию их продуктов в клеточный метаболизм; экспрессию генов молекул, обеспечивающих проведение сигнала с BCR внутрь клетки; экспрессию генов мембранных молекул, необходимых для взаимодействия с другими клетками (в первую очередь с T-лимфоцитами и ФДК); экспрессию на мембране корецепторных комплексов.
Выделяют 3 главные субпопуляции В-лимфоцитов - В1-, В2(именно эти клетки мы привыкли называть собственно В-лимфоцитами) и В-клетки маргинальной зоны (Marginal Zone B, сокращенно MZB). В1-клетки разделяют на подклассы В1а (CD5+) и B1b (CD5-), сходные по своим свойствам. В1-клетки и В-клетки маргинальной зоны участвуют в формировании первой линии иммунной защиты и служат переходным звеном от врождённого к адаптивному иммунитету. В2-клетки относятся к подсистеме адаптивного иммунитета, являясь основными клетками гуморального иммунного ответа.
B2-лимфоциты
• Этапы B2-лимфопоэза. В лимфопоэзе B2-лимфоцитов выделяют 6 этапов: общая лимфоидная клетка-предшественник → ранняя про-B-клетка → поздняя про-B-клетка → большая пре-B-клет- ка → малая пре-B-клетка → незрелая B-клетка → зрелая неиммунная B-клетка (выходит из костного мозга в периферическую лимфоидную ткань).
♦ Общая лимфоидная клетка-предшественник. Экспрессируется несколько молекул адгезии, обеспечивающих оседлость в течение необходимого периода времени в костном мозгу, среди них VLA-4 (Very Late Activation Antigen-4 - очень поздний активационный Аг 4), лигандом которого на клетках стромы является VCAM-1 (Vascular Cell Adhesion Molecule-1 - молекула-1 адгезии к стенке сосуда).
♦ Ранняя про-B-клетка. Происходит перестройка D-J в генах тяжёлых цепей, причём на обеих гомологичных хромосомах. В этой стадии (помимо молекул адгезии) экспрессируется Рц c-kit (CD117) для первого фактора роста - мембранной молекулы клеток стромы SCF - стволовоклеточного фактора.
Это взаимодействие обеспечивает надлежащее число митозов предшественников B-лимфоцитов, ещё не поделённых на клоны по Рц для Аг.
♦ Поздняя про-B-клетка. Происходит рекомбинация ДНК V-DJ сначала на одной из гомологичных хромосом. Если она окажется непродуктивной, то та же попытка делается на второй гомологичной хромосоме. Если перестройка на первой хромосоме продуктивна, вторая хромосома использована не будет.
- Как только в клетке происходит трансляция полипептида тяжёлой цепи, он экспрессируется на мембране в составе так называемого пре-B-Рц. Его экспрессия транзиторна, но абсолютно необходима для правильной дифференцировки B-лимфоцитов.
- На поздней про-B-клетке также экспрессируются Рц для цитокинов ИЛ-7 и SDF-1, секретируемых клетками стромы и вызывающих пролиферацию и накоплению «полуклонов» B-лимфоцитов (про-B- и больших пре-B-клеток) с уже известной специфичностью по тяжёлой цепи, но ещё неизвестной - по лёгкой. Это тоже увеличивает разнообразие молекул Ig: с одной и той же тяжёлой цепью будет сочетаться больше разных вариантов лёгких цепей.
♦ Пре-B-клетка. Происходит перестройка V-J лёгких цепей (сначала одной из цепей - κ или λ) на одной из гомологичных хромосом. Если продуктивная перестройка не получится с первой попытки, предпринимаются следующие. Клетки, в которых не получилось ни одной продуктивной перестройки в генах тяжёлых и лёгких цепей, погибают по механизму апоптоза - явления, весьма распространённого среди лимфоцитов.
♦ Незрелый B-лимфоцит. Уже экспрессируется дефинитивный BCR состава: L-цепь + μ-цепь + Igα + Igβ.
• Развитие толерантности. На стадии незрелых B-лимфоцитов начинается также развитие толерантности к собственным тканям организма. Для этого предусмотрено три механизма: делеция аутореактивных клонов, ареактивность (анергия) и «редактирование» Рц по антигенной специфичности. Первые два механизма продолжают действовать и по выходе лимфоцита из костного мозга, т.е. при контакте со значительными количествами аутоантигенов.
♦ Делеция клонов. Связывание мембранного Аг незрелой B-клеткой (имеется Аг-распознающий Рц с IgM, но ещё нет Рц с IgD) является сигналом для апоптоза. Таким образом удаляются
B-лимфоциты, несущие Рц, способные связывать белки собственных тканей.
♦ Ареактивность. Связывание незрелого B-лимфоцита с растворимым Аг не приводит к апоптозу, но лимфоцит приходит в состояние анергии, т.е. вместо активации лимфоцита к иммунному ответу блокируется проведение сигнала.
♦ «Редактирование» рецепторов происходит в небольшой части незрелых B-клеток, в которых ещё активны рекомбиназы. В этих клетках связывание IgM в составе BCR на поверхности незрелого B-лимфоцита с Аг является сигналом для запуска нового процесса рекомбинации VDJ/VJ на второй из двух гомологичных хромосом: если «повезёт», новая комбинация не будет аутореактивной.
• Маркёр завершения B-лимфопоэза (образования зрелого неиммунного B-лимфоцита, готового к выходу из костного мозга в периферическую лимфоидную ткань) - одновременная экспрессия (коэкспрессия) на мембране 2-х типов BCR - с IgM и IgD (причём IgD больше, чем IgM).
• Иммуногенез. После распознавания Аг и вступления в иммунный ответ B-лимфоцит проходит в фолликулах периферических лимфоидных органов и тканей ещё две стадии додифференцировки, которые называют иммуногенезом.
♦ Пролиферация центробластов. В фолликулах B-лимфоциты, называемые на этой стадии центробластами, интенсивно пролиферируют, удерживаясь связями со специальными клетками стромы - дендритными клетками фолликулов (ФДК).
о На ФДК экспрессированы необычные Рц для иммуноглобулинов (FcR), способные продолжительное время (дни, месяцы, возможно, годы) удерживать комплекс Аг-АТ на мембране клетки.
о В центробластах происходит возрастание аффинности АТ в отношении своего Аг по механизму гипермутагенеза, так как на этом этапе дифференцировки выживают те из вновь мутировавших B-лимфоцитов, у которых аффинность BCR к Аг на поверхности ФДК выше.
♦ Выбор дальнейшего пути. На второй стадии иммуногенеза происходит выбор: B-лимфоцит становится либо B-лимфоцитом памяти (дифференцированный резерв на случай повторной встречи с тем же Аг), либо плазмоцитом - терминальным продуцентом больших количеств секретируемых АТ заданной специфичности Активированные B-лимфоциты, т.е. получившие информацию о структуре конкретной антигенной детерминанты и сигнал к пролиферации, размножаются и додифференцируются. Совокупность окончательно дифференцированных потомков B-лимфоцита составляет клон плазматических клеток, синтезирующих АТ (Ig) именно к этой и только к этой антигенной детерминанте. Обратите внимание, что в цитоплазме плазматической клетки находится огромное количество синтезирующего белок (Ig) аппарата - гранулярной эндоплазматической сети. На мембране плазмоцита уже нет ни Ig, ни MHC-II, в них прекращается переключение классов Ig и гипермутагенез, а продукция АТ уже не зависит от контакта с Аг и взаимодействий с T-лимфоцитами.
Описанный путь дифференцировки характерен для B2-лимфоцитов, которые давно известны и хорошо изучены. Однако, существует и другая субпопуляция B-лимфоцитов - B1-клетки.
B1-лимфоциты
• Клетки-предшественники B1-лимфоцитов отселяются из кроветворной ткани в брюшную и плевральную полости ещё в эмбриональном периоде, поэтому их пул у взрослых за счёт костного мозга не пополняется.
• Предназначение B1-лимфоцитов - быстрая реакция на «просачивающиеся» в прибарьерные полости инфекционные микроорганизмы из числа широко распространённых.
• АТ B1-лимфоцитов не очень разнообразны, но полиспецифичны. Почти все они относятся к IgM, распознаваемые ими Аг - наиболее распространённые соединения клеточных стенок бактерий.
• Преобладающая часть Ig сыворотки крови здорового человека синтезируется именно B1-лимфоцитами.
Конститутивные иммуноглобулины(нормальные антитела)
[править]Ещё до встречи с каким бы то ни было внешним Аг, в крови и биологических жидкостях организма уже присутствуют так называемые нормальные (конститутивные) иммуноглобулины. У взрослых большинство из них относится к IgG, но есть также IgA и IgM. Эти АТ способны связывать множество Аг (как ауто-, так и экзогенных). Мишенями для нормальных Ig могут быть: другие иммуноглобулины; TCR; молекулы CD4, CD5 и HLA-I; FcγR; лиганды для молекул межклеточной адгезии и др.
Функции нормальных АТ. Есть основания полагать, что нормальные АТ выполняют ряд весьма важных для здоровья организма функций: - «первая линия обороны» против инфекций; - удаление из организма отживших клеток и продуктов катаболизма; - представление Аг для T-лимфоцитов; - поддержание гомеостаза аутоиммунной реактивности; - противовоспалительное действие (нейтрализация суперантигенов; индукция синтеза противовоспалительных цитокинов; аттенуация комплементзависимого повреждения тканей и др.).
Активация В лимфоцитов
[править]В лимфоциты реаrируют на три различных типа антиrенов
1. Тимус-независимые антигены типа I
Некоторые антиrены. такие, как бактериальный липополисахарид, при достаточно высокой концентрации способны к поликлональной активации значительной части популяции В лимфоuитов. т, е. для такой активации антиrенная специфичность поверхностных рецепторов клетки роли не иrрает. При низкой конuентрации подобных антиrенов, не приводящей к поликлональной активаuии. т.е. В лимфоциты, у которых муноrлобулиновые
рецепторы специфичны по отношению к данным антиrенам, будут пассивно фокусировать их на своей поверхности. При этом за счет собственной
митоrенной активности эти антиrены будут стимулировать пролиферацию клеток.
2. Тимуснезависимые антигены типа 2
Некоторые линейные антиrены, медленно pacпадающиеся в орrанизме и имеющие часто повторяющуюся, определенным обрзом орrанизованную детерминанту, например полисахарид пневмококков, полимеры Dаминокислот, поливинилпирролидон, тоже способны непосредственно без участия Т
клеток стимулировать В лимфоциты т. е, относятся к тимус независимым. Они длительное время персистируют на поверхности специализированных макрофаrов краевого синуса лимфатическоrо узла и марrинальной зоны селезенки, Связывание этих антиrенов с антиrенспеuифическими В клетками происходит с высокой авидностью и обусловлено перекрестным взаимодействием антиrенных детерминант с иммуноrлобулиновыми рецепторами .
Тимуснезависимые антиrены обоих типов вызывают преимущественный синтез IgM, и индуцируемый ими иммунный ответ практически не
сопровождается формированием клеток памяти.
3. Тимус зависимые антиrены. Необходимость кооперации с Т хелперами.
Мноrие антиrены относятся к rруппе тимусзависимых; у животных, подверrнутых неонатальной тимэктомии и имеющих мало Т клеток. они либо не вызывают синтеза антител, либо этот синтез очень слаб. Эти антиrены в отсутствие Т лимфоuитов лишены иммуноrенности: они могут быть одновалентными в отношении спеuифичности каждой детерминанты. подвергаться быстрой деrрадаuии фаrоuитирующими клетками, наконец, не обладать собственной митоrенной aктивностью, Связавшись с В клеточным реuептором, они, так же как и гаптены. не способны активировать В
клетку, Вспомним определение гаптена это небольшая молекула. например динитрофенил, которая может связываться с уже имеющимся антителом или поверхностным реuептором на спеuифической В-клетке, но не способна стимулировать продукцию антител, т. е. caму В клетку, Как уже отмечалось, гаптены приобретают иммуноrенность при соединении с подходящим белком-носителем, В настоящее вpeмя известно, что функция носителя заключается в стимуляции Т-хелперов, помогающих В-клеткам реагировать на гаптен, стимулируя последние дoполнительными сиrналами.
Процессинг антигена в В клетках
Необходимость ковалентной связи гаптена с носителем заставляет предполаrать, что Т хелперы должны распознавать детерминанты носителя
на поверхности реаrирующей В-клетки. Лишь в этом случае они cмогут rенерировать соответствующие дополнительные стимулирующие сиrналы. Однако, поскольку Т-клетки распознают связанный с мембраной процессированный антиген в комплексе с продуктами мне, Т-хелперы не могут распознать нативный антиrен, просто присоединенный (непроцессированный) к иммуноrлобулиновому рецептору В-клетки. Парадокса тут, однако,
нет, поскольку В-клетки могут презентировать антиген Т-хелперам. На самом деле они могут выполнять эту функцию при гораздо меньшей концентрации антигена, чем обычные презентирующие клетки, поскольку они могут фокусировать антиген на поверхностных рецепторах, Таким образом. они должны иметь возможность «процессировать» антиген, и в настоящее время считают, что антиген, связавшийся с поверхностным Ig, попадает в эндосомы вместе с молекулами МНС класса II, а затем вновь возвращается на поверхность клетки в процессированной форме, Он accoциирован с молекулами МНС класса II и доступен для распознавания специфическими Т-хелперами. Теперь понятна необходимость ковалентной связи гаптена с носителем, Из-за наличия гаптепа носитель процессируется в В-клетках, запроrраммированных на синтез антител к гаптену. После стимуляции Т-хелперами, распознающими процессированный носитель, этим клеткам действительно удается выполнить свою проrрамму и производить антитела, реаrируюшие с гаптеном.
Пролиферация клона обеспечивается Т-клеточными растворимыми факторами
Тимус-независимые поликлональные активаторы стимулируют деление В-клеток, взаимодействуя не с иммуноrлобулиновыми рецепторами, а с дрyrими структурами поверхностной мембраны. Тимус-независимые антиrены типа 2, по видимому, вызывают деление В-клеток как за счет пе
peкpecтнoгo связывания иммуноrлобулиновых peцепторов, так и с помощью вспомоrательных факторов, выделяемых макрофаrами, Здесь мы обсудим Т-зависимый иммунный ответ, который отличается большим разнообразием изотипа антител, аффинности их поверхностных рецепторов, более продолжительной памятью и большим размером клона. Первыми начинают делиться Т-хелперы, на поверхности которых экспрессируются высокоаффинные рецепторы к ИЛ-2, Эти клетки пролиферируют в ответ либо на собственный ИЛ-2, либо на ИЛ-2, продуцируемый дрyrой субпопуляцией Т-хелперов. Т-лимфобласты тоже выделяют мноrочисленные растворимые факторы (лимфокины), влияющие на дифференцировку мноrих типов клеток: В-клеток, предшественников цитотоксических Т-клеток, макрофаrов, эндотелиальных клеток и др. По этой причине их часто называют индукторными клетками, Однако мы оrраничимся pacсмотрением процесса экспансии активированных В-клеток. Эти клетки обладают поверхностными рецепторами к BSF- 1, который, помимо активации В-клеток в фазе G0 может действовать и как ростовой фактор. Раньше ero называли BCGF-1(от анrл. B cell growth factor), т, е. фактор роста В-клеток 1. В присутствии высоких локальных концентраций BSF- 1, продуцируемоrо прилежащими Т-клетками или дрyrими Т-клетками, находящимися поблизости, отмечается пролиферация В-клеток. Их дальнейшая клональная экспансия стимулируется друrим ростовым фактором, BCGF II . В некоторых экспериментальных условиях in vitro ИЛ-2, γ-ИФН и ИЛ-1 действуют синерrично с описанными выше ростовыми факторами В-клеток, но то, какую роль они играют в физиолоrических условиях in vivo, до сих пор вызывает споры.
Т-клеточные факторы, обеспечивающие созревание эффекторных клеток
После клональной экспансии дифференцировочные факторы обеспечивают созревание В-лимфобластов в клетки с эффекторными функциями. Фактор дифференцировки В-клеток BCDFγ(от анrл, B cell difТerentiation factor) ускоряет образование плазматических клеток с высоким уровнем
секреции IgM, BCDFy вызывает переключение синтеза с IgM на IgG, а также индуцирует те изменения, которые необходимы для обеспечения
высокой скорости синтеза и секреции антител. До сих пор неизвестен молекулярный механизм образования клеток памяти и обусловливающий высокую частоту мутаций V-гeнoB Ig. Известно, что эти процессы происходят в зародышевых центрах вторичных фолликулов.
Заключение
[править]Т-лимфоциты. Главный комплекс гистосовместимости
[править]Т-клетки — разновидность лимфоцитов, основные этапы развития которых проходят в тимусе, что и определило их название (тимусзависимые, или Т-лимфоциты). Для них характерен определенный способ распознавания антигенов (большинство Т-клеток распознает комплекс антигенов с молекулами MHC) и участие в реализации иммунного ответа в качестве исполнительных и регуляторных клеток.
Т-лимфоциты морфологически неотличимы от В-лимфоцитов. Эти клетки дифференцируют по экспрессии на их поверхности маркерных молекул. Общий маркер для всех разновидностей этих Т-лимфоцитов, отсутствующий у других клеток, — молекулярный комплекс TCR–CD3. Как уже упоминалось, этот комплекс включает антигенраспознающий димер TCR и вспомогательный молекулярный комплекс CD3. Выявление CD3 — константных молекул, общих для всех разновидностей Т-лимфоцитов — применяют для идентификации Т-клеток (моноклональные анти-CD3-антитела обычно распознают ε-цепь этого комплекса).
Дифференцировка Т-лимфоцитов
[править]Дифференцировки лимфоцита Т состоит в в экспрессии антигенраспознающего рецептора и необходимых дополнительных сервисных молекул,чтобы факт распознавания антигена имел действенные последствия, направленные на санацию организма от мешающих антигенов. Эти сервисные молекулы(мембранные,а также секретируемые цитокины) обеспечивают взаимодействие Т-лимфоцитов с другими клетками организма.
Антигенраспознающий рецептор Т-лимфоцитов обозначают TCR(T-cell receptor). TCR является гетеродимером—состоит из двух равновеликих полипептидных цепей.У млекопитающих известно две разновидности пар цепей в TCR. В одной паре цепи обозначают а и β,соответствующие Т-лимфоциты — Ταβ. Вторая пара цепей — γ и δ соответствующие Т-лимфоциты обозначают Tγδ. Каждый индивидуальный Т-лимфоцит несет какой-либо один вариант рецептора — либо αβ, либо γδ.
В отличие от иммуноглобулинов TCR исключительно трансмембранные молекулы, т.е. Т-лимфоцит всегда работает собственным «клеточным телом». Т-лимфоциты предназначены для распознавания поверхностных структур собственных клеток организма. Если что-то на поверхности своих клеток будет «раздражать» Т-лимфоцит (например,примесь вирусных пептидов), то он постарается организовать уничтожение поврежденной клетки.
Т-лимфоцит распознает ("связывается" с) комплекс MHC-I или МНС-II с неким пептидом, который и есть антиген в общем понимании. Один определенный участок молекулы TCR вступает в химическую связь с молекулой MHC-I / MHC-II, второй участок того же TCR в тот же момент времени вступает в связь с пептидом-антигеном. Этот феномен называют двойным распознаванием.
Подавляютцее большинство Т-лимфоцитов с рецептором TCR αβ не распознают свободные нативные антигены(еще раз подчеркнем отличие от иммуноглобулинов, которые как раз умеют работать с нативными антигенами в том виде,в каком «судьба забросила» их во внутреннюю среду организма или даже на слизистые оболочки). Другие клетки должны каким-то образом пропустить антиген через себя и выставить его на своей мембране в комплексе с MHC-I/II, чтобы Т-лимфоцит «обратил на антиген свое внимание». Это и есть феномен представления антигена (или, как иногда говорят, транслитерацией с английского—презентации антигена) Т-лимфоциту. Какие клетки в организме способны быть антигенпредставляющими и механизмы этого процесса мы разберем в отдельном разделе, здесь лишь отметим строгую необходимость представления антигена Т-лимфоциту другими клетками.
Строение рецептора Т-лимфоцитов для антигена (TCR)
[править]
Раскрытие природы антигенраспознающего рецептора Т-клеток (TCR) оказалось одной из наиболее трудных задач за всю историю иммунологии. Несмотря на целенаправленные исследования с конца 60-х годов ХХ века, эта задача была разрешена только в начале 80-х годов, когда совместными усилиями нескольких исследовательских групп, использовавших моноклональные антитела, специфичные к клонам Т-клеток, были идентифицированы 2 полипептидные цепи (α и β), входящие в состав основного типа рецептора Т-клеток для антигенов. Рецептор стали обозначать как TCR (T-cell receptor), или αβTCR. К концу 80-х годов было открыто еще две развновидности полипептидных цепей (γ и δ), образующих другой тип TCR — γδTCR. Еще до открытия полипептидных цепей ТСR был описан комплекс молекул CD3, который оказался связанным с TCR обоих типов. Они непосредственно не участвуют в распознавании антигенов, но несут сигнальную функцию.
Димеры αβ и γδ
[править]TCR представляет собой гетеродимерный белок, состоящий из двух субъединиц — α и β либо γ и δ, представленных на поверхности клетки. Субъединицы закреплены в мембране и связаны друг с другом дисульфидной связью.
По своей структуре субъединицы TCR относятся к суперсемейству иммуноглобулинов. Каждая из субъединиц образована двумя доменами с характерной иммуноглобулиновой укладкой, трансмембранным сегментом и коротким цитоплазматическим участком.
Димеры αβ и γδ — собственно антигенраспознающая часть TCR. Они имеют аналогичное строение и молекулярную организацию. Полипептидные цепи, входящие в состав TCR, принадлежат к суперсемейству иммуноглобулинов. Димеры TCR организованы значительно проще, чем иммуноглобулины. Цепи TCR по строению сходны с L-цепями иммуноглобулинов. Каждая цепь TCR имеет 2 внеклеточных домена, один из которых вариабельный, а другой (расположенный ближе к мембране) — константный. Домены содержат 87-113 аминокислотных остатков.
Гомология полипептидных цепей TCR и иммуноглобулинов невелика, но они имеют сходную доменную организацию. Домены цепей TCR образованы двумя β-слоями. В константном домене они содержат 4 и 3, а в вариабельном — по 4 β-складки. Во всех типах полипептидных цепей TCR в каждом из двух доменов содержится по одному участку гликозилирования. В отличие от L-цепей, полипептидные цепи TCR являются мембранными молекулами, имеющими трансмембранный (10-12 аминокислотных остатков) и короткий цитоплазматический (3-5 аминокислотных остатков) участки. Цепи скреплены дисульфидной связью, расположенной непосредственно над клеточной мембраной в шарнирном участке молекул. Трансмембранные отделы цепей связаны друг с другом за счет противоположных электрических зарядов. Цепи димера (αβ или γδ) связаны с полипептидными цепями комплекса CD3, также нековалентно, на основе электростатических взаимодействий (при участии лизина в TCR и аспарагиновой кислоты в CD3).
В V-доменах TCR, как и в V-доменах иммуноглобулинов, есть 4 каркасных участка с относительно постоянной аминокислотной последовательностью и 3 — CDR. Особенно высокая вариабельность свойственна CDR3.
Гипервариабельные участки двух цепей формируют антигенсвязывающую полость TCR. Как и в иммуноглобулинах, выделяют несколько семейств V-доменов TCR, различающихся строением каркасных последовательностей.
В отличие от антител, распознающих эпитопы свободных антигенов, αβTCR распознает пептидные фрагменты антигенов, встроенные в молекулы MHC. При этом антигенный пептид взаимодействует с наиболее вариабельным CDR3, а прилежащие участки молекулы MHC — с CDR1 и CDR2 . Для распознавания необходимо сохранение димерной структуры рецепторов, тогда как изолированные пептидные цепи не способны распознавать антиген. β-Цепи константных доменов полипептидных цепей TCR, относящиеся к различным семействам, различаются по способности связывать суперантигены. Растворимые формы TCR не образуются. Растворимые молекулы TCR, созданные генно-инженерными методами, не способны распознавать антигены. Антигенсвязывающие участки TCR обладают идиотипической специфичностью, иногда сходной с таковой антител.
В норме на поверхности Т-клетки содержится 30 000-40 000 молекул αβTCR, то есть в 4-5 раз меньше, чем BCR на поверхности В-клетки. TCR, как и CD3, являются абсолютными маркерами Т-лимфоцитов: они экспрессируются только на зрелых Т-клетках. Каждая Т-клетка может нести на поверхности только один тип TCR — αβ или γδ. На этой основе выделяют две главные разновидности Т-клеток, кардинально различающиеся по своим свойствам. Большинство (>95 %) Т-клеток, локализующихся во вторичных лимфоидных органах, циркулирующих в крови и лимфе, имеют рецептор αβ-типа. γδТ-клетки составляют минорную субпопуляцию (1-3 %), представленную преимущественно в барьерных тканях, особенно в слизистой оболочке кишечника, где их содержание достигает 20-30 % от общего числа Т-лимфоцитов.
Комплекс CD3
[править]
Комплекс полипептидных цепей, называемый CD3, выявили в 1979 г. с помощью моноклональных антител. Позже было установлено, что он входит в состав TCR и выполняет сигнальную функцию. Комплекс включает молекулы 4 типов — γ, δ (не путать с γ- и δ-цепями димера TCR), ε и ζ. Димер ζ-цепей в настоящее время выделяют в особый комплекс, имеющий свой CD-номер (CD247). Все цепи, образующие CD3 и CD247, представляют собой трансмембранные белки I типа (ориентированы своей N-концевой частью наружу). Внеклеточные части γ-, δ- и ε-цепей содержат по 1 домену суперсемейства иммуноглобулинов и достаточно консервативны (межвидовая гомология — 70-80 %). Структура доменов стабилизирована дисульфидными связями. Цепи CD3-комплекса связаны между собой, а также с димерами TCR и ζ2 нековалентно. Во внутриклеточной части γ-, δ- и ε-цепей содержится мотив ITAM. К этим цепям примыкает (а при активации клетки формирует прямую связь) тирозинкиназа Fyn. Это свидетельствует об участии цепей комплекса CD3 во внутриклеточной передаче сигналов.
ζ-Цепи не принадлежат к суперсемейству Ig. Они формируют димер, связанный расположенной над мембраной дисульфидной связью. Около 10 % молекул представляют не гомо-, а гетеродимер ζ- и η- цепей (продукт альтернативного сплайсинга гена, кодирующего ζ-цепь). В Т-клетках слизистых оболочек в составе димера выявляют еще один тип цепей — γ-цепь (то есть образуется ζγ-димер), идентичная γ-цепи, входящей в состав FcεR1 и ряда других Fc-рецепторов . ζ-Цепь не имеет участков гликозилирования. Из 143 остатков ζ-цепи только 9 расположены внеклеточно; 22 остатка образуют трансмембранный участок, а 112 — внутриклеточную часть. В ней содержится 3 активационных мотива ITAM, что свидетельствует об очень активном участии молекулы в передаче сигналов. И действительно, ζ-димер, благодаря своей связи с киназой ZAP-70, передает сигнал от рецепторных структур к ферментам и адапторным белкам, направляющим его далее по основным путям внутриклеточной передачи сигнала.
Существует несколько моделей четвертичной структуры TCR-CD3 комплекса . Согласно моновалентной модели, комплекс содержит по одной цепи каждого типа, кроме ε- и ζ-цепей, представленных по две цепи каждая. При этом α-цепь пространственно связана с димером γε , а β-цепь — с димером δε; ζ-димер расположен между α- и β-цепями. В соответствии с бивалентной моделью комплекс содержит 2 симметричных тетрамера состава αβγε и αβδε, между которыми расположен ζ-димер. Последняя модель в большей степени соответствует данным анализа молярного соотношения полипептидных цепей комплекса. В то же время суммарная молекулярная масса такого комплекса составляет около 300 кДа, что превышает ее расчетную (на основе второй модели) величину — 235 кДа.
TCR, содержащие антигенраспознающие димеры αβ и γδ, организованы сходным образом. Полипептидные цепи комплекса CD3 синтезируются в избытке. Их сборка происходит в эндоплазматическом ретикулуме. При этом сначала формируется тетрамер, состоящий из одной γ, одной β и двух ε-цепей, затем к нему присоединяется димер αβ или γδ. В аппарате Гольджи происходит их гликозилирование и полимер перемещается на мембрану, где к нему подсоединяется ζ-димер. Экспрессия CD3 без включения антигенспецифического димера αβ/γδ невозможна и свободный комплекс CD3 остается в цитоплазме.
Гены α- и β-цепей рецептора Т-лимфоцитов для антигена
[править]В геноме человека и млекопитающих выделяют 6 кластеров (скоплений)генов, кодирующих молекулы полипептидных цепей антигенраспознающих молекул — Н-, κ- и λ-цепей иммуноглобулинов и α-, β- и γ- цепей TCR αβ- и γδ -типов . Последовательности, кодирующие δ-цепь ТCR, расположены внутри гена α-цепи, но обычно их рассматривают как отдельный, 7-й генетический кластер. Гены человека обозначают прописными буквами — сначала буквы, обозначающие молекулу, в состав которой входит кодируемая цепь (IG или TR), затем название цепи в латинском эквиваленте (Н, К , L , A и т. д.) и завершает обозначение тип кодируемого участка молекулы (вариабельный или константный — V или C). Например, ген IGHV кодирует вариабельный домен Н-цепей иммуноглобулинов. Гены расположены на четырех хромосомах — 2 (κ), 7 (β, γ), 14 (Н, α, δ) и 22 (λ).

В каждом кластере присутствуют гены, кодирующие константные домены — С-гены (в случае кластера IGH — 9, по числу изотипов Н-цепей). В кластерах присутствуют также V-сегменты, кодирующие не весь вариабельный домен, а только 95-96 аминокислотных остатков, расположенных до участка CDR3. V-сегменты содержат около 300 пар оснований. Число V-сегментов, последовательно расположенных в 5’-части кластера, сильно варьирует — от 3 (в TRDV) до 129 (в IGHV). Некоторые V-сегменты не экспрессируются (псевдогены), так что реальное число кодирующих генов значительно меньше (для IGНV — 45). V-сегменты и C-гены пространственно разобщены. Между ними на значительном расстоянии от V-сегментов расположены короткие сегменты — J (соединительные — от Joining), содержащие 35-50 пар оснований, а в некоторых кластерах (Н, B, D) — также D-сегменты (от Divеrsity). Число сегментов J и D варьирует (J — от 4 до 61, D — от 2 до 12).
Между V-, D- и J-сегментами расположены рекомбинационные сигнальные последовательности (RSS — Recombination signal sequences). С 3’-конца от V-гена расположена консервативная последовательность из 7 нуклеотидных остатков (гептамер) 5’CACAGTG3’, далее — соединительный участок (спейсер), содержащий 12 или 23 основания, и нонамер (5’ACAAAAACC3’). И гептамеры, и нонамеры имеют палиндромные последовательности (при считывании в обоих направлениях они оказываются комплементарными). После участка с «нерегламентированной» последовательностью следует нонамер, участок из 23 или 12 оснований, гептамер и J- или D-сегмент. «Правило 12/23» соблюдается всегда: если правее (на 3’-конце) первого кодирующего участка (например, V) расположен 12-членный спейсер, то левее (на 5’-конце) второго участка (например, J) должен располагаться 23-членный спейсер, и наоборот.
Кластеры генов TCR организованы аналогичным образом.
Приведенное выше строение кластеров рецепторных генов характерно для всех клеток, кроме зрелых лимфоцитов. Описанную конфигурацию
генов называют зародышевой, и V-сегменты, кодирующие V-домен без 3-го гипервариабельного участка, также называют зародышевыми. В зрелых
лимфоцитах эти участки организованы иначе — они содержат зрелый V-ген, кодирующий полный V-домен (образован за счет присоединения к зародышевому V-сегменту одного из DJ-сегментов). Описанные выше упорядоченные участки между сегментами V и DJ удаляются в результате глубокой перестройки структуры генетических кластеров, кодирующих рецепторные гены, называемой реаранжировкой (рекомбинацией) генов. Этот процесс происходит при дифференцировке в каждом лимфоците независимо, что приводит к формированию зрелого V-гена, уникального для данной клетки.
Случайно отобранные V- и DJ-сегменты соединяются, при этом неиспользуемый генетический материал удаляется.
Реаранжировка генов рецепторов лимфоцитов начинается с экспрессии под влиянием дифференцировочных стимулов генов V(D)J-рекомбинационного комплекса . Это комплекс содержит 6 компонентов:
- димер рекомбиназ (экзонуклеаз) RAG-1/RAG-2;
- ДНК-зависимую протеинкиназу;
- ДНК-лигазу IV;
- терминальную дезоксинуклеотидилтрансферазу (TdT), кодирующую нематричный синтез олигодезоксинуклеотидов;
- гетеродимер HMG 1/2;
- гетеродимер Ku70/Ku80.
При наличии сегмента D (гены H-цепи иммуноглобулинов, β- и δ-цепей TCR) сначала происходит перестройка на участке между D- и J-сегментами с формированием тандема DJ. Далее перестройка захватывает участок между V- и DJ-сегментами. В обоих случаях сначала происходит реорганизация пространства между перестраиваемыми участками с помощью RSS. Этот процесс начинается с экспрессии генов RAG. Молекулы RAG-1 и RAG-2 присоединяются к концам последовательностей 12 и 23 соединяемых участков гена. Затем субъединицы RAG димеризуются и происходит сближение связанных с ними участков. Этому способствует комплементарное взаимодействие пар гептамеров и нонамеров, основанное на палиндромности этих последовательностей (см. рис. 3.14). Этот процесс осуществляется с участием гетеродимера HMG1/2. В местах примыкания RSS к кодирующим последовательностям происходит разрыв двух нитей ДНК (он катализируется рекомбиназой RAG), причем не в точно определенной позиции, а с возможными отклонениями в несколько нуклеотидных остатков. Разорванные нити ДНК замыкаются друг на друга. В результате формируется «шпилька», в которой ведущая нить ДНК переходит в комплементарную ей нить . Вырезанный отрезок, содержащий RSS, замыкается при соединении разорванных нитей. В результате формируется кольцевая структура — рекомбинационное вырезанное кольцо (REC — от Recombination excision circle).
На следующем этапе происходит «разрешение» шпилек с обеих сторон от места разрыва: при участии ДНК-зависимой протеинкиназы эндонуклеаза повторно разрывает ДНК, но не на вершине «шпильки», а сбоку, образуемые при этом отрезки ДНК различаются по длине. Более длинная нить разворачивается, и на ней комплементарно достраивается вторая. Описанные события приводят к появлению в составе ДНК новой последовательности, палиндромной по отношению к исходной. Такую последовательность называют «Р-вставка» (от Palindromic). В этот же очень короткий промежуток времени с участием TdT происходит добавление на свободных концах ДНК олигонуклеотида случайного состава. Поскольку синтез этого олигонуклеотида происходит не на матрице ДНК, такой вариант вставки называют N-вставкой (от Nоn-template). Протяженность N-вставок не превышает 20 нуклеотидов (обычно меньше 10). Только после этого происходит воссоединение нитей ДНК с 5’- и 3’-концов. В процессах репарации ДНК участвуют ДНК-лигаза IV, ДНК-зависимая протеинкиназа и димер Ku70/Ku80. На этом процесс реаранжировки конкретного гена завершается. Сформированный зрелый ген может транскрибироваться. После сплайсинга мРНК с нее транслируется белок — цепь иммуноглобулина или молекулы TCR.
Описанные процессы происходят в 3’-концевой части V-гена — в участке, сформированом при участии DJ-сегментов. Эта область соответствует третьему гипервариабельному участку — CDR3. В результате этот участок значительно превосходит по вариабельности CDR1 и CDR2, структура которых при реаранжировке V-генов не изменяется. Программа для соматического гипермутагенеза в генах TCR отсутствует (в отличие от генов иммуноглобулинов).
Описанные процессы повышают вариабельность рецепторных V-генов в разной степени. Во-первых, вариабельность этих генов заложена в их зародышевой конфигурации. При наличии 30-40 вариантов зародышевых V-генов (что соответствует действительности для цепей, образующих TCR αβ-типа и иммуноглобулины) комбинирование V-доменов двух цепей при построении антигенсвязывающего участка приводит к формированию 1000—1500 вариантов клеточных рецепторов (то есть в 1000 раз меньше, чем необходимо для распознавания всего множества антигенов). Комбинация различных зародышевых V- и J- (а для половины цепей — еще и D-) сегментов повышаетэту величину на 1-2 порядка. При этом необходимо учитывать неточную локализацию разрывов цепей ДНК V-, D- и J-сегментов при реаранжировке генов, а также наличие Р- и N-вставок. Наконец, к троекратному увеличению вариабельности приводит смещение рамки считывания в D-сегменте.
По некоторым данным, суммарная вариабельность антигенраспознающих участков достигает для BCR 1012—1017, для TCRαβ — 1016—1019, для TCRγδ — 1012—1017 вариантов. Очевидно, что в полной мере такая вариабельность не может быть реализована (общее число клеток в организме человека составляет 1013—1014, из них менее 1012 — лимфоидные). Реальное число клонов Т-клеток, отражающее число вариантов антигенраспознающих участков TCR, составляет 2,5×107 , что заведомо превышает число объектов распознавания. Таким образом, процесс реаранжировки V-генов успешно решает задачу генерации разнообразия антигенраспознающих структур лимфоцитов.
Большое число потенциально возможных вариантов антигенсвязывающих рецепторов на лимфоцитах является попыткой медленно размножающихся и медленно эволюционирующих видов многоклеточных организмов «угнаться» за изменчивостью сверхбыстро размножающихся и эволюционирующих инфекционных микроорганизмов.
Природа сделала такой шаг — наделила суперизменчивостью в процессе онтогенеза в рамках одного тела единственный гистотип клеток (только лимфоциты) и единственную категорию молекул в этих клетках (антигенраспознающие рецепторы — TCR , Ig) . Лимфоцитарный иммунитет есть у очень небольшого числа видов земных многоклеточных животных, напомним — всего у 1,4 %. Следовательно, 98,6 % видов многоклеточных не имеют лимфоцитарной иммунной системы. Лимфоцитарный иммунитет понадобился для спасения от инфекций особей таких видов животных, которые оставляют единичное потомство — рожают редко и мало детенышей, значит, если не каждому, то большинству надо выжить, чтобы сохранился вид. Лимфоциты со своими рецепторами появились 300 млн лет назад, вероятно, у челюстных рыб (jawed fish).
Корецепторные молекулы Т-лимфоцитов — CD4 и CD8
[править]В процесс распознавания Т-клетками антигена (точнее, комплекса антигенного пептида с молекулой MHC), наряду с антигенраспознающим рецепторным комплексом вовлекаются дополнительные молекулы. Наиболее важные из них — корецепторы CD4 и CD8. Назначение этих молекул состоит прежде всего в повышении сродства рецепторного комплекса к лиганду за счет дополнительного связывания корецепторов с молекулами MHC (отсюда обозначение молекул как корецепторов). Поскольку антигенный пептид может презентироваться Т-клетке в составе молекул MHC, относящихся к двум разным классам — I и II, в распознавании могут участвовать две разновидности корецепторов — CD8 и CD4. Молекула CD8 обладает сродством к MHC-I, а молекула CD4 — к MHC-II. Поскольку на зрелых Т-клетках экспрессирован либо CD4, либо CD8, антигенные пептиды в составе молекул MHC-I распознаются CD8+ Т-клетками, а антигенные пептиды в составе молекул MHC-II — CD4+
Т-клетками. Связывание корецепторов повышает сродство TCR к антигенному комплексу в 100 раз.
СD4 и CD8 — маркеры двух главных субпопуляций αβТ-клеток — соответственно, Т-хелперов и цитотоксических Т-лимфоцитов. Однако эти молекулы экспрессируются не только на клетках названных субпопуляций: CD4 в небольшом количестве выявляют на дендритных клетках и макрофа гах, а CD8 — на естественных киллерах. На незрелых Т-клетках — кортикальных тимоцитах — оба корецептора экспрессируются одновременно (что определяет мембранный фенотип CD4+CD8+). В процессе дифференцировки происходит супрессия гена одного из корецепторов, тогда как второй продолжает экспрессироваться.
Структурно 2 типа корецепторов существенно отличаются друг от друга, хотя оба относятся к суперсемейству иммуноглобулинов. Обе молекулы состоят из трансмембранных полипептидных цепей I типа, причем СD4 — мономер, а CD8 — димер.
Молекулярная масса CD4 — 56 кДа. Внеклеточная часть единственной цепи CD4 содержит 4 иммуноглобулиноподобных домена, из которых 2 построены по типу V-, а 2 других — по типу С-доменов иммуноглобулинов. Наружный домен содержит участок, отвечающий за взаимодействие с молекулами MHC-II. В этом же домене расположен рецепторный сайт для вируса ВИЧ-1 (остатки 31-57 и 81-94 домена V1). CD4 — основной рецептор для ВИЧ, поэтому клетками-мишенями этого вируса служат CD4+ Т-лимфоциты — Т-хелперы, а также макрофаги и дендритные клетки.
Молекула CD8 — димер. На большинстве αβТ-клеток CD8 — гетеродимер, образованный α- и β-цепями, на некоторых Т-клетках, локализованных преимущественно в слизистых оболочках (у человека это исключительно γδТ-клетки) — гомодимер αα. Значение существования двух типов гетеродимеров CD8 не установлено. Обе цепи CD8 сходны по размеру и строению. Их молекулярная масса составляет 34 кДа (α) и 32 кДа (β). Во внеклеточной части цепи гомодимера образуют единственный иммуноглобулиноподобный домен, отделенный от мембраны длинным спейсерным участком. Цепи связаны нековалентно. С молекулой MHC-I взаимодействует α-цепь.
Цитоплазматическая часть и CD4 и CD8 связана с тирозинкиназой Lck (семейство Src). Прочность связи увеличивается при распознавания комп- лекса антигенный пептид-молекула MHC в результате конформационных изменений корецептора. Киназа Lck играет важнейшую роль в передаче активационного сигнала от TCR. Таким образом, CD4 и CD8 участвуют не только в распознавании комплекса антигенного пептида и молекулы MHC, но и выполняют сигнальную функцию.
Еще одна функция корецепторов реализуется в процессе презентации антигена Т-лимфоцитам. Корецепторы вместе с молекулой Lck, в отличие от комплекса TCR-CD3, входят в состав рафтов — структурно-функциональных элементов мембраны, важных для формирования иммунного синапса — временной структуры, обеспечивающей эффективное распознавание антигена Т-клетками и формирование полноценного активационного сигнала. Уже на ранних стадиях активации Т-клеток в процессе презентации антигена между комплексом TCR-CD3 и корецепторами происходит нековалентное взаимодействие, что позволяет корецептору «ввести» рецепторный комплекс в состав рафта, тем самым обусловливая эффективность презентации .
Наряду с проявлением усиливающих эффектов, корецепторы способны передавать супрессорные сигналы при распознавании антигена и последующей активации клеток. Супрессорный эффект проявляется, например, при изолированном перекрестном «сшивании» молекул корецепторов моноклональными антителами. На фоне такого связывания стимуляция через ТСR вызывает апоптоз Т-лимфоцитов.
Дифференцировка Т-лимфоцитов в тимусе. Позитивная и негативная селекция тимоцитов
[править]
При значительном сходстве путей развития В- и Т-лимфоцитов дифференцировка Т-клеток более продолжительна. Это объясняется главным образом особенностями распознающего аппарата Т-клеток, требующего сложной «настройки». Т-лимфоциты — единственные клетки крови, развитие которых не может осуществляться в микроокружении костного мозга — основные этапы дифференцировки они проходят в специальном органе — вилочковой железе, или тимусе. Тимус содержит эпителиальные клетки, отсутствующие в костном мозгу. Они и являются тем уникальным и ключевым фактором микроокружения, который способен обеспечить развитие Т-лимфоцитов.
Миграция в тимус клеток-предшественников
[править]Развитие дважды отрицательных тимоцитов и перестройка генов T-клеточного рецептора
[править]DN1 стадия
[править]Самые ранние CD44+CD25- тимоциты локализуются в перимедуллярной зоне коры тимуса. Они представляют собой полипотентные кроветворные предшественники, их V-гены имеют зародышевую, т.е. неперестроенную конфигурацию. Только в некоторых клетках на этой стадии проходит начальный, малоспецифичный этап перестройки генов — сближение сег-ментов D и J в генах β- и δ-цепей. На стадии DN1 клетки интенсивно пролиферируют (до 10 делений), что приводит к 1000-кратно-му увеличению их числа. Это наиболее продолжительный этап развития Т-клеток (10 сут — 50% времени развития Т-клеток в тимусе). Основной ростовой фактор на этом этапе — SСF (С-Kit лиганд). В это время рецептор для IL-7 экспрессирован слабо или вообще не экспрессирован. Факторами дифференцировки на этом этапе развития служат Wnt и Hedgehog, а также Notch, коммиттирующий клетки-предшественники к дифференцировке в Т-лимфоциты.
DN2 стадия
[править]На стадии DN2 тимоциты перемещаются в сторону наружных слоев коры по градиенту CXCL12, секретируемого эпителиальными клетками наружной коры. Длительность стадии — 2 сут. Клетки продолжают пролиферировать уже преимущественно под действием IL-7 и в меньшей степени — SCF. На этой стадии сигналы от Notch коммиттируют Т-клетки к дифференцировке в различные линии (γδ или αβ) и экспрессируется ген, кодирующий pTCRα, — знак выбора αβ-направления развития. Это коммиттирование становится необратимым только после реаранжировки генов TCR на стадии DN3. Тогда же экспрессируются гены рекомбинационного комплекса.
DN3 стадия
[править]При переходе на стадию DN3 запускается основное событие дифференцировки Т-лимфоцитов — перестройка V-генов TCR. Включение этого процесса является следствием экспрессии в тимоцитах группы дифференцировочных факторов под влиянием эпителиального микроокружения. Для раннего развития Т-клеток необходима экспрессия генов Notch, Runx-1, GATA-3, Ikaros, Gfi1, c-Myb, PU.1, E2A/HEB, TCF-1. Особенно важную роль играют факторы семейства Notch (особенно Notch-1 и Notch-3), действующие почти на всех этапах раннего развития тимоцитов и блокирующие другие пути дифференцировки клеток-предшественников (в направлении В-, NK-, дендритных клеток).
Для запуска перестройки V-генов TCR наиболее важна передача сигнала, осуществляемая Notch-1 на стадиях DN2 и DN3. Рецептор для этого фактора экспрессируется тимоцитами на указанных стадиях развития. Лиганды Notch-рецептора — молекулы Delta и Jagged — находятся на поверхности эпителиальных клеток тимуса. Определенную роль в индукции перестрой-ки V-генов играют цитокины, в частности IL-7, который особенно важен для запуска перестройки V-гена γ-цепи. Еще более существенна роль IL-7 в качестве фактора выживания, индуцирующего экспрессию антиапоптотического фактора Bcl-2. На этом этапе развития после запуска перестройки V-генов TCR развитие макрофагов и В-лимфоцитов становится невозможным.
Реаранжировка происходит в основном при переходе от стадии DN2(CD4+CD25+) к стадии DN3 (CD44-CD25+), которые называют также стадиями про-Т и пре-Т, соответственно. На этих стадиях экспрессируются гены RAG1 и RAG2, ген фермента TdT и гены других компонентов рекомбинационного комплекса. Перестройка V-генов TCR происходит, как принято считать, в последовательности δ, γ, β. Однако это правило соблюдается не очень строго: все 3 гена начинают перестраиваться практически одновременно. Как и в случае V-генов иммуноглобулинов, сначала перестраиваются гены только на одной хромосоме. В генах β- и δ-цепей сближаются сегменты D и J, а затем происходит полномасштабная перестройка с вовлечением основного сегмента V-гена и формированим непрерывных последовательностей VDJ. Реаранжировка генов γ-цепи проходит так же, но с одним отличием: поскольку в гене γ-цепи отсутствует D-сегмент, в результате перестройки формируется последовательность VJ. Как и при реаранжировке V-генов иммуноглобулинов, при неудачной перестройке V-гена на одной хромосоме процесс повторяется на другой хромосоме. Успешная перестройка служит сигналом к прекращению этого этапа реаранжировки. Это обусловливает экспрессию клеткой только одного варианта продуктов перестроенных V-генов. Реаранжировка V-генов TCR делает невозможной дифференцировку про-Т-клеток в направлении NK- и дендритных клеток.
При удачной перестройке V-гена β-цепи экспрессируется пре-T-рецеп-тор. Он представляет собой димер, состоящий из полноценной β-цепи и инвариантной (т.е. лишенной вариабельного участка) цепи, называемой пре-TCRα. Экспрессия этой молекулы на мембране сопровождается ее спонтанной олигомеризацией, что само по себе (т.е. без связывания какого-либо лиганда) сигнализирует о благополучной перестройке. Экспрессия пре-T-рецептора и передача сигнала с этой молекулы служит 1-й контрольной точкой перестройки TCR. Ответ на этот сигнал — усиление экспрессии фактора,блокирующего развитие апоптоза (Bсl-2), и запуск пролиферации клеток (индуцируется преимущественно IL-7). Если после двух попыток перестройки проторецептор не экспрессируется, клетка подвергается апоптозу. Как и при реаранжировке V-генов иммуноглобулинов, успешная перестройка V-гена β-цепи происходит в 55% клеток. Отбор тимоцитов, успешно перестроивших V-ген β-цепи, путем подавления их апоптоза и индукции пролиферации, называют β-селекцией. В период β-селекции временно прекращается экспрессия генов RAG1и RAG2и приостанавливается процесс перестройки генов.
К концу фазы DN3 тимоциты приобретают фенотип CD44-CD25+. Длительность фазы DN3 до β-селекции составляет 2 сут, а период β-селекции — еще 1 сут. На заключительном этапе фазы DN3 на клетках экспрессируется корецептор CD4 (стадия ISP — от Immature single-positive, т.е. незрелых моноположительных тимоцитов).
DN4/ISP стадия
[править]Тимоциты приобретают фенотип CD44-CD25 -одновременно с экспрессией корецепторов CD4 и CD8 (точнее, экспрессией молекулы CD8 в дополнение к уже присутствующей на мембране молекулы CD4). Продолжительность стадии дважды положительных тимоцитов невелика (1,5–2 сут), однако в это время происходит несколько событий, принципиально важных для развития Т-лимфоцитов. Одно из этих событий — реализация завершающего этапа формирования αβTCR — перестройка V-гена α-цепи. Поскольку в α-гене отсутствуют D-сегменты, реаранжировка приводит к образованию VJ-продукта. Хотя вероятность возникновения ошибки при этом почти такая же, как при перестройке V-гена β-цепи, результативность реаранжировки α-гена выше. При неудачной перестройке генов, расположенных на обеих хромосомах, процесс начинается заново, причем в него вовлекаются другие V- и J-сегменты. Такой «перебор» сегментов продолжается до успешной перестройки, что может занять 3–4 сут. Все это время не прекращаются экспрессии генов, кодирующих RAG-1, RAG-2 и TdТ. Именно поэтому вероятность неудачи на этом этапе реаранжировки даже ниже, чем на этапе перестройки V-генов L-цепи иммуноглобулинов в В-клетках.
После перестройки V-генов обеих цепей происходит сборка их продуктов и экспрессия «зрелого» TCR на поверхности клетки. Важно, что специфичность TCR у каждого индивидуального тимоцита различна, поскольку процесс перестройки осуществляется в них независимо от других клеток и вероятность совпадения нуклеотидной последовательности в перестроенных генах разных клеток практически равна нулю. Зрелый TCR экспрессируется в комплексе с CD3 и ζ-цепями. Поскольку CD3 и ζ-димер отвечают за передачу сигнала от рецептора в ядро, клетки уже на этом этапе имеют функционально полноценный рецептор. Вероятно, появление на поверхности тимоцита зрелого рецептора служит сигналом, необходимым для прекращения экспрессии Т-клеткой генов RAG1 и RAG2 и для поддержания ее жизнеспособности. В этом состоит суть второй «контрольной точки» при формировании TCR. Плотность экспрессии TCR на поверхности тимоцитов сначала невелика. Выживаемость клеток в этот период обеспечивается взаимодействием молекулы семейства TNF — CD70 тимоцита и молекулы семейства TNFR — CD27 эпителиальной клетки.
Положительная селекция
[править]Дважды положительные клетки очень чувствительны к апоптозу (в связи с низкой экспрессией ими антиапоптотических факторов, таких, как Bcl-2 и Bcl-XL). Для выживания дифференцирующимся Т-клеткам нужна поддержка микроокружения, особенно эпителиальных клеток коры тимуса, в которой локализуются CD4+CD8+ тимоциты. Сигнал, необходимый для выживания, тимоциты получают в ходе положительной селекции. Набор рецепторов, формируемый в ходе случайной перестройки генов, никак не связан с реальными потребностями иммунной системы. В то же время для нормального функционирования иммунной системы нужно, чтобы Т-клетки несли TCR, распознающие молекулы MHC, содержащие пептидные фрагменты антигенов. Положительная селекция обеспечивает отбор только тех тимоцитов, которые экспрессируют ТСR, обладающие сродством к молекулам MHC.
Положительной селекции подвергаются дважды положительные тимоциты фенотипа CD4+CD8+CD3loCD27-. В качестве «отбирающего фактора» выступают кортикальные эпителиальные клетки, экспрессирующие цитокератин СК8 и молекулы MHC обоих классов, но лишенные костимулирующих молекул. Тимоциты, перемещаясь от периферии коры к кортико-медуллярной зоне, тесно контактируют с эпителиальным ретикулумом, образующим трехмерный каркас тимуса. При этих механических контактах TCR тимоцитов взаимодействуют с экспрессированными на поверхности эпителиальных клеток молекулами MHC как I, так и II классов, содержащими фрагменты различных эндогенных молекул (чужеродные молекулы в тимусе отсутствуют). Если TCR обладает сродством к молекуле MHC, тимоцит получает поддерживающий сигнал, основными результатами которого служат повышение экспрессии антиапоптотического фактора Bсl-2 и продвижение тимоцита по клеточному циклу. Внешний признак успешного прохождения тимоцитом положительной селекции — экспрессия маркера активации клетки CD69, а также молекул CD5, CD27 и костимулирующей молекулы CD28, сопровождающаяся повышением плотности экспрессии рецепторного комплекса TCR–CD3 на поверхности клетки. Т-лимфоциты, рецепторы которых лишены сродства к МНС, подвергаются апоптозу «по умолчанию», т.е. не в силу сигнала извне, передаваемого через мембранные рецепторы, а вследствие срабатывания внутренних (митохондриальных) механизмов. Поскольку сродством к молекулам MHC обладают TCR лишь незначительной части клонов образующихся тимоцитов, на этапе положительной селекции погибает 90% CD4+CD8+тимоцитов.
Отрицательная селекция
[править]Тимоциты, прошедшие положительную селекцию, мигрируют в корти-комедуллярное сочленение и в мозговой слой тимуса, где они проходят следующий этап отбора — отрицательную селекцию. На этом этапе тимоциты представлены дважды положительными клетками или «полузрелыми» мооно-положительными клетками фенотипа СD4+/CD8+CD24hi. Отрицательную селекцию осуществляют медуллярные дендритные и эпителиальные клетки. Те и другие клетки экспрессируют молекулы MHC обоих классов и костимулирующие молекулы (СD80, CD86, CD40). Маркеры медуллярных эпителиальных клеток — цитокератин 5 и лектин улитки UEA1.
На этом этапе происходит дискриминация тимоцитов по степени сродст-ва к комплексу MHC–пептид. Клетки, обладающие высоким сродством, подвергаются апоптозу как потенциально опасные (поскольку они хорошо распознают пептидные фрагменты аутологичных белков в составе аутоло-гичных молекул MHC, они могут индуцировать аутоиммунные реакции). Сигналом к реализации апоптоза служит экспрессия ядерного фактора Nur77, который, таким образом, служит маркером клеток, подлежащих элиминации. В результате жизнеспособность сохраняют только тимоциты, рецепторы которых обладают умеренным (промежуточным) сродством к аутологичным комплексам MHC–пептид. Именно такие клетки мигрируют в периферический отдел иммунной системы и участвуют в развитии иммунного ответа и реализации антигенспецифической иммунной защиты.
Постоянно возникает вопрос, почему сигнал, поступающий в тимоциты через TCR, в одном случае (положительная селекция) обеспечивает поддержание жизнеспособности клеток, а в другом (отрицательная селекция) вызывает их гибель. Основой этих различий являются особенности клеток, вступающих в соответствующую фазу селекции. В силу различной молекулярной конститутции внутриклеточная сигнализация при аналогичных внешних сигналах и использовании практически одних и тех же сигнальных путей приводит к доминированию различных факторов и включению различных результирующих механизмов, приводящих в одном случае к поддержанию жизнеспособности, в другом — к развитию апоптоза. Полностью детали внутриклеточной сигнализации при положительной и отрицательной селекции тимоцитов не выяснены. Однако известно, например, что при положительной селекции в передачу сигнала в большей степени вовлекаются ферменты MAP-каскада, приводящие к образованию транскрипционного фактора c-Fos, а также Са2+ -зависимый сигнальный путь, обеспечивающий формировнаие фактора NF-AT. В то же время при отрицательной селекции доминируют JNK- и p38-ветви MAP-каскада, приводящие к образованию транскрипционного фаткора с-Jun. Маркером отрицательной селекции является киназа MINK.
Из сказанного выше следует, что Т-клетки как бы «натаскиваются» на распознавание собственных антигенов, а не чужеродных молекул, но степень агрессивности Т-клеток в отношении собственных молекул ограничивается отрицательной селекцией. Этим клеткам предстоит распознавать комплексы аутологичных молекул МНС с пептидными фрагментами чужеродных белков, что осуществляется в силу высокой перекрестной реактивности TCR. Тем не менее, риск аутоагрессивности сохраняется и для его ограничения требуются дополнительные механизмы, такие как контроль со стороны регуляторных Т-клеток.
При отрицательной селекции удаляются клоны, распознающие с высоким сродством антигены, представленные в тимусе. В связи с этим возникает вопрос, насколько набор антигенов, экспрессируемых в тимусе, является представительным для всего организма. Общеизвестно, что существуют органоспецифические антигены — белки, характерные для того или иного органа и выполняющие специфические функции. Из этого следует, что в популяции тимоцитов, прошедших отрицательную селекцию, должны сохраняться клоны, способные распознавать органоспецифические антигены других органов (не тимуса).
Однако такие клетки элиминируются при отрицательной селекции (если не полностью, то в значительной степени) благодаря эктопической экспрессии в тимусе небольших количеств органоспецифических антигенов. Этот процесс контролирует продукты гена AIRE(от Autoimmunity regulator). Белок, кодируемый геном AIRE, содержит домены, предназначенные для взаимодействия с ДНК (т.е. он является транскрипционным фактором), домены, ответственные за взаимодействие с ядерными рецепторами, а также 2 домена со структурой «цинковых пальцев» (zink finger). Механизмы действия белка AIRE неизвестны. Результат его активности — экспрессия генов органоспецифических антигенов различных органов (прежде всего эндокринных) в клетках мозговой зоны тимуса — эпителиальных, в меньшей степени — дендритных и В-лимфоцитах (редких, но тем не менее выявляемых в тимусе). Всего в тимусе экспрессируется 2000–3000 генов внетимусных белков, для экспрессии 500 из них доказана роль AIRE. Эта экспрессия мозаична: обычно в каждой клетке может экспрессироваться один из белков, причем каждый белок экспрессируется всего примерно в 100 клетках. В связи этим возникает вопрос, как столь незначительное количество антигена может обеспечить элиминацию аутореактивных клонов. Считают, что в этом принимают участие дендритные клетки, утилизировавшие продукты распада эпителиальных клеток или получившие антиген путем «откусывания» фрагментов эпителиальных клеток. О результативности такого механизма отрицательной селекции свидетельствует резкое возрастание аутоиммунных патологий при мутациях гена AIRE, ведущих к развитию синдрома APECED (Autoimmune polyendocrinopathy, candidiasis, endodermal dystrophy— аутоиммунная полиэндокринопатия, кандидоз, энто-дермальная дистрофия).
На этапе отрицательной селекции гибнет почти 50% тимоцитов, прошедших положительную селекцию (около 5% от числа незрелых дважды положительных тимоцитов). Однако в действительности достаточно много аутоспецифических Т-клеток не элиминируется в процессе отрицательной селекции и пополняет пул зрелых Т-лимфоцитов, создавая угрозу ауто-агрессии. Для предотвращения этой угрозы необходимы дополнительные механизмы защиты в виде редактирования генов α-цепей TCR, индукции анергии и контроля иммунного ответа регуляторными Т-лимфоцитами.
Дифференцировка CD4+ и CD8+ тимоцитов
[править]Одновременно с селекцией тимоцитов происходит разделение их на субпопуляции, основанное на избирательной экспрессии корецепторов CD4 или CD8. Поскольку зрелые моноположительные тимоциты локализуются в мозговом слое тимуса, можно предположить, что разделение на субпопуляции происходит на этапе отрицательной селекции, однако не исключено, что этот процесс может быть связан с положительной селекцией. Дифференцировка Т-клеток регулируется как внутренними (дифференцировочные факторы), так и внешними (сигналы, генерируемые при контактах между клетками) стимулами. Несмотря на то, что факторы группы Notch действуют на этом этапе развития тимоцитов, они не оказывают решающего влияния на выбор пути дифференцировки. Считают, что для дифференцировки Т-лимфоцитов в CD8+ клетки нужен сигнал большей интенсивности, чем для дифференцировки CD4+ Т-клетки. Более специфично действие других факторов: сочетанная экспрессия в клетках факторов Th-POK и GATA-3 направляет Т-клетку по CD4+-пути, тогда как экспрессия факторов Tox и Runx3 — по CD8+пути.
Установлено, что на CD4+CD8+клетках в определенный момент ослабляется экспрессия корецептора CD8 (фенотип СD4+CD8lo). Если TCR специфичен к MHC-II, как и доминирующий корецетор (CD4), то в клетке генерируется сильный сигнал, и она переходит на стадию CD4+CD8-. Если TCR обладает более высоким сродством к комплексу пептид–MHC-I, т.е. специфичность ТСR и CD4 не совпадает, формируется слабый сигнал. Это приводит к усилению экспрессии CD8 и утрате CD4, т.е. к развитию CD4-CD8+Т-клеток.
После такой селекции путем подтверждения адекватности корецеп-тора клетка приобретает функциональные свойства, соответствующие ее назначению. Так, CD8+T-клетки (Т-киллеры) приобретают способность формировать цитолитический молекулярный комплекс, что обеспечивает функционирование такой Т-клетки в качестве цитотоксического Т-лимфоцита. В CD4+T-лимфоцитах (Т-хелперах) формируются внутриклеточные механизмы, необходимые для выполнения «хелперной» функции, прежде всего — способность активно вырабатывать цитокины при активации. В результате Т-клетки дифференцируются в функционально полноценные субпопуляции цитотоксических и хелперных Т-лимфоцитов.
В результате описанных выше процессов в тимусе образуется популяция функционально полноценных αβТ-лимфоцитов, способных участвовать в иммунном ответе и обеспечивать антигенспецифическую иммунную защиту организма. Популяция зрелых Т-клеток гетерогенна по двум параметрам — специфичности ТСR и функциональной активности. Разнообразие специфичностей TCR служит основой клональной структуры популяции Т-клеток. Тимоциты, сформировавшие уникальный по составу и специфичности рецептор, пройдя селекцию, образуют клон — группу потомков родоначальной клетки с рецепторами той же специфичности. В результате селекции клонов сохраняются и поддерживаются только клетки, распознающие комплексы аутологичных молекул MHC и эндогенных пептидов с умеренным сродством, недостаточным для развития ответа на аутоантигены, но достаточным для распознавания чужеродных пептидов в составе молекулы MHC на основе перекрестной реактивности.
Созревшие тимоциты довольно долго (7–14 сут) не покидают тимус, пребывая преимущественно в наружных слоях мозгового слоя, богатых дендритными клетками. В этот период завершается формирование аутотолерантности и Т-клетки приобретают свойства, важные для поддержания их жизнеспособности вне тимуса. Так, вследствие активации сиалилтрансфераз происходит сиалирование мембранных гликопротеинов, защищающее лимфоциты от поглощения макрофагами. Созревшие Т-лимфоциты начинают экспрессировать набор мембранных молекул адгезии и рецепторов для хемокинов, необходимые для направленной миграции клеток в специализированные участки иммунной системы и для последующей рециркуляции.
Развитие Т-клеток в тимусе длится около 20 сут. За это время, с одной стороны, происходит массовая (до 99%) гибель тимоцитов в процессе их созревания (главным образом, на разных этапах селекции), а с другой — пролиферация выживших клеток с образованием клонов. В зрелом возрасте из тимуса ежедневно эмигрируют Т-клетки в количестве, равном 1% от общей численности тимоцитов.
Помимо рассмотренных выше субпопуляций CD4+ и CD8+ Т-лимфоцитов в тимусе дифференцируются «неклассические» субпопуляции Т-клеток.
Главный комплекс гистосовместимости
[править]
Главный комплекс гистосовместимости - это группа генов и кодируемых ими антигенов клеточной поверхности, которые играют важнейшую роль в распознавании чужеродного и развитии иммунного ответа. Главный комплекс гистосовместимости человека получил название HLA . HLA был открыт в 1952 г. при изучении антигенов лейкоцитов. Антигены HLA представляют собой гликопротеиды, находящиеся на поверхности клеток и кодируемые группой тесно сцепленных генов 6-й хромосомы(6p). Антигены HLA играют важнейшую роль в регуляции иммунного ответа на чужеродные антигены и сами являются сильными антигенами.
Генетика главного комплекса гистосовместимости
[править]Локусы HLA обладают высоким полиморфизмом, т.е. в каждом локусе среди популяции находится множество альтернативных форм гена (аллелей). Гены HLA лежат очень близко друг к другу, поэтому большинство людей наследуют аллели этих локусов как два набора, по одному от каждого родителя. Этот набор аллелей называется гаплотипом. Человек наследует один гаплотип от матери, второй – от отца. Аллели экспрессируются кодоминантно, то есть в одной клетке экспрессируются продукты и материнского, и отцовского гена. Вероятность того, что два неродственных человека будут иметь идентичные наборы HLA крайне низка. Локусы HLA занимает большое пространство — 4 млн пар нуклеотидов и содержит больше 200 генов. Выделяют 3 класса генов MHC— I, II и III. В отторжении несовместимых трансплантатов и презентации антигена Т-клеткам участвуют продукты генов классов I и II, расположенные соответственно в 3’- и 5’-частях комплекса. Первоначально их разделяли по ндукции их продуктами преимущественно гуморального (I класс) или клеточного (II класс, описанный несколько позже, чем I) иммунитета. Выделяют 2 группы генов I класса. Первую образуют гены А, В и С, отличающиеся беспрецедентно высоким полиморфизмом — известно по нескольку сотен их аллельных форм (например, HLA-B— 830). Это классические гены I класса. Другую группу образуют неклассические гены Е, F, G, H (гены с ограниченным полиморфизмом). Только продукты классических генов I класса участвуют в презентации антигена Т-лимфоцитам.
Гены MHC класса II также включают несколько вариантов. В презентации антигена непосредственно участвуют продукты генов DR(αи β), DP (αи β)и DQ(αи β), кодирующие соответствующие полипептидные цепи молекул. Во всех случаях для генов β-цепей характерен значительно более высокий полиморфизм, чем для генов α-цепей.
Гены MHC класса III, как уже упоминалось, не причастны к молекулам гистосовместимости и осуществляемой ими презентации. Они кодируют некоторые компоненты комплемента, цитокины семейства фактора некроза опухоли, белки теплового шока.
Молекулы MHC — полиморфные продукты главного комплекса гистосовместимости классов I и II
[править]HLA-I. Молекулы I класса содержатся на поверхности всех типов клеток, кроме эритроцитов и ворсинчатого трофобласта, представляют собой гетеродимеры, состоящие из двух полипептидных цепей — тяжелой (46 кДа) и легкой (12 кДа). Из них только тяжелая субъединица (α-цепь) является продуктом главного комплекса гистосовместимости, и именно с ней связаны иммунологические функции молекулы. Цепь а пронизывает плазматическую мембрану и имеет три внеклеточных домена — αl, α2 и αЗ. Вариабельность молекулы сконцентрирована в αl- и α2-доменах; домен αЗ лишен полиморфизма.
Легкая (β) цепь представлена β2-микроглобулином. Это продукт гена, который локализован на хромосоме 15, т.е. не входит в состав комплекса HLA. β2-микроглобулин генетически однороден и напрямую не участвует в реализации функций HLA-I. Его роль сводится к транспорту α-цепи на поверхность клетки. Молекулы HLA-I представлены тремя наиболее важными подклассами — HLA-A, HLA-B и HLA-C. Они кодируются одноименными генами, которым соответствует определенная позиция (локус) на хромосоме 6. В генотипе каждого человека имеется шесть генов HLA-I — по три в каждом гаплотипе. Недавно открыты дополнительные локусы HLA-I — E, F и G. Их гены отличаются ограниченным полиморфизмом и необычным тканевым распределением своих продуктов. Функции этих, так называемых неклассических HLA-молекул не известны, но они не участвуют в представлении антигенов, по крайней мере обычных пептидов.
HLA-II. Молекулы II класса построены из двух нековалентно связанных пептидных цепей примерно одинакового размера — α (35 кДа) и β (28 кДа). Обе они являются продуктами главного комплекса гистосовместимости и участвуют в реализации его иммунологических функций. Каждая цепь состоит из двух внеклеточных доменов (αl—α2 и β1—β2), которые прочно фиксированы на клетках при помощи трансмембранного участка молекулы. Вариабельные последовательности входят в состав αl- и α1-доменов; α2- и β2-домены не имеют аллотипов. Подобно HLA-I, молекулы HLA-II представлены тремя основными подклассами — DR, DQ и DP. В генотипе каждого человека имеется 12 функционально значимых (т.е. экспрессируемых) генов HLA-II — шесть в каждом гаплотипе (по три гена для α- и β-цепей). Наиболее полиморфны гены β-цепей, и именно они указываются в цифровых формулах молекул класса II (α домен обозначается буквой А, β-домен — буквой В). Буква D ошибочно продолжает нотацию HLA, начатую локусами А, В и С. Все эти обозначения (А, В, С, D) возникли до разделения HLA на классы. Область D оказалась суммой нескольких локусов (DR, DQ, DP) и по сути является синонимом II класса.
Таким образом, все молекулы MHC в общей сложности содержат 2 примембранных домена суперсемейства иммуноглобулинов и 2 дистальных домена другой (сходной между собой) структуры. Дистальные домены в молекулах MHC-I образованы одной цепью (α), а в молекулах MHC-II — разными цепями (α и β). Именно эти дистальные домены молекул MHC связывают антигенный пептид и играют ключевую роль в формировании лиганда TCR.
Подчеркнем одно очень важное обстоятельство, касающееся вариабельности ключевых молекул иммунной системы. Исключительно высокий уровень вариабельности свойствен как антигенраспознающим структурам (антителам, TCR), так и молекулам MHC, участвующим в построении лиганда ТСR. Однако все варианты антител и TCR (порядка 106) присутствуют в одном организме, являясь продуктами одновременно присутствующих в нем генов, в то время как вариабельность молекул МНС проявляется на уровне популяций человека и животных, тогда как в каждом конкретном организме может присутствовать не более 2 вариантов молекул — продуктов аллельных генов. Если учесть, что у человека есть 8 высокаполиморфных генов MHC (А, В, С, а также β-гены DP, DQ и DR и α-гены DP и DQ), то число вариантов полипептидных цепей MHC не может превышать 16.
Молекулы MHC-I и MHC-II представлены на поверхности клеток, но существенно различаются по тканевому распределению. Молекулы MHC-I присутствуют практически на всех ядросодержащих клетках организма и отсутствуют на эритроцитах и клетках ворсинчатого трофобласта. На каждой клетке обычно содержится около 7000 молекул MHC-I. Плотность их экспрессии может изменяться под влиянием различных факторов, в частности, цитокинов. Молекулы MHC-II присутствуют на поверхности ограниченного числа клеточных типов. Они экспрессируются прежде всего на АПК — дендритных клетках, В-лимфоцитах и активированных макрофагах.
Содержание молекул на поверхности этих клеток сильно варьирует. На одной дендритной клетке обычно содержится порядка 100 000 молекул MHC-II. При определенных условиях (например, при воспалении) они могут появляться на поверхности других активированных клеток — эпителиальных, эндотелиальных и т.д. Классический индуктор молекул MHC-II — IFNγ. Особенность мембранных молекул MHC — их быстрый обмен на поверхности клеток, особенно характерный для MHC-I (время обновления молекул — около 6 ч).
Механизмы образования комплексов пептидов-антигенов с молекулами главного комплекса гистосовместимости
[править]Как уже упоминалось выше, продукты генов MHC в силу своей чрезвычайно высокой вариабельности в пределах популяции обусловливают отторжение пересаживаемых тканей. Долгое время эти молекулы изучали преимущественно в контексте трансплантологии, что определило их обозначение как генов и антигенов гистосовместимости. Однако пересадка тканей — искусственная процедура, практически не имеющая аналогов в естественных условиях (наиболее близкая аналогия — развивающийся плод млекопитающих — скорее служит примером противостояния отторжению несовместимых тканей). Поэтому вскоре после описания генов MHC и их продуктов возник вопрос об их функциях. Их биологическое назначение было осмыслено в 70-х годах XX века в уже упоминавшихся исследованиях Р. Цинкернагеля (R. Zinkernagel) и П. Догерти (Р. Dogherty), которые пока-зали, что Т-клетки распознают «измененное свое» — фрагмент антигена, встраивающийся в состав молекулы MHC, вместе с модифицированной этим пептидом молекулой MHC (Нобелевская премия 1996 г.). Таким образом, антиген распознается Т-клеткой только при встраивании его фрагментов в состав молекул MHC, которые при этом выступают не только в роли каркаса, несущего пептид, но и в качестве распознаваемого лиганда. Только в таком виде антиген может быть распознан Т-лимфоцитами. Поскольку Т-клетки участвуют как в индукции иммунного ответа, так и в его регуляции и осуществлении ряда эффекторных функций, презентация антигенного пептида Т-лимфоцитам может рассматриваться как одно из ключевых событий иммунного ответа. Это определяет исключительную важность процесса встраивания пептида в молекулы МНС.
Молекулы MHC, не содержащие пептида, встроенного в антигенсвязывающую полость, нестабильны. На поверхности клеток присутствуют молекулы MHC, содержащие в своем составе пептиды. Таким образом, встроенный в молекулу MHC пептид следует рассматривать как ее интегральную часть. В каждой клетке в составе молекул MHC презентируются тысячи разных пептидов, что еще больше увеличивает вариабельность рассматриваемых молекул. В структуре антигенсвязывающей полости молекул MHC-I и MHC-II имеются некоторые особенности. В MHC-I полость замкнута, т.е. ограничена не только с боков, но и с концов. В результате размер пептида, способного встроиться в нее, строго ограничен 8–10 аминокислотными остатками (чаще всего — 9). В отдельных случаях, если размеры пептида превышают указанные значения, он «выпирает» из щели, формируя арку. В MHC-II полость ограничена только с боков и имеет открытые концы. Поэтому размер встраивающихся в нее пептидов может варьировать в широких пределах — от 12 до 25 аминокислотных остатков; концы пептида могут выступать за пределы полости.
В молекулы MHC-I встраиваются пептиды — образующиеся в цитоплазме клетки в процессе естественной деградации цитоплазматических белков в специальных образованиях (протеасомах). Протеасомы — надмолекулярные структуры с константой седиментации 20S (молекулярная масса — 1500 кДа). Они сформированы наружным и внутренним кольцами, каждое из которых образовано семью субъединицами — α(наружное кольцо) и β(внутреннее кольцо). Три β-субъединицы — β1, β2 и β5 обладают протеолитической активностью и участвуют в расщеплении белков цитозоля. Под влиянием IFNγ(образуется при иммунных процессах NKT-, NK- и Th1-клетками) синтезируются цепи iβ1(LMP2), iβ2(MECL1) и iβ5(LMP-7), замещающие соответствующие протеолитические субъединицы. Обновленную протеа-сому называют иммунопротеасомой. Смысл замены субъединиц состоит в усилении хемотриписно- и трипсиноподобной активности и ослаблении каспазоподобной активности протеасомы, что приводит к повышению эффективности образования пептидов с основными и гидрофобными С-концами (именно они встраиваются в молекулы MHC-I) и уменьшению доли пептидов с кислыми С-концами (не встраиваются в MHC-I).
Образовавшиеся пептиды транспортируются из цитополазмы в эндоплазматический ретикулум, в котором на рибосомах синтезируются полипептидные цепи молекулы MHC-I — α-цепь и β2-микроглобулин. Транспорт пептидов происходит с участием транспортных систем ТАР (Transporter asso-ciated with antigen processing), кодируемых MHC-генами ТАР1 и ТАР2. α-Цепь молекул класса I сразу после синтеза и встраивания в мембрану эндо-плазматического ретикулума соединяется с β2-микроглобулином. Однако, как уже упоминалось, молекулы MHC, не содержащие пептид, нестабильны. Их конформация стабилизируется временно с помощью специальных молекул — шаперонов (в данном случае — калнексина и калретикулина). Доставленные в эндоплазматический ретикулум пептиды при контакте с молекулами MHC-I встраиваются в их полость, после чего молекулы шаперонов отделяются от готовой и стабилизированной молекулы класса I. В составе мембран ндоплазматического ретикулума молекулы класса I перемещаются сначала в аппарат Гольджи, а затем при помощи секреторных везикул — на поверхность клетки. В результате на клеточной поверхности оказываются молекулы MHC-I, содержащие различные фрагменты внутриклеточных белков.
Пептиды, презентируемые в составе молекул MHC-II, имеют внеклеточное происхождение. Дендритные и другие АПК поглощают экзогенные молекулы в процессе эндоцитоза. Выделяют 4 разновидности эндоцитоза:
- фагоцитоз;
- макропиноцитоз;
- клатринопосредованный эндоцитоз;
- кавеолоопосредованный эндоцитоз.
Фагоцитарный механизм относительно слабо используется любыми АПК, кроме моноцитов/макрофагов, для которых этот путь интернализации является основным. Макропиноцитоз широко распространен при интернализации экзогенных веществ макрофагами и незрелыми дендритными клетками. Клатринзависимый механизм чаще всего бывает задействован при поглощении иммунных комплексов и других формах рецепторного эндоцитоза (одинаково выражен у незрелых и зрелых дендритных клеток). Кавеолозависимый эндоцитоз происходит несколько реже. Среди рецепторов, усиливающих эндоцитоз, наиболее важную роль (особенно для дендритных клеток) играет лектиновый рецептор DEC-205. В результате эндоцитоза формируются ранние эндосомы, содержащие интернализованные белки из межклеточного пространства. Некоторые ранние эндосомы возвращаются на наружную мембрану со сроком полужизни 1–2 мин. Около 25% эндосом транспортируется вглубь клетки и сливается с секреторными везикулами, формирующимися из эндоплазматического ретикулума и содержащими встроенные в мембрану молекулы MHC-II. В эндосомы может проникать также содержимое цитозоля (по механизму аутофагии), что приводит к презентации фрагментов цитоплазматических белков в составе молекул MHC-II. Структуру еще не связавших пептид молекул MHC-II стабилизирует полипептидная цепь Ii (от англ. — Invariant сhain), заполняющая антигенсвязывающую полость и примыкающая к боковой поверхности цепей молекулы класса II. Участок внутриклеточного пространства, в котором происходят описываемые процессы, называют MIIC (MHC class II compartment). При перемещении в глубь клетки внутренняя среда эндосом закисляется, что способствует активации содержащихся в них протеаз — катепсинов L и S. С такой закисленной эндосомой сливаются везикулы, содержащие молекулы MHC-II. Катепсины расщепляют белки, содержащиеся в эндосоме, с образованием пептидов. Одновременно они расщепляют Ii-цепь таким образом, что в составе молекулы класса II остается только фрагмент Ii-цепи, встроенный в пептидсвязывающую полость. Этот пептид обозначают как CLIP (Class II associated invariant chain peptide). Пептиды, образующиеся из экзогенных белков, вытесняют CLIP из полости. В этом процессе задейст-вована молекула HLA-DM (продукт гена MHC класса II), присутствующая в везикуле. Взаимодействие HLA-DM с MHC-II катализирует высвобождение CLIP, в результате чего пептидсвязывающая полость MHC становится доступной для встраивания других пептидов. У мышей с мутациями гена HLA-DM этот процесс не осуществляется, в результате чего все молекулы MHC-II содержат один и тот же пептид — CLIP. После слияния эндосом с везикулами поздняя эндосома перемещается к поверхности клетки. Происходит экзоцитоз ее содержимого. При этом мембрана везикулы сливается с мембраной клетки, в результате чего молекулы MHC-II, несущие пептид, оказываются на поверхности клетки.
Описанные процессы встраивания фрагментов внутриклеточных и внеклеточных белков в молекулы MHC отражают важные для клетки процессы, назначение которых пока непонятно. Всем клеткам организма зачем-то нужно представлять на своей поверхности фрагменты собственных белков, а АПК — еще и фрагменты белков из их окружения. Очевидно, иммунная система лишь воспользовалась готовым механизмом для формирования антигенных структур, распознаваемых Т-клетками, и запуска иммунных процессов.
Сродство корецепторов CD4 и CD8 к молекулам MHC разных классов (соответственно, II и I) имеет важное значение для «разделения труда» Т-клеток, несущих эти корецепторы. CD4+ Т-клетки получают сигнал от АПК и отвечают на внеклеточные антигены, т.е. на молекулы, локализованные вне клеток или в эндосомах. CD4+ Т-клетки участвуют в защите от таких патогенов. Активирующий сигнал эти лимфоциты получают от дендритных клеток, представляющих им антиген в составе молекул MHC-II. В связи с выполняемыми ими функциями, CD4+Т-клетки называют Т-хелперами. CD8+Т-клетки, распознавая внутриклеточные белки, презентируемые в составе молекул MHC-I, участвуют в защите от внутриклеточных патогенов. Основная функция CD8+Т-клеток — цитолиз (убийство, киллинг) инфицированных клеток. Выполнение этой функции CD8+Т-клетками облегчается тем, что молекулы MHC-I присутствуют на всех ядросодержащих клетках организма. CD8+Т-клетки называют цитотоксическими Т-лимфоцитами, или Т-киллерами.
Суперантигены
[править]В борьбе за свое существование инфекционные микроорганизмы «научились» синтезировать некие вещества, которые поступают с «нашими» Т-лимфоцитами «не по правилам». Эти вещества называют суперантигенами. Когда они попадают в организм, то последний не может встретить их попыткой распознавания специфическим TCR потому, что суперантигены благодаря своим особым химическим свойствам способны присоединяться снаружи клетки. АПК презентируют суперантигены Т-клеткам, но не поглощают и не процессируют их. Суперантигены обладают сродством к молекулам MHC-II (но не MHC-I) и связываются с их «боковой» поверхностью. CD4+Т-лимфоциты распознают суперантигены при помощи TCR, но во взаимодействие вовлекается участок V-домена β-цепи, не связывающий антиген. Например, стафилококковый экзотоксин — суперантиген SEB — связывается с одной стороны с α1-доменом молекулы MHC-II, а с другой — с β-цепью TCR, семейств Vβ7 и Vβ8. В результате в реакцию на суперантигены вовлекаются не отдельные клоны, а все Т-клетки, экспрессирующие TCR семейств, к которым обладает сродством данный суперантиген. Обычно доля вовлекаемых CD4+Т-клеток составляет 20–30% от их общего числа. CD8+Т-клетки при этом не активируются, поскольку их TCR не обладают сродством к молекулам MHC-II, с которыми взаимодействует суперантиген. В результате массовой активации Т-хелперов происходит неадекватный выброс цитокинов, а затем массовая гибель Т-клеток по механизму апоптоза. Таков закон лимфоцитарного иммунитета: на свой ли антиген или неспецифически, но единожды активированный лимфоцит обреченна апоптоз(феномен AICD—activation-induced cell death — индуцированной активацией клеточной смерти). Делеция реагирующих клонов существляется в 3 стадии: острую (в течение 12–20 ч — апоптоз без делений), подострую (апоптоз после 3–5-дневной пролиферации) и хроническую (после длительной персистенции суперантигена). Это вносит свой вклад в патогенез соответствующих инфекционных заболеваний.
Генетический полиморфизм главного комплекса гистосовместимости
[править]
Система генов тканевой совместимости человека (Human Leukocyte Antygen — HLA) является одной из наиболее полиморфных генетических систем, выполняющей в организме человека ряд функций. Важнейшими из них являются генетический контроль иммунного ответа и поддержание иммунного гомеостаза, нарушение которых лежит в основе таких патологических процессов, как аутоиммунные заболевания и развитие опухолей. Исследование полиморфизма системы HLA является одним из наиболее эффективных подходов к изучению структуры и функции главного комплекса гистосовместимости человека. Необходимость таких научных работ обусловлена, в том числе и тем фактом, что без полного представления о строении системы генов тканевой совместимости невозможно успешное развитие клинической трансплантологии. Особенно это касается пересадки аллогенного костного мозга.
Обеспечивая регуляцию иммунного ответа, система HLA (главный комплекс гистосовместимости человека) осуществляет генетический контроль взаимодействия всех иммунокомпетентных клеток организма, распознавание своих и чужеродных (в том числе измененных собственных) клеток, запуск и реализацию иммунного ответа и, в целом, обеспечивает выживание человека как вида в условиях экзогенной и эндогенной агрессии. Многообразие указанных функций обеспечивается особенностями строения главного комплекса гистосовместимости. Одна из этих особенностей — экстремальный аллельный полиморфизм комплекса генов HLА, являющийся «мощным механизмом вариабельности и естественного отбора» человека как вида, — позволяет ему противостоять постоянно эволюционирующему множеству патогенов.
Несмотря на сравнительно короткий период изучения системы HLA, она является на сегодняшний день самой хорошо изученной генетической системой не только в геноме человека, но и у млекопитающих в целом. Во многом этому способствовал беспрецедентно высокий уровень научной кооперации в исследовании HLA, где даже не принято патентование результатов. Один из основателей современной иммуногенетики Ж. Доссе в своей Нобелевской речи назвал изучение HLA самым ярким примером гуманитарного сотрудничества в истории человечества.
Самыми полиморфными участками аллелей HLA I класса являются 2-й и 3-й экзоны, но наиболее значимо (особенно для HLA-B) аллельное разнообразие 1-го экзона. Остальные экзоны и интроны сравнительно менее полиморфны. Что касается локусов HLA класса II, то в данном случае более полиморфен 2-й экзон, хотя некоторый полиморфизм обнаружен также в других экзонах (например, для локуса DQA1) и интронах.
Полиморфизм этих генов в популяции выгоден для выживания вида: не у одного, так у другого человека в популяции организм может быть сумеет представить Т-лимфоцитам своим вариантом молекул МН С антигены того или иного (в том числе и из вновь возникающих) инфекционного микроорганизма. Но вот каждый конкретный человек либо сумеет, либо нет воспринять конкретный микробный антиген и если не сумеет, то не сможет защититься от данного микроба иммунным ответом и инфекция может убить его.
Почему же число генов МН С I + II у индивидуума 12 и не больше? Ведь чем больше было бы генов МНС , тем большее разнообразие антигенов могли бы представлять антигенпредставляющие клетки для распознавания Т-лимфоцитам . Ограничение числа генов МН С можно объяснить механизмами позитивной и негативной селекции тимоцитов на связывание с МНС, представленными в тимусе во время и на месте лимфопоэза Т-лимфоцитов .
Исследования показывают, что из каждого подмножества тимоцитов, оставленных живыми при позитивной селекции на связывание с конкретным вариантом молекулы МНС , 5% будет элиминировано при негативной селекции как слишком аутореактивные, т.е . каждый вариант молекул МНС «стоит жизни» 5% тимоцитов . На 12 вариантов молекул МНС (если считать только I и II классы) в тимусе должно быть ликвидировано 12 х 5 = 60% тимоцитов . Реально в тимусе погибает более 95% тимоцитов и лишь менее 5% выходят в периферические лимфоидные органы . Видимо, в эволюции увеличивать полигенность МНС больше было нельзя.
Антигенпредставляющие молекулы «не МНС» - CD1
[править]Особую группу антигенпрезентирующих молекул образуют гомологи продуктов MHC-I — молекулы CD1 (CD1a, CD1b, CD1c и CD1d), кодируемые пятью полиморфными генами (CD1 A-D), локализованными у человека в хромосоме 1. По своей структуре молекулы CD1 сходны с MHC-I (гомология составляет 20–25%). Они обладают сходной доменной структурой (домены α1, α2 и α3). CD1 — трансмембранные белки, связанные с молекулой β2 -микроглобулина. Молекулярная масса белковой части CD1-комплекса — 33 кДа.
Домены α1 и α2 образуют антигенсвязывающую полость, закрытую с обоих концов (как и в молекулах MHC-I). Ее вместимость несколько больше, чем в молекулах MHC-I. CD1 связывает бактериальные и аутологичные липиды ( диацилглицерол, миколевую кислоту и т.д.) и липопептиды. От других молекул CD1 по ряду свойств отличается CD1d. Эта молекула связывает аутологчиные гликолипиды. Ее наиболее известный лиганд — α-галактозилцерамид. Молекулы CD1a, CD1b и CD1c экспрессируются на поверхности дендритных клеток, моноцитов и макрофагов, причем у человека CD1c служит маркером всей популяции дендритных клеток, а CD1а — клеток Лангерганса. CD1d в малом количестве экспрессируется на дендритных клетках (кроме клеток Лангерганса), моноцитах и макрофагах.
Неполиморфные CD1 молекулы, подобные молекулам МНС I класса, являются новой системой, презентирующей гликолипидные антигены Т-лимфоцитам. Они участвуют в иммунитете к микобактериям туберкулеза и имеют отношение к врожденному иммунитету, аутотолерантности и противоинфекционному иммунитету, особенно к гликолипидным антигенам, появляющимся при стрессе, повреждении тканей и инфекции.
Т-лимфоциты с рецептором γ δ для антигена (Тγδ)
[править]Субпопуляции нормальных киллеров
[править]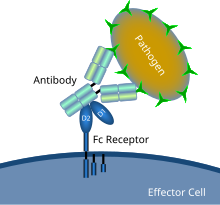
Нормальные киллеры или NK (от англ. natural killer ) - это большие зернистые лимфоциты с характерной морфологией: основная часть обильной цитоплазмы содержит несколько митохондрий , свободные рибосомы с отдельными элементами шероховатого эндоплазматического ретикулума , аппарат Гольджи и характерные электроноплотные гранулы, связанные с мембраной. Большие зернистые лимфоциты с активностью нормальных киллеров выполняют цитотоксические функции, также как и цитотоксические T- лимфоциты.
Основная обязанность киллерных клеток - выявлять и уничтожать собственные клетки организма, в которых что-то нарушилось: они убивают опухолевые клетки и клетки, зараженные вирусами (а также, возможно, и другими чужеродными агентами). Нормальные киллеры (НК-клетки) у человека составляют примерно 5% лимфоцитов периферической крови. Чаще всего они имеют фенотип CD3-CD16+CD56+CD94+ и гаметное (неперестроенное) расположение генов. Существует две субпопуляции NK-клеток: с высоким уровнем экспрессии CD56 и с низким уровнем экспрессии CD56. Первая субпопуляция в большей степени специализирована на осуществлении цитотоксической функции, а вторая – на продукции цитокинов. Таким образом, хотя НК относятся к лимфоидным клеткам, они лишены маркеров Т- и В-лимфоцитов.
NK-клетки не проходят дифференцировку в тимусе, они выходят из костного мозга в кровь и затем мигрируют в ткани, где осуществляют врожденную иммунную защиту, называемую естественной цитотоксичностью, которая особенно важна для защиты организма от вирусов и опухолей.
Во время инфекции или опухолевого роста NK-клетки привлекаются в очаг патологии и активируются цитокинами и хемокинами, секретируемыми другими клетками врожденного иммунитета, в первую очередь гранулоцитами, или вирус-инфицированными клетками других тканей в очаге инфекции. Особенно важную роль в этом играют интерфероны I типа (IFN-α IFN-β), ИЛ-15 и ИЛ-12. IFN-ы I типа, которые продуцируются клетками многих типов в ответ на инфицирование вирусами, являются сильными активаторами NK-клеток, включая клеточно-опосредованную неспецифическую цитотоксичность и продукцию ими цитокинов.
Активированные NK-клетки синтезируют также TNF-α (индуцирующий апоптоз клеток-мишеней), ИЛ-24 (аутокринно индуцирующий синтез TNF-α и IFN-γ), ИЛ-32 (член семейства ИЛ-1, провоспалительный цитокин и индуктор синтеза TNF-α), а также ИЛ-13 и ИЛ-26 (член семейства ИЛ-10), которые являются противовоспалительными цитокинами, подавляют Тх1-ответ и стимулируют синтез IgE.
Одной из характеристик НК является наличие Fc-рецептора .
Цитотоксическое действие NK-клеток на клетки-мишени
[править]NK-клетки оказывают цитотоксическое действие на опухолевые и инфицированные вирусами клетки с помощью механизмов, сходных с теми, которые используют CD8+ЦТЛ.
В цитоплазме NK-клеток содержатся многочисленные гранулы, содержащие перфорин и грэнзимы. В отличие от CD8+ЦТЛ, у которых формирование гранул происходит после их активации, NK-клетки и в покоящемся состоянии содержат в своей цитоплазме секреторные гранулы. Поэтому морфологически они представляют собой большие гранулярные лимфоциты. После прикрепления NK-клетки к клетке-мишени с помощью соответствующих рецепторов в клетку поступает достаточно сильный активационный сигнал, и она отвечает дегрануляцией. В месте межклеточного контакта выделяются перфорин и грэнзимы, которые вызывают апоптоз клетки-мишени (аналогично CD8+ЦТЛ). В отличие от CD8+ЦТЛ, синтезирующих TNF-β (лимфотоксин), NK-клетки продуцируют TNF-α, который также содержится в секреторных гранулах и может индуцировать апоптоз клеток-мишеней, экспрессирующих на своей поверхности рецепторы к этому цитокину.
Возможна также прямая клеточная цитотоксичность, не опосредованная действием цитокинов. Она обусловлена тем, что NK-клетки содержат на своей поверхности Fas-лиганд (мембраносвязанная форма TNF) и легко индуцируют апоптоз клеток-мишеней, экспрессирующих на своей поверхности Fas-рецепторы
Необходимо отметить, что распознавание клеток-мишеней NK-клетками не рестриктировано по белкам МНС. Поэтому во многих случаях цитотоксическая активность этих клеток одинакова как по отношению к сингенным, так и к аллогенным опухолям. Кроме того, цитотоксическая активность NK-клеток не снижается при уменьшении экспрессии белков МНС I класса, характерном для некоторых опухолей.
Как уже упоминалось, NK-клетки с фенотипом CD56+16+, имеющие на своей поверхности Fc-рецепторы к IgG, участвуют в осуществлении антителозависимой клеточной цитотоксичности (АЗКЦТ). IgG своими Fab-фрагментами связывается с антигенными детерминантами на поверхности клеток-мишеней, а с помощью Fc-фрагмента прикрепляется к Fc-рецептору на поверхности NK-клеток. В результате через Fc-рецептор стимулируется дегрануляция этих клеток. Выделяющиеся перфорин, грэнзимы и TNF-α индуцируют гибель антигенно чужеродных клеток. Показано, что большинство NK-клеток способны участвовать в АЗКЦТ.
Этот механизм сочетает в себе элементы адаптивного (участие антител) и врожденного (участие NK-клеток) иммунитета. Помимо NK-клеток, в АЗКЦТ могут участвовать и другие клетки системы врожденного иммунитета – макрофаги, нейтрофилы и эозинофилы. При дегрануляции, индуцированной через Fc-рецепторы, нейтрофилы, эозинофилы и отчасти макрофаги выделяют литические ферменты, разрушающие мембраны клеток-мишеней. Гранулы макрофагов содержат также TNF-α, индуцирующий апоптоз.
NK-клетки вовлечены в раннюю фазу иммунного ответа на инфицирование вирусами и внутриклеточными бактериями. Активность этих клеток стимулируется IFN-α, IFN-β и ИЛ-12, которые выделяются инфицированными клетками, а также активированными через Толл-подобные рецепторы макрофагами и дендритными клетками. В случае вирусной инфекции уровень этих цитокинов быстро повышается, за ним следует повышение числа NK-клеток в очаге инфекции, достигая максимума на 3-й день. Они сдерживают прогрессирование инфекции, пока не произошло образование CD8+ЦТЛ. После того, как численность CD8+ ЦТЛ достигает максимума (на 7-10 день после инфицирования), титр вируса быстро снижается (до 0 на 11-12 день).
Это свидетельствует о том, что NK-клетки являются первой линией защиты против вирусов (убивая инфицированные клетки и подавляя их размножение с помощью IFN-γ) в течение времени, необходимого для активации, пролиферации и дифференцировки пЦТЛ в CD8+ЦТЛ. При этом NK-клетки с помощью IFN-γ способствуют индукции адаптивного иммунного ответа, так как данный цитокин стимулирует дифференцировку Тх1, которые являются ключевыми клетками, вызывающими формирование пула эффекторных CD8+ЦТЛ.
Рецепторы, с помощью которых NK-клетки детектируют клетки-мишени
[править]
NK-клетки осуществляют распознавание потенциальных клеток-мишеней, используя специальные клеточные рецепторы, с помощью которых они опознают аномалии клеточной поверхности, такие как снижение или отсутствие экспрессии молекул МНС I класса, необычный профиль поверхностных антигенов, экспрессированных на некоторых опухолевых и инфицированных вирусами клетках, а также повышенное содержание индуцированных клеточным повреждением молекулярных мишеней на клеточной поверхности.
Детектирование клеток-мишеней NK-клетки осуществляют с помощью двух типов рецепторов – активационных и ингибиторных.
Осуществление цитотоксического действия на опухолевые и инфицированные вирусами клетки требует прямого контакта атакующих NK-клеток и клеток-мишеней. Для этого NK-клетки должны обладать механизмом, направляющим их цитотоксическое действие на аномальные клетки и защищающим нормальные. Выполнение этого двойного требования и обеспечивается двумя наборами рецепторов: ингибиторными и активационными.
Ингибиторные рецепторы подавляют цитоксическое действие NK-клеток путем связывания с белками МНС I класса или другими поверхностными молекулами, постоянно экспрессирующимися на нормальных здоровых клетках.
Активационные рецепторы, напротив, индуцируют цитотоксическое действие NK-клеток путем связывания с молекулярными структурами, которые индуцируются клеточным повреждением или кодируются встроенными в геном клетки-мишени генами вирусов или онкогенами.
У человека ингибиторные и активационные рецепторы относятся к суперсемейству иммуноглобулинов и называются KIR-рецепторами (от Killer cell-Ig-like Receptors). KIR-рецепторы — трансмембранные гликопротеины cдвумя или тремя внеклеточными иммуноглобулинподобными доменами (KIR2D и KIR3D, соответственно) и длинным (L) или коротким (S) цитоплазматическим участком. Рецепторы с L-участками проводят ингибирующий сигнал, а с S-участками — активирующий. Лигандами для KIR-рецепторов являются антигены HLA I класса, экспрессирующиеся почти на всех ядросодержащих клетках организма. KIR-рецепторы NK-клеток являются разновидностью так называемых паттерн-распознающих рецепторов (ППР) врожденного иммунитета, к которым также относятся Толл-подобные рецепторы и NOD-рецепторы.
ГЕНЕТИКА И НОМЕНКЛАТУРА KIR-СИСТЕМЫ
KIR-рецепторы кодируются генами, расположенными в 19-й паре хромосом(19q13.4) и занимает участок протяженностью 100 – 200 Kb лейкоцитарного рецепторного комплекса — LRC. В их составе содержится 2 или 3 внеклеточных домена и несколько внутриклеточных, с помощью которых (в зависимости от их структуры) KIR-рецепторы могут подавлять или активировать цитотоксичность NK-клеток. У мышей аналогом KIR-рецепторов являются лектиноподобные рецепторы.
К настоящему времени идентифицировано 15 KIR-генов (13 экспрессируемых, 2 псевдогена), а также анцестральный KIR3DL0, картируемый за пределами KIR-локуса. Существуют «структурные» или «рамочные» (framework) гены, которые присутствуют во всех гаплотипах. Структурный ингибирующий ген KIR3DL3 расположен с центромерного конца, KIR3DL2— с теломерного, а в центре региона структурную функцию выполняют псевдоген KIR3DP1 и ген KIR2DL4. Гены разделены между собой последовательностями длиной около 2 kb. Удлиненная последовательность (14kb) слева от гена KIR2DL4 разделяет центромерную и теломерную области и является сайтом наиболее частой реципрокной рекомбинации — механизма для формирования новых гаплотипов. При этом, гены KIR2DL1-3(кодирующие рецепторы, лигандами для которых являются HLA-C) расположены в центромерной части локуса, тогда как гены KIR3DL1(лиганд — HLA-B) и KIR3DL2(лиганд — HLA-A) находятся в теломерной части. Внутри каждой из частей отмечается высокое неравновесное сцепление генов.
Номенклатуру генов, кодирующих KIR-рецепторы, определяет HUGO Genome Nomenclature Committee (HGNC). В первом докладе HGNC было названо 87 аллелей KIR-генов. На настоящий момент известно более 600 аллелей, которые кодируют свыше 300 уникальных белковых последовательностей . Названия, присвоенные KIR-генам, отражают строение молекул и основаны на двух характеристиках: количестве внеклеточных иммуноглобулинподобных доменов и длине цитоплазматического участка:
- KIR2DL– двухдоменный ингибирующий рецептор;
- KIR2DS– двухдоменный активирующий рецептор;
- KIR3DL– трехдоменный ингибирующий рецептор;
- KIR3DS– трехдоменный активирующий рецептор.
KIR-генотип состоит из двух гаплотипов, один из которых наследуется от отца, а другой от матери. В зависимости от количества и типа генов выделяют две группы гаплотипов: А и В. Они различаются по количеству активирующих и ингибирующих KIR-генов. Число генов, представленных в одном гаплотипе, может варьировать от 7 (в редких случаях — 5) до 12, и зависит преимущественно от наличия или отсутствия активирующих KIR .
А-гаплотипы содержат только один активирующий ген (KIR2DS4), пять ингибирующих (KIR2DL1/3, 3DL1/2/3) и KIR2DL4, который обладает как активирующими, так и ингибирующими свойствами. Для этого гаплотипа характерен высокий уровень аллельного полиморфизма. В-гаплотипы характеризуются присутствием более чем одного активирующего гена, более вариабельны по количеству генов, но имеют более низкий уровень аллельного полиморфизма. Они содержат от одного до пяти активирующих KIR-генов (KIR2DS1/2/3/5 и KIR3DS1) и могут включать ингибирующие гены, отсутствующие в гаплотипах группы А (KIR2DL2и 2DL5)
ВЗАИМОДЕЙСТВИЕ С АНТИГЕНАМИ HLAI КЛАСС
Двухдоменные KIR-рецепторы связываются с антигенами HLAлокуса С (за исключением KIR2DL4), трехдоменные — локусов A и B.
Несмотря на то, что KIR-рецептор связывается с тем же участком молекулы HLA, что и Т-клеточный рецептор (TCR), эти взаимодействия имеют качественные различия. В то время как связывание с молекулой HLA I класса приводит к конформационным изменениям в TCR, KIR и HLA взаимодействуют как «жесткие тела». Вследствие этого данное лиганд-рецепторное взаимодействие чрезвычайно чувствительно к единичным аминокислотным заменам в домене D1 KIR-рецептора и α1-цепи HLA-лиганда.
Активация NK-клеток определяется суммарным воздействием на эти клетки активационных и ингибиторных рецепторов, величина этой активации определяется динамическим балансом активирующих и ингибирующих сигналов, обеспечиваемых через эти рецепторы.
Ингибиторные KIR-рецепторы распознают различные варианты полиморфных молекул МНС I класса, а также подобные им по строению вирусные белки. Так как практически все клетки экспрессируют молекулы МНС I класса, ингибирование цитотоксической функции NK-клеток через эти рецепторы является одним из наиболее важных механизмов для предотвращения разрушения нормальных клеток организма NK-клетками. Снижение или полное отсутствие экспрессии молекул МНС I класса (характерное для опухолевых клеток и клеток, инфицированных некоторыми вирусами, которые блокируют эту экспрессию) уменьшает или полностью отменяет ингибирующий сигнал. Это смещает баланс в сторону преобладания активационных сигналов, что стимулирует цитотоксичность NK-клеток.
Таким образом, активационный порог NK-клеток в конечном счете определяется уровнем экспрессии молекул МНС I класса на клетках хозяина. Клетки, экспрессирующие нормальные уровни неизмененных молекул МНС I класса, как правило, избегают всех видов цитотоксического действия NK-клеток.
Активационные KIR-рецепторы более многочисленны, чем ингибиторные. Основные активационные рецепторы NK-клеток распознают либо собственные модифицированные повреждением молекулы, либо белки, кодируемые вирусными генами или онкогенами.
Одной из важных групп индуцированных клеточным повреждением лигандов активационных KIR-рецепторов являются молекулы МНС I класса, экспрессия которых нарушена повреждением или стрессом, а также связанные с молекулами МНС I класса стресс-индуцированные белки.
Другая группа лигандов представлена вирусными белками (такими как гемагглютинины вируса гриппа), продуктами онкогенов, а также пептидами патогенов, например, M. tuberculosis. В этой роли могут также выступать МНС-подобные вирусные белки.
Дополнительные сигналы, активирующие NK-клетки, могут быть обеспечены цитокинами, в первую очередь IFN-α,β, TNF-α, ИЛ-12 и ИЛ-15. Активации NK-клеток при вирусной инфекции может способствовать также наличие TLR3 рецепторов в их цитоплазме.
Активация Т-лимфоцитов
[править]Что такое активация лимфоцита
[править]Апоптоз и торможение активации
[править]==== Апоптоз ====гибель клетки.
Торможение активации
[править]Иммунорецепторы :активирующие рецепторы и негативные корецепторы лимфоцитов
[править]Иммунный ответ
[править]Определение иммунного ответа. Этапы иммунного ответа
[править]Механизмы врождённого иммунитета не всегда могут сдержать развитие инфекции. В таких случаях запускается адаптивный иммунный ответ. В отличие от врождённого иммунитета, реализуемого клетками, сформировавшимися в процессе онтогенеза независимо от контакта с патогенными микроорганизмами, адаптивный иммунный ответ развивается только в ответ на контакт с конкретным антигеном. При этом в иммунный ответ вовлекаются только клоны лимфоцитов, распознающие проникшие в организм чужеродные антигены. Эта специфическая адресная реакция называется иммунным ответом. Таким образом, иммунный ответ - многоэтапный процесс с обязательным участием лимфоцитов и других клеток иммунной системы.
Основные задачи иммунного ответа:
• распознавание лимфоцитами антигена в нативном состоянии (например, молекулы патогена) и представленного на поверхности модифицированных клеток (например, заражённых вирусами);
• деструкция патогена и повреждённых клеток;
• элиминация (выведение) продуктов деструкции из организма;
• формирование иммунной памяти.
В иммунном ответе выделяют индуктивную и эффекторную (продуктивную) фазы. В индуктивную фазу происходит презентация антигена, т.е. передача информации об антигене от клеток врождённого иммунитета (АПК) инициаторам адаптивного иммунитета - Т-хелперам. Затем выбирается путь дальнейшего развития иммунного ответа по клеточному или гуморальному пути: через индукцию дифференцировки разновидностей Т-хелперов (Th1, Th2, Th17 и других, см. ). Наконец, при участии этих Т-хелперов происходит параллельная дифференцировка эффекторных клеток и клеток памяти. Эффекторная фаза иммунного ответа состоит в выполнении своих функций образовавшимися эффекторными клетками. Эта активность реализуется в форме клеточной или гуморальной иммунной защиты. В конце иммунного ответа благодаря включению регуляторных механизмов прогрессирование иммунных реакций замедляется и в результате приводит к их прекращению. Дифференцировавшиеся в процессе иммунного ответа клетки памяти активируются только при повторной встрече с антигеном - при вторичном иммунном ответе. Он протекает в принципе так же, как первичный, но развивается быстрее и реализуется значительно эффективнее первичного .
Иммунологическая память
[править]Взаимодействия клеток в иммунном ответе
[править]Молекулы межклеточной адгезии
[править]Антигенпредставляющие клетки
[править]- Макрофаг. Способен загружать антигенные эпитопы только на HLA 2 типа. Как правило фагоцитирует только крупные антигенные объекты( внутриклеточно расположенные вирусы, грибы, бактерии, простейшие). Участвует в CD4+T – клеточном ответе. Потом становится ядром – центром гранулемы – иммунного воспаления. Активируется CD4+T cells.
Макрофаги играют важную роль в естественном иммунитете и адаптивных иммунных ответах. Они могут фагоцитировать микробы, иммунные комплексы и клетки-мишени, захватывать, процессировать и представлять антигены Т-клеткам, а также секретировать многочисленные продукты: цитокины, белки комплемента, протеиназы, метаболиты арахидоновой кислоты, NO и др. кислородные радикалы. Макрофаги участвуют в дифференцировке Тh1 за счёт секреции IL12. Существуют циркулирующие и фиксированные (резидуальные) макрофаги. Активация макрофагов обеспечивается Тh1 (IFN), а инактивация - Тh2 (IL10). Специализированные формы резидуальных макрофагов:- Kupffer’s cells (печень) Macrophages селезёнки Pulmonary alveolar macrophages (лёгкие) Multinucleate giant cell (грануломы при ГЗТ)
- Дендритные клетки. Профессиональные антигенпредставляющие клетки. Они способны загружать антигенные эпитопы на HLA1 and HLA2. Захватив антигенный материал пиноцитозом, могут его долго кумулировать до встречи с лимфоцитом соответствующего клона, у которого BCR or TCR будет подходить к клеткам этого типа.
Дендритные клетки представляют гетерогенную популяцию клеток, участвующих в эндоцитозе, процессинге и представлении антигенов лимфоцитам. Существуют зрелые и незрелые дендритные клетки (ДК), а также несколько отличающихся морфологических и функциональных типов. -МОРФОЛОГИЧЕСКИЕ ТИПЫ ДЕНДРИТНЫХ КЛЕТОК:Клетки Лангерганса (в эпидермисе, эпителии слизистых) Интерстициальные ДК (под эпителием)Плазмацитоидные (под эпителием) Интердигитативные ДК (в Т-зонах: паракортикальных областях лимфоузлов и парафолликулярных регионах МАЛТ)Тимические ДК (в тимусе; близки к интердигитативным ДК) -ФУНКЦИОНАЛЬНЫЕ ТИПЫ ДЕНДРИТНЫХ КЛЕТОК: 1. Т-клеточные ответы Миелоидная (моноцитарная) дендритная клетка (тип 1) генерирует из миелоидного предшественника, секретирует IL6, IL12, IFNа, TNFб, способствует пролиферации Тх1 и стимулирует Т- клеточные иммунные ответы. К этой группе относятся клетки Лангерганса, интерстициальные (CD11c+) и интердигитативные клетки (CD40+). Клетка Лангерганса (CD1+, CD207+) содержит лангерин (в гранулах Birbeck) и присутствует в эпидермисе кожи (ДАЛТ), крайней плоти у мужчин и эпителии многих слизистых оболочек (МАЛТ). 2. В-клеточные ответы Плазмацитоидная (лимфоидная) дендритная клетка (тип 2) – минорная субпопуляция (1%), генерирует из лимфоидного предшественника дендритной клетки, секретирует IFNа/IFNб, IL4, IL10, участвует в В-клеточных иммунных ответах. Маркёрами плазмацитоидных клеток (pDC) являются CD303 и CD304.
- В – лимфоцит. Способен загружать антигенные эпитопы только на HLA2 and CD1. Пиноцитируют бактериальные токсины, белки и фосфолипиды( загружаются на CD1). Участие этих клеток ограничено только гуморальным ответом. Антигеннезависимая дифференцировка В-клеток (коммиттмент) начинается в печени плода, продолжается в костном мозге, стартуя на 10-й неделе эмбриогенеза и протекая в течение всей жизни как в костном мозгу, так и МАЛТ.
Основные черты В-лимфопоэза: 1. Экспрессия специфического BCR - маркёра В-клона, ассоциированных молекул Ig(CD79a)/Ig(CD79b) и корецепторов (CD21/CD19/ CD81/CD225). 2. Селекция («экзамен») в ходе дифференцировки: - положительная селекция - отбор и выпуск в кровоток клонов, способных к распознаванию собственных HLA и экзоантигенов; - отрицательная селекция: а) aпоптоз клонов, направленных против мембранных аутоантигенов; б) анергия клонов, направленных против растворённых аутоантигенов. 3. Cпособность дифференцироваться в плазматические клетки в ходе гуморальных (В-клеточных) адаптивных иммунных ответов.
Цитокины
[править]Цитокины.Это белки с небольшой молекулярной массой, образуются в клетках иммунной системы. Главным образом – в лимфоцитах( фабрика цитокинов). Также образуются в печени, клетках ЦНС, эпителии. Действуют подобно гормонам иммунной системы. Действие цитокинов в основном паракринное или аутокринное. Только три цитокина имеют эндокринный эффект: IL1, IL6,TNF Историческая группировка цитокинов. 1.интерлейкины( описано 27) 2.интерфероны – IFNα,β,γ. IFNα,β – относят к 1 – ому типу, IFNγ – относят ко 2 – ому типу. 3.колониестимулирующие факторы( лейкопоэтины)
•макрофагальный – M – CSF
•моноцитарно – гранулоцитарный – G – MCSF
•гранулоцитарный – G – CSF
4.фактор некроза опухолей – TNFαβ 5.хемокины – очень много( классификация на сайте). Общие свойства цитокинов. 1.плейотропность и многофункциональность 2.аутокринный и паракринный, реже - эндокринный способ действия. 3.взаимозаменяемость и синергизм среди одних и антагонизм среди других 4.провоспалительный или противовоспалительный эффекты 5.кратковременность эффекта шединг – слущивание рецепторов. Функциональные профили цитокинов.
- Провоспалительные – IL1α, IL1β, IL6, IL8, IL12, IL18, IFNγ, TNFα,β, G – MCSF
- ротивовоспалительный профиль – рецепторный антагонист IL1; IL10, TFRβ, IFNα,β.
- IL4 – мощный провоспалительный цитокин для атопиков, но в очаге воспаления 4 типа он мощный противовоспалительный фактор( по Джелу - Кумбсу).
- Ростовые факторы – IL7 – для раннего лимфопоэза
По модели генетического нокаута у мышей по IL7 дает картину тотального иммунодефицита IL2 – для позднего лимфопоэза, для прайминга
- Пирогенные факторы: IL6, IL1, TNFα,β, IFNα,β,γ.
- Хемокины – IL8, макрофагальные хемоаттрактантные белки(MCP1 - 5), макрофагальные воспалительные белки( MIP1 - 3), Rantes.
Ключевые цитокины для отдельных клеток:
- IL9.Вырабатывается CD4+ лимфоцитами. Один из ключевых факторов для пролиферации и дифференцировки тучных клеток. Стимулирует тромбоцитарный росток. Очень активен при мегакариоцитарном лейкозе
- IL12.Вырабатывается антиген – представляющими клетками. Ключевой фактор дифференцировки Th1 из Th0. Индуцирует продукцию IFNγ Т – лимфоцитами и NK – клетками, активирует NK – клетки.
В модели с генетическим нокаутом отсутствуют Th1.
- IL4.Вырабатывается Th2, тучными клетками, костномозговыми стволовыми клетками. СТИМУЛИРУЕТ РОСТ И ДИФФЕРЕНЦИРОВКУ Th2. Индуцирует пролиферацию В – лимфоцитов и переключение на синтез IgE, IgG4. В модели с генетическим нокаутом отсутствуют Th2, снижена концентрация IgE.
- IL8.Вырабатывается очень многими клетками – макрофагами, фибробластами, эндотелиоцитами.
Регулируют активность нейтрофилов( хемотаксис, поглощение, участие в воспалении). Стимулирует новообразование капилляров, что способствует метастазированию опухоли. В модели с генетическим нокаутом – нейтропения.
- IL5.Вырабатывается Th2, тучными клетками, эозинофилами. Ключевой фактор роста и созревания эозинофилов. В модели с генетическим нокаутом снижено количество эозинофилов, IgE, подавление поздней фазы атопического воспаления
-клетки – активаторы макрофагов IFNγ
23. Основные Интерлейкины.
- IL1. Существуют IL1α, IL1β, IL1ra(рецепторный антагонист).
В модели с генетическим нокаутом у животных невозможно развитие острофазной реакции. Эти интерлейкины вырабатываются большинством клеток иммунной системы, но основные продуценты – макрофаги, эндотелиоциты, фибробласты, нейтрофилы. Эти интерлейкины многофункциональны:•стимулируют все фазы иммунного ответа•воспаления •вызывают лейкоцитоз•в больших концентрациях вызывают инфекционно – токсический шок •стимулируют острофазную реакцию IL1α – мембрансвязанная форма IL1β – свободносекретируемая молекула, которая попадает в интрацеллюлярное пространство IL1ra – связываясь с рецептором для IL1α,β, ингибирует активность IL1α,β.
- IL2.Вырабатывается Т – лимфоцитами. Ключевой ростовой фактор для дифференцировки клеток в ходе иммунного ответа( при клональной экспансии), стимулирует активность NK – клеток.
В модели с генетическим нокаутом у мышей развивается иммунодефицит преимущественно по Т – звену, частично по В – звену. Рецептор для IL2(IL2R) экспрессируется на лимфоцитах и состоит из трех цепей – α( CD25), β( CD122), γ( CD132).
- IL3.Мультиколониестимулирующий фактор. Стимулирует лейкопоэз на ранних стадиях. Вырабатывается Т – лимфоцитами, тучными клетками, эпителиоцитами. У мышей с генетическим нокаутом нарушен лейкопоэз и дифференцировка эозинофилов.
- IL4.Вырабатывается Th2, тучными клетками, костномозговыми стволовыми клетками. СТИМУЛИРУЕТ РОСТ И ДИФФЕРЕНЦИРОВКУ Th2. Индуцирует пролиферацию В – лимфоцитов и переключение на синтез IgE, IgG4. В модели с генетическим нокаутом отсутствуют Th2, снижена концентрация IgE.
- IL5.Вырабатывается Th2, тучными клетками, эозинофилами. Ключевой фактор роста и созревания эозинофилов. В модели с генетическим нокаутом снижено количество эозинофилов, IgE, подавление поздней фазы атопического воспаления.
- IL6.Вырабатывается очень многими клетками. Многофункционален, дополняет активность IL1. Регулирует острофазную реакцию. В модели с генетическим нокаутом отсутствует острофазная реакция, снижается синтез IgA.
- IL7.Вырабатывается стволовыми клетками. Ключевой ростовой фактор лимфоцитов на ранних стадиях( фактор commitment). В модели с генетическим нокаутом развивается синдром «тяжелого комбинированного иммунодефицита»(SCID – severe combined immunodeficiency).
- IL8.Вырабатывается очень многими клетками – макрофагами, фибробластами, эндотелиоцитами.
Регулируют активность нейтрофилов( хемотаксис, поглощение, участие в воспалении). Стимулирует новообразование капилляров, что способствует метастазированию опухоли. В модели с генетическим нокаутом – нейтропения.
- IL9.Вырабатывается CD4+ лимфоцитами. Один из ключевых факторов для пролиферации и дифференцировки тучных клеток. Стимулирует тромбоцитарный росток. Очень активен при мегакариоцитарном лейкозе.
- IL10.Вырабатывается Th2, В – клетками, макрофагами. Блокирует образование Th1, инактивирует макрофаги, стимулирует продукцию IgA. В модели с генетическим нокаутом развивается тяжелый энтероколит и анемия, а также задержка роста животных.
- IL11.Вырабатывается костномозговыми стволовыми клетками. Стимулирует пролиферацию мегакариоцитов.
Наблюдаются большие концентрации при плазмоцитоме( миеломная болезнь).
- IL12.Вырабатывается антиген – представляющими клетками. Ключевой фактор дифференцировки Th1 из Th0. Индуцирует продукцию IFNγ Т – лимфоцитами и NK – клетками, активирует NK – клетки.
В модели с генетическим нокаутом отсутствуют Th1.
- IL13.Вырабатываются Th2. Стимулирует пролиферацию и дифференцировку В – лимфоцитов, продукцию IgM, IgE, IgG4, продлевает жизнь макрофагам.
- IL14.Вырабатывается Т – лимфоцитами.Стимулирует рост В – клеток.
- IL15.Вырабатывается макрофагами, эпителиоцитами. Эффект сходен с эффектом IL2. Активирует NK – клетки.
- IL16.Вырабатывается CD8 – Т – клетками, но рецептором для него является молекула CD4.Это хемокин для всех Т – лимфоцитов( стимулирует миграцию Т - клеток).
- IL17. Вырабатывается В – клетками памяти. Стимулирует продукцию G – CSF, IL6, 8, простагландина Е2.
- IL18. Вырабатывается макрофагами, остеобластами, гепатоцитами. Стимулирует синтез IFNγ, активирует NK – клетки, является кофактором для дифференцировки Th1.
Колониестимулирующие факторы. •GM – CSF( гранулоцитарно – моноцитарный колониестимулирующий фактор). Вырабатывается CD4 – Т – клетками, макрофагами, эндотелиоцитами. Стимулирует моно – и гранулоцитопоэз на ранних стадиях. Выраженная провоспалительная активность.В модели с генети ческим нокаутом развивается моно – и гранулоцитопения, альвеолярный протеинозис. •G – CSF. Вырабатывается макрофагами, эндотелиоцитами. Стимулирует гранулоцитопоэз. •M – CSF Вырабатывается макрофагами и эндотелиоцитами. Стимулирует моноцитопоэз.
Взаимодействие Т- и В-лимфоцитов
[править]Тимуснезависимые антигены
[править]Дихотомия (иммунное отклонение) в дифференцировке CD4+ ThO-лимфоцитов в процессе индукции иммунного ответа: развитие субпопуляций Тh1 и Th2
[править]Супрессия иммунного ответа
[править]Иммунологическая толерантность
[править]Отторжение трансплантата
[править]Иммунная система и опухоли
[править]Cправочная информация
[править]СИСТЕМА МАРКЁРНЫХ АНТИГЕНОВ CD
[править]Обозначения: (+) - экспрессия маркёра, (-) - отсутствие маркёра, (норма): экспрессия/отсутствие маркёра в норме, (патология): экспрессия/отсутствие маркёра при патологии.
CD1-50
[править]Антиген кортикальных тимоцитов и ДК - кластер, состоящий из двух подсемейств. Одно из них включает молекулы CD1a, CD1b и CD1c, другое - CD1d и CD1e. CD1 относят к суперсемейству иммуноглобулинов; является членом семейства MHC-подобных гликопротеинов класса I. CD1 состоит из тяжёлой α-цепи с молекулярной массой 45-65 кДа, нековалентно связанной с β2-микроглобулином. Число иммуноглобулиновых доменов может варьировать от 1 до 8 и контролируется 5 неполиморфными генами (1q22-q23). CD1 рестриктирует ответ T-лимфоцитов на некоторые антигены, важен для развития T-клеток. CD1+ T-клетки распознают как пептидные антигены, так и липидные антигены микобактерий (миколевые кислоты и производные липоарабиноманнана).
• CD1a (OMIM 188370). (+) - (норма): кортикальные тимоциты (70%), активированные T-клетки, клетки Лангерганса, ДК; (+) - (патология): пре-T-клетки острого лимфолейкоза с фенотипом кортикальных тимоцитов, при гистиоцитозе клеток Лангерганса, при миелолейкозе, злокачественные B-клетки, ДК кожных T-лимфом. (-) - зрелые периферические T-лимфоциты.
• CD1b (OMIM 188360). (+) - (норма): те же клетки, что и CD1a. (+) - (патология): миелолейкозы, некоторые злокачественные B-клетки. • CD1c (OMIM 188340). (+) - (норма): те же клетки, что и CD1a, и CD1b, а также субпопуляция нормальных периферических B-клеток. CD1c+ T-клетки дополнительно распознают микобактериальные гексозил-1-фосфоизопреноиды и маннозил-Р1фосфодолихолы. (+) - (патология): миелолейкозы и некоторые B-клеточные опухоли. • CD1d (OMIM 188410). (+) - эпителиальные клетки пищеварительного тракта и NKT-лимфоциты, B-лимфоциты и ДК. • CD1e (OMIM 188411). (+) - ДК.
CD2
LFA-2 (Lymphocyte Function-Associated antigen 2) - антиген 2, ассоциированный с функцией лимфоцитов, рецептор E-розеткообразующих клеток, рецептор для эритроцитов барана (OMIM 186990; 1p13.1). Молекулярная масса 50 кДа. Поверхностный антиген 95% тимоцитов, 99% зрелых периферических T-лимфоцитов, 80-90% NK-клеток, 50% редких тимических B-лимфоцитов. Функции: в качестве молекулы адгезии взаимодействует с лигандом CD58 (LFA-3) АПК, участвует в альтернативной активации T-клеток; регулирует T- и NK-опосредованный цитолиз, ингибирует апоптоз активированных периферических T-лимфоцитов. (+) - тимоциты, T-клетки, NK-лимфоциты.
• CD2R - CD2-эпитоп активированных T-лимфоцитов. (+) - активированные T-клетки. • CD2AP (CMS) - ассоциированный с CD2 белок AP (OMIM 604241, хромосома 6) - связывается с цитоплазматическим концом CD2. Необходим для передачи внеклеточных сигналов к цитоскелету. • CD2BP1 (PSTPIP) - связывающий CD2 белок 1 (OMIM 606347; 15q24-q25.1) - участвует в регуляции активности онкогена ABL. • CD2BP2 - связывающий CD2 белок 2 (OMIM 604470) - необходим для связывания CD2 с CD58.
CD3
Входит в состав αβTCR и γδTCR; принадлежит к суперсемейству иммуноглобулинов; состоит из четырёх полипептидных цепей: димера цепей e (масса каждой цепи 20 кДа), цепей у (25-28 кДа) и 5 (20 кДа). Эти цепи нековалентно связаны между собой, а также с димерами TCR и двумя ζ-цепями рецептора. Контролируется расположенным в локусе 11q23 тесно сцепленным кластером генов. Цитоплазматический хвост цепей CD3 содержит по одному домену ITAM, фосфорилирование которых индуцирует возникновение внутриклеточного активирующего сигнала и передачу его по сигнальному пути к клеточному ядру. Фосфорилирование осуществляется связанными с рецепторным комплексом киназами Fyn и Lck, активирующимися в результате взаимодействия лиганд-TCR. (+) - тимоциты, периферические T-лимфоциты (60- 80%), NKT-клетки, большинство клеток хронического T-клеточного лейкоза, 70% клеток острого T-клеточного лейкоза.
• CD3G (у) (OMIM 186740). • CD3D (5) (OMIM 186790). • CD3E (e) (OMIM 186830).
CD4
Мономерный трансмембранный гликопротеин суперсемейства иммуноглобулинов (OMIM 186940; 12pter-p12). Молекулярная масса 55 кДа. Содержит 4 внеклеточных домена (D1-D4), трансмембранный домен и цитоплазматический участок. Служит маркёром T-хелперов. Выполняет функции корецептора αβTCR - связываясь с инвариантным β2-доменом MHC-II, участвует в распознавании молекул процессированного антигена, презентируемого АПК. Через цитоплазматическую часть молекулы и нековалентно связанную с ней тирозинкиназу Lck участвует в трансдукции активирующего внутриклеточного сигнала. Является рецептором для ВИЧ, связываясь через домен D1 с белком вируса gp120. (+) - (норма): тимоциты (80-90%), зрелые T-лимфоциты (65% T-хелперов), моноциты, макрофаги, клетки Лангерганса, ДК. (+) - (патология): некоторые опухоли T-клеточного происхождения.
CD5
Поверхностноклеточный трансмембранный гликопротеин с молекулярной массой 67 кДа (11q13); имеет цитоплазматический домен, участвующий в передаче сигнала. Относится к семейству обогащённых цистеином рецепторов-«мусорщиков» SRCR (Scavenger Receptor CysteineRich; от англ. scavenger - мусорщик), называют также - «скэвенджеррецептор». Участвует в процессах адгезии T- и B-лимфоцитов. Физически связан с антигенраспознающими рецепторами T- и В1-лимфоцитов. При формировании сигнального пути образует физическую связь между ζ-цепью TCR и внутриклеточными протеинтирозинкиназами. Лигандами для CD5 служат gp40-80, CD72, каркасная область молекул иммуноглобулинов. (+) - тимоциты, все зрелые T-лимфоциты, отдельная субпопуляция В1-лимфоцитов (В1а-клетки). • CD5L (SPa) - подобный CD5 антиген (OMIM 602592; 1q21-q23). SPa относят к рецепторам модифицированных липопротеинов (рецепторам-«мусорщикам»). Играет роль в регуляции апоптоза в макрофагах и моноцитах. (+) - лимфоидные клетки селезёнки, тимуса, клетки костного мозга, печени плода.
CD6
Одноцепочечный трансмембранный гликопротеин (11q13) молекулярной массой 105-130 кДа; имеет 3 внеклеточных домена. Служит молекулой адгезии между тимоцитами и клетками тимического эпителия. Принадлежит к семейству рецепторов-«мусорщиков». (+) - (норма): незрелые (низкий уровень) и зрелые тимоциты, большинство периферических T-клеток, часть B-лимфоцитов, некоторые нейроны. (+) - (патология): B-клетки хронического лимфолейкоза. Лиганды CD6: CD166 и ALCAM (молекула адгезии активированных лейкоцитов).
CD7
Трансмембранный и секреторный белок (17q25.2-q25.3~). Молекулярная масса 40 кДа. Принадлежит к суперсемейству иммуноглобулинов. Играет важную роль в активации T-лимфоцитов, во взаимодействии между T- и B-лимфоцитами в период раннего развития лимфоцитов. (+) - (норма): тимоциты и лимфоциты периферической крови (85%), большинство NK-клеток. (+) - (патология): маркёр T-клеточного острого лимфолейкоза.
CD8'
Корецептор αβT-лимфоцитов, маркёр ЦТЛ. Взаимодействует с инвариантным доменом α3 MHC-I при распознавании комплекса пептид- MHC. Принадлежит к суперсемейству иммуноглобулинов; существует в двух формах: гомодимерной c двумя цепями α (молекулярная масса каждой цепи 32 кДа) и гетеродимерной с цепями β (молекулярная масса 37 кДа) и α. Цепи имеют по одному внеклеточному домену, в гомо- и гетеродимерах соединены дисульфидной связью. При помощи цитоплазматической части цепей молекулы и тирозинкиназы Lck, нековалентно связанной с α-цепью, участвует в трансдукции активирующего внутриклеточного сигнала. (+) - тимоциты (90%), 25-35% зрелых периферических T-клеток (цитотоксические лимфоциты), NK-клетки (30%).
• CD8A - полипептидная α-цепь (OMIM 186910; 2p12). • CD8B - полипептидная β-цепь (OMIM 186730; 2p12).
CD9
Поверхностный трансмембранный антиген (OMIM 143030; 12p13). Существует в двух изоформах: с молекулярной массой 24 кДа и 36 кДа. Принадлежит к семейству тетраспанинов. Участвует в адгезии клеток и в активации тромбоцитов, взаимодействует с интегринами и гликопротеином Psg17 из группы специфичных для беременности белков PSG (Pregnancy-Specific Glycoproteins) семейства раково-эмбриональных антигенов; необходим также для миграции и слияния клеток (например, при оплодотворении и в миогенезе). (+) - активированные T-лимфоциты; ранние, активированные и дифференцированные B-лимфоциты; моноциты, тромбоциты, эозинофилы, базофилы, клетки эндотелия сосудов, а также в нервных структурах, мышцах, париетальном эпителии гломерул, тубулярном эпителии почек и др.
• CD9P1 (PTGFRN, FPRP) - негативный регулятор рецептора простагландина F2 (OMIM 601204; 1p13.1-q21.3) - взаимодействует с CD9 и CD81. (+) - кератиноциты и клетки слюнных желёз, а также во множестве трансформированных клеточных линий (например, HeLa).
CD10
Трансмембранный гликопротеин молекулярной массой 100 кДа (3q25.1-q25.2) (CALLA - от Common Acute Lymphocytic Leukemia Antigen - общий антиген острого лимфобластного лейкоза и его маркёр; мембранная Zn-металлоэндопептидаза [EC 3.4.24.11], нефрилизин [энкефалиназа]; нейтральная эндопептидаза NEP [от Neutral EndoPeptidase]).
Выявление CD10 подтверждает диагноз эндометриоза, лимфомы Беркитта, фолликулярной лимфомы, рака толстой кишки. (+) - (норма): кора надпочечников, пре-B-клетки, головной мозг (в том числе сосудистое сплетение), кортикальные тимоциты, строма эндометрия, клетки центров размножения лимфоидных фолликулов, гранулоциты, печень, плацента, щёточная каёмка энтероцитов. (+) - (патология): аденомиоз эндометрия, пре-B-лимфоцитарный острый лимфолейкоз (75%), бластный криз при хроническом миелолейкозе (90%), карцинома толстой кишки, дерматофиброма и дерматофибросаркома, аденокарцинома эндометрия, опухоли стромы эндометрия, рак желудка, глиомы, гепатоцеллюлярная карцинома, аденокарцинома поджелудочной железы, меланома, опухоли производных мезонефроса, мюллеровых и вольфовых протоков, опухоли почек и простаты, рабдомиосаркома, шваннома, миома и миосаркома матки.
CD11
Группа поверхностноклеточных рецепторов (ITGA, интегрины a), осуществляющих адгезию лейкоцитов между собой и к межклеточному матриксу. ITGA - гетеродимеры, состоящие из нековалентно связанных цепей - лёгкой, идентичной Р-цепи (CD18), и разных тяжёлых a-цепей, обозначаемых как CD11a, CD11b, CD11c и CD11d; их гены локализованы в локусе 16p11.2.
• CD11a (ITGAL) - белок с внеклеточной, трансмембранной и цитоплазматической частями. Молекулярная масса 180 кДа. Принадлежит к семейству β2-интегринов (αLβ2), является субъединицей αL интегрина LFA-1 (LFA1A, OMIM 153370). Он опосредует большинство иммунных, воспалительных и эффекторных реакций, обеспечивает адгезию (в комплексе с CD18; комплекс «CD11a/ CD18») ЦТЛ к их мишеням. (+) - все лейкоциты, включая T- и B-лимфоциты, макрофаги, нейтрофилы, эозинофилы. Лиганды: ICAM-1 (CD54), ICAM-2 (CD102), ICAM-3 (CD50).
• CD11b (ITGAM) - субъединица αM рецептора CR3 для компонента комплемента iC3b (Mac-1, Mo1A, интегрин CR3, рецептор для iC3b, CR3A) (OMIM 120980). Молекулярная масса 165 кДа. Принадлежит к семейству β2-интегринов (αMβ2). Обеспечивает адгезию нейтрофильных лейкоцитов между собой и к поверхности эндотелия, а также фагоцитоз частиц, опсонизированных iC3b. Лиганды: фибриноген, фактор свёртывания X, ICAM-1 (CD54), Saccharomyces cerevisiae, Staphylococcus epidermidis, Histoplasma capsulatum. (+) - (норма): ФДК, моноциты, макрофаги, гранулоциты, некоторые NK-клетки, некоторые B- и T-лимфоциты; (+) - (патология): клетки острого миелолейкоза: M1-M3 (35-70%), M4-M5 (80- 90%), волосатоклеточный лейкоз (99%).
• CD11c (ITGAX) - белок с внеклеточной, трансмембранной и цитоплазматической частями. Молекулярная масса 150 кДа. Является субъединицей αX рецептора CR4 для компонента комплемента iC3b (интегрин CR4, рецептор для iC3b) (OMIM 151510). Принадлежит к семейству β2-интегринов (αxβ2). CD11c участвует в удалении опсонизированных частиц и иммунных комплексов, связывается с фибриногеном, необходим для адгезии макрофагов и нейтрофилов к эндотелию. Лиганды: iC3b, CD23, ICAM-1 (CD54), фибронектин. (+) - (норма): 50% активированных CD4/CD8+ T-клеток, гранулоциты, моноциты, макрофаги, ДК и NK-клетки. (+) - (патология): клетки острого миелолейкоза - M4-M5 (50%), волосатоклеточный лейкоз (99%), B-лимфоцитарный хронический лимфолейкоз (хороший прогноз).
• CD11d (ITGAD) - субъединица αD семейства β2-интегринов (αDβ2) (OMIM 602453), связывает CD50.
CDw12
Фосфопротеин молекулярной массой 150-160 кДа. (+) - гранулоциты, моноциты, NK-клетки, тромбоциты.
CD13
GP150. Поверхностный антиген лейкоцитов GP150, аминопептидаза N-PEPN (EC 3.4.11.2; OMIM 151530; 15q25-q26). Рецептор некоторых коронавирусов - возбудителей инфекционных заболеваний верхних дыхательных путей. Дефекты GP150 приводят к развитию лейкозов/ лимфом; аутоантитела к CD13 вовлечены в развитие хронической реакции «трансплантат против хозяина» после трансплантации костного мозга. (+) - ранние предшественники моноцитов и гранулоцитов, эндотелий, фибробласты, остеокласты; микроворсинки энтероцитов, эпителия канальцев почки, плаценты, жёлчных ходов; синаптические мембраны, периневрий; антиген миелоидных клеток (CD33 более специфичен). (+) - (патология): острый миелолейкоз: M1-M5 (75-95%), M6 (обычно); хронический миелолейкоз (90%); острый лимфолейкоз: пре-B-клетки (10%), пре-T-клетки (редко).
CD14
Рецептор для ЛПС, эндотоксинов (OMIM 158120; 5q31). Связывание ЛПС и CD14 через LBP (LPS Binding Protein - ЛПС-связывающий белок) приводит к активации макрофагов и секреции цитокинов. CD14 существует также в растворимой форме в сыворотке крови, оказывая провоспалительное действие. (+) - макрофаги/моноциты (90%), слабая экспрессия: гранулоциты, клетки Лангерганса, ДК, B-лимфоциты. (+) - (патология): B-лимфоцитарный хронический миелолейкоз (90%), фолликулярная лимфома (80%), диффузная крупноклеточная B-лимфома (40%), острый миелолейкоз: M4/M5 (50-90%).
CD15
Концевой разветвлённый трисахарид, входящий в состав гликолипидов и многих гликопротеинов клеточной поверхности (OMIM 104230; 11q21). Молекулярная масса 46 кДа. (+) - миелоидные клетки (90%), активированные B- и T-клетки (в том числе при инфекционном мононуклеозе), эозинофилы; клетки Рид-Штернберга. (+) - (патология): 20% клеток T-лимфом, 5% клеток B-лимфом.
• CD15s - лиганд CD62P и CD62E. (+) - гранулоциты и макрофаги. • CD15u - сульфатированный CD15.
CD16
Трансмембранный белок молекулярной массой 50-80 кДа суперсемейства иммуноглобулинов - низкоаффинный рецептор для Fcфрагмента IgG III (FcγRIII) (OMIM 146740; 1q23). Экспрессируется на нейтрофилах, макрофагах, эозинофилах, NK-клетках. Опосредует фагоцитоз, антителозависимую клеточную цитотоксичность.
• CD16a (FcγRIIIA). (+) - NK-клетки (10-20%), гранулоциты, моноциты (редко), альвеолярные макрофаги, некоторые T-лимфоциты. (-) - миелодиспластический синдром. • CD16b (FcγRIIIB). (+) - нейтрофилы.
CD17
Гликосфинголипид семейства лактозилцерамидов, связывает бактерии. Молекулярная масса 150-160 кДа. (+) - нейтрофилы, макрофаги/ моноциты, тромбоциты, базофилы, B-клетки (CD19+), ДК миндалин.
CD18
Лёгкая β2-цепь семейства интегринов молекулярной массой 95 кДа (21q22.3). Совместно с тяжёлой цепью α формирует: LFA-1 - CD11a/ CD18, CR3 (Mac-1) - CD11b/CD18 и CR4 - CD11c/CD18. (+) - лейкоциты.
CD19
Мембранный антиген B-клеток (OMIM 107265; 16p11.2). Молекулярная масса 120 кДа. Принадлежит к суперсемейству иммуноглобулинов. Служит маркёром B-лимфоцитов, входит в состав корецепторного комплекса B-клеток и играет роль адапторной молекулы при внутриклеточной передаче сигнала с BCR; формирует нековалентный комплекс с CD21. (+) - пре-B- и B-клетки.
CD20
Поверхностный антиген B-лимфоцитов (OMIM 112210; 11q12q13.1) - трансмембранный фосфопротеин семейства тетраспанинов. Молекулярная масса 33-37 кДа. (+) - большинство B-клеток (появляется после экспрессии CD10 и CD19, но до экспрессии CD21/CD22 и поверхностных иммуноглобулинов), моноциты/макрофаги, активированные T- и B-лимфоциты, ДК лимфоидных фолликулов. (+) - (патология): 90% клеток B-лимфом, 40% клеток пре-B-лимфоцитарного острого лимфолейкоза, 80% клеток лимфомы Ходжкина.
• CD20L - подобный CD20 антиген (OMIM 606498; 11q12-q13.1) - трансмембранный белок гемопоэтических клеток. • CD20L2 - подобный CD20 антиген 2 (OMIM 606499; 11q12-q13.1) - трансмембранный белок, экспрессируемый в ткани яичек.
CD21
CR2. Рецептор 2 для компонента комплемента (связывает фрагменты молекул С3 системы комплемента - C3d, iC3b и C3dg, а также антиген gp350/220 вируса Эпштейна-Барр) (OMIM 120650; 1q32). Молекулярная масса 145 кДа. CD21 образует сигнальные комплексы с CD19, CD81, CD225; вместе с CD23 служит маркёром ДК. (+) - зрелые B- и ФДК, тимоциты, клетки эпителия, фетальные астроциты.
CD22
SIGLEC2, BL-CAM. Мембранный антиген B-клеток (OMIM 107266; 19q13.1). Молекулярная масса 140 кДа. Член суперсемейства иммуноглобулинов, сиалоадгезин, молекула адгезии B-клеток, рецептор хоминга B-лимфоцитов в костный мозг. Связываясь с лигандом CD75, обеспечивает взаимодействие между B-лимфоцитами. Нековалентно сцеплен с B-клеточным рецептором. Негативно регулирует силу сигнального пути, индуцируемого взаимодействием лиганд-BCR; служит ингибирующим рецептором B-лимфоцитов. Cвязывается с сиаловой кислотой и FcγRIIB1, взаимодействует с CD45R0 на T-клетках, с IgM и гаптоглобином в сыворотке. (+) - B-клетки. (+) - (патология): B-лимфоцитарный острый лимфолейкоз.
CD23
FCER2. Низкоаффинный рецептор для IgE, FceRII (OMIM 151445; 19p13.3). Молекулярная масса 45 кДа. Принадлежит к семейству Са2+зависимых лектинов типа С. Индуцирует секрецию клетками провоспалительных цитокинов: ИЛ-1 и ИЛ-6, ФНО, GM-CSF. Взаимодействуя с CD21, опосредует ряд биологически значимых процессов: пролиферацию миелоидных предшественников, межклеточную адгезию, регуляцию синтеза IgE, секрецию гистамина базофилами, рост B-клеток и их выживаемость в зародышевых центрах, созревание протимоцитов и др. (+) - зрелые B-клетки, экспрессирующие IgM или IgD; моноциты/ макрофаги, NK-клетки и некоторые T-лимфоциты, тромбоциты, эозинофилы, базофилы, клетки Лангерганса, ФДК. (+) - (патология): B-лимфоцитарный хронический лимфолейкоз.
CD24
Термостабильный гликопротеин муцинового типа HSA (Heat Stable Antigen) (6q21). Молекулярная масса 35-45 кДа. Принадлежит к семейству заякоренных белков GPI (CD24/HAS/CD52). Способствует дифференцировке и активации гранулоцитов и B-лимфоцитов, соединяясь с P-селектином (CD62P); участвует в процессах костимуляции и адгезии лейкоцитов. (+) - B-лимфоциты на всех стадиях развития до плазматических клеток, миелоидные клетки, зрелые гранулоциты, а также клетки эпителия почек. (+) - (патология): клетки карциномы, большинство пре-B-лимфоцитарных хронических лимфолейкозов, B-лимфомы.
CD25
Низкоаффинная a-цепь рецептора ИЛ-2 (OMIM 606367; 10p15-p14). Молекулярная масса 55 кДа. Вместе с β- (CD122) и γ-цепями (CD132) образует высокоаффинный рецептор для ИЛ-2. Маркёр регуляторных T-клеток, активации T-лимфоцитов; играет важную роль в опосредованном T-клетками иммунном ответе. В мономерной растворимой форме выявляют в сыворотке. (+) - активированные B- и T-клетки, моноциты/макрофаги. (+) - (патология): волосатоклеточный лейкоз.
CD26
DPP4. Дипептидилпептидаза IV (EC 3.4.14.5; OMIM 102720; 2q24.3) - антиген активации Т-клеток, кофактор CD4 (способствует входу ВИЧ в клетки). (+) - зрелые тимоциты, активированные T- и B-лимфоциты, NK-клетки, моноциты, макрофаги, эпителий канальцев почки, энтероциты, эндотелий синусоидов селезёнки.
CD27
S152. Антиген активации Т-клеток. TNFRSF7. (OMIM 186711;12p13). Молекулярная масса 110-120 кДа. Трансмембранный гликопротеин суперсемейства рецептора фактора некроза опухоли. Маркёр активации T-клеток. Взаимодействие с CD70 необходимо для пролиферации и дифференцировки B-лимфоцитов в плазматические клетки. (+) -T-клетки, B-клетки памяти.
CD28
Антиген T-клеток (OMIM 186760; 2q33). Молекулярная масса 90 кДа. Член суперсемейства иммуноглобулинов, ключевая костимулирующая молекула для активации и пролиферации T-клеток; рецептор для CD80 (B7-1) и CD86 (B7-2). (+) - CD4+ T-клетки (95%), CD8+ T-клетки (50%), активированные B-клетки, плазматические клетки.
CD29
VLAB, ITGB1, GPIIa. Рецептор для фибронектина, субъединица β1интегрина очень позднего активационного антигена VLA (Very Late Activation antigen) (OMIM 135630; 10р11.2). Молекулярная масса 130 кДа. (+) - фибробласты, тромбоциты, T-клетки.
CD30
TNFRSF8. Антиген (гликопротеин) активации лимфоцитов из суперсемейства рецептора ФНО (OMIM 153243; 1р36). Молекулярная масса 120 кДа. Лиганды: CD30L (CD153) и факторы, ассоциированные с рецептором ФНО - TRAF1, TRAF2, TRAF3, TRAF5 (от TNF Receptor-Associated Factors). (+) - (норма): гранулоциты, плазматические клетки, активированные B- и T-клетки, NK-клетки, моноциты. (+) - (патология): клетки, инфицированные ВИЧ, вирусами HTLV-1, Эпштейна-Барр, HHV8, гепатита B; клетки Рид-Штернберга, 90% анапластических крупноклеточных лимфом, периферические T-клеточные лимфомы, эмбриональные карциномы яичка.
CD31
PECAM-1. Одноцепочечная трансмембранная молекула межклеточной адгезии тромбоцитов и эндотелия типа 1 (OMIM 173445; 17q23). Молекулярная масса 130 кДа. Интегрин αvβ3, член суперсемейства иммуноглобулинов, маркёр эндотелия. (+) - (норма): эндотелий, тромбоциты, макрофаги и клетки Купфера, гранулоциты, NKT-клетки, мегакариоциты, фибробласты, остеокласты, нейтрофильные лейкоциты. (+) - (патология): эпителиоидная гемангиоэндотелиома, эпителиоидная саркомоподобная гемангиоэндотелиома, плазмоцитомы, некоторые карциномы и саркомы.
CD32
FCGR2A, IGFR2. Низкоаффинный рецептор FcγRIIB для IgG (OMIM 146790; 1q23). Молекулярная масса 40 кДа. Принадлежит суперсемейству иммуноглобулинов. (+) - моноциты, гранулоциты, эозинофилы, B-клетки, базофилы, тромбоциты.
CD33
SIGLEC3. Антиген (гликопротеин) миелоидной дифференцировки (OMIM 159590; 19q13.1). Молекулярная масса 150 кДа. Член семейства сиалоадгезинов. (+) - (норма): миелоидные предшественники, большинство моноцитов, эпидермальные клетки Лангерганса. (+) - (патология): острый миелолейкоз M1-M5 (75-85%), M7, хронический миелолейкоз (90%); бласты (все), некоторые острые лимфолейкозы.
• CD33L1. SIGLEC6. Антиген CD33-подобный, лектин 6, иммуноглобулиноподобный, связывающий сиаловую кислоту (OMIM 604405). • CD33L2. SIGLEC5. Антиген CD33-подобный, лектин 5, иммуноглобулиноподобный, связывающий сиаловую кислоту.
CD34
HPCA1. Поверхностный антиген предшественников гемопоэза (OMIM 142230; 1q32). Молекулярная масса 116 кДа. Обладает адгезивными свойствами. CD34 - сильно гликозилированный белок семейства сиаломуцинов; основной маркёр гемопоэтических стволовых клеток человека. (+) - (норма): предшественники гемопоэтических клеток, эндотелий (TdT+, HLADR+). (+) - (патология): альвеолярная саркома, пре-B-лимфоцитарный острый лимфолейкоз (75%), острый миелолейкоз (40%), острый миелолейкоз - M7 (большинство), хордоидные глиомы, дендритная фибромиксолипома, эпителиоидные саркомы, стромальные опухоли пищеварительного тракта, гигантоклеточная фибробластома, гранулоцитарная саркома, гамартомные опухоли при эпилепсии, гемангиоперицитомы (50%), воспалительные фиброзные полипы желудка, саркома Капоши, липосаркомы, злокачественные опухоли нервов, менингеальные гемангиоперицитомы, менингиомы, метанефрическая аденосаркома почки, сосочковая карцинома щитовидной железы, паратестикулярная лейомиосаркома (30%), шванномы, склерозирующая липосаркома, солитарные фиброзные опухоли, синовиальная саркома, бласты при миелопролиферативных заболеваниях.
CD35
CR1. Рецептор 1 для компонентов комплемента (C3b, C4b, iC3b) (OMIM 120620; 1q32). Молекулярная масса гетерогенна - 35-250 кДа. Связан с эритроцитарными групповыми антигенами Knops, McCoy, Swain-Langley, York. (+) - гранулоциты, макрофаги, B-клетки, T-клетки (10%), часть NK-клеток, эритроциты, ФДК, эозинофилы, подоциты, некоторые астроциты.
CD36
GPIV, GP4, GPIIIb - гликопротеин IV тромбоцитов, рецептор для тромбоспондина семейства рецепторов-«мусорщиков» (OMIM 173510; 7q11.2). Молекулярная масса 90 кДа. Локус фиксации инфицированных Plasmodium falciparum эритроцитов к эндотелию. (+) - (норма): тромбоциты, моноциты, макрофаги, эндотелий мелких сосудов, ранние эритроидные клетки, мегакариоциты. (+) - (патология): острый миелолейкоз M3-M7.
• CD36L1 (SCARB1, CLA1) - антиген CD36-подобный, рецептор типа скэвенджер (OMIM 601040). • CD36L2 (SCARB2) - антиген CD36-подобный, рецептор типа скэвенджер (OMIM 602257).
CD37
Поверхностный антиген лейкоцитов (OMIM 151523; 19p13-p13.4). Молекулярная масса 40-52 кДа. Принадлежит к семейству тетраспанинов (Tetraspanin-26). (+) - (норма): B-клетки, нейтрофильные лейкоциты, гранулоциты, моноциты. (+) - (патология): волосатоклеточный лейкоз, B-клеточные лимфомы.
CD38
Одноцепочечный трансмембранный гликопротеин семейства АДФрибозилциклаз (OMIM 107270; 4р15). Молекулярная масса 45 кДа. Участвует в адгезии между лимфоцитами и эндотелием. (+) - (норма): плазматические клетки, лимфоидные предшественники, NK-клетки, Bи T-клетки, моноциты, эритроидные и миелоидные предшественники, тимоциты, бласты, мозг, мышцы, почки, печень, яичники, поджелудочная железа, плацента, яички. (+) - (патология): лимфома, нейробластома.
CD39
ENTPD1. Эктонуклеозидтрифосфатдифосфогидролаза 1, апираза 1 (OMIM 601752; 10q24). Молекулярная масса 78 кДа. Участвует в межклеточной адгезии и в различных клеточных функциях - во взаимодействии ДК и T-лимфоцитов при презентации антигена, в модуляции воспалительного и иммунного ответа, служит ингибитором активации тромбоцитов. Экспрессируется на активированных B-лимфоцитах, NK-клетках, макрофагах, клетках Лангерганса, ДК. (+) - (норма): B- и T-лимфоциты, NK-клетки, эндотелий, плацента.
• CD39L1 (ENTPD2) - апираза 2 (OMIM 602012). • CD39L2 (ENTPD6) - апираза 6 (OMIM 603160). • CD39L3 (ENTPD3) - апираза 3. • CD39L4 (ENTPD5) - апираза 5 (OMIM 603162).
CD40
TNFRSF5. Трансмембранный одноцепочечный белок семейства рецептора фактора некроза опухоли (OMIM 109535; 20q12-q13.2). Молекулярная масса 85 кДа. Служит костимулирующей молекулой при активации АПК и B-лимфоцитов. Взаимодействие CD40 на АПК и CD154 на Th1-клетках играет ключевую роль в формировании клеточного иммунного ответа. (+) - (норма): B-клетки, макрофаги, ДК, эндотелий сосудов, эпителий почек, фибробласты, кератиноциты. (+) - (патология): карциномы, большинство B-клеточных лимфом, B-лимфоцитарные острые лимфолейкозы (некоторые).
CD41
GPIIb. Гликопротеин тромбоцитов IIb (α-цепь комплекса IIb/IIIa; 3q29). Связан с актином цитоскелета - рецептор для фибриногена, фактора фон Виллебранда и фибронектина. (+) - (норма): тромбоциты, мегакариоциты. (+) - (патология): острый миелолейкоз - M7, бласты.
CD42
GPIX. Комплекс CD42a-d.
• CD42a, гликопротеин GP Ib.IX молекулярной массой 23 кДа (3q21). Опосредует адгезию тромбоцитов. • CD42b, гликопротеин GP Ib молекулярной массой 160 кДа (17pterp12). Гетеродимер из цепей a (CD42b) и Р (CD42c) с дисульфидной связью. • CD42c, гликопротеин GP IBB молекулярной массой 22 кДа (22q11.21-q11.23). Формирует нековалентный комплекс с CD42a и CD42d. • CD42d, гликопротеин GP V молекулярной массой 85 кДа (3q29). Участвует в формировании высокоаффинного рецептора для тромбина. Рецептор фактора фон Виллебранда и тромбина. (+) - (норма): тромбоциты и мегакариоциты.
CD43
SPN, LSN, GPL115. Сиалогликопротеин (сиалофорин, лейкосиалин) (16р11.2; OMIM 182160). Молекулярная масса 95-135 кДа. Одноцепочечная трансмембранная молекула с антиадгезивными свойствами. (+) - (норма): большинство T-клеток, активированные B-клетки, NKклетки, гранулоциты, моноциты, мегакариоциты, мозг; (+) - (патология): 80% T-клеточных лимфом, гранулоцитарные саркомы, острый миелолейкоз, большинство острых лимфолейкозов, плазмоцитомы; болезнь тучных клеток (также «+» к триптазе, CD68, CD117).
CD44
HERMES, Pgp1, MDU3 (OMIM 107269; 16р11.2). Молекулярная масса 85-90 кДа. Трансмембранная многофункциональная молекула (гликопротеин) с адгезивными свойствами. (+) - (норма): T- и B-лимфоциты, моноциты, гранулоциты, ДК, эритроциты, фибробласты, клетки эпителия и эндотелия, молочная железа, толстая кишка, желудок, матка. (+) - (патология): 80% колоректальных карцином.
• CD44H - (CD44s) - главный рецептор гиалуроновой кислоты. • CD44R - (CD44v).
CD45
LCA, PTPRC. Общий антиген лейкоцитов (1q31-q32), принадлежит к семейству протеинтирозинфосфатазных рецепторов (OMIM 151460). Трансмембранная молекула с внеклеточным доменом и цитоплазматическим участком, состоящим из двух тандемных каталитических фосфатных доменов. Лиганды: CD2, CD3, CD4, CD22. (+) - (норма): гемопоэтические клетки и их предшественники; (-) - эритроциты, негемопоэтические клетки, лимфомы, множественная миелома, клетки Рид-Штернберга.
• CD45RO (молекулярная масса 180 кДа). (+) - (норма): T-клетки памяти, активированные T-клетки, некоторые B-клетки, гранулоциты (слабо), макрофаги (слабо), кортикальные тимоциты. (+) - (патология): 75% T-клеточных неходжкинских лимфом, T-клеточный острый лимфолейкоз, 25% острых миелолейкозов. • CD45RА (молекулярная масса 205-220 кДа) - клетки мозговой части тимуса. • CD45RB (молекулярная масса 190-220 кДа). • CD45RC.
CD46
Мембранный кофакторный белок MCP (Membrane Cofactor Protein) (1q32). Молекулярная масса 45-70 кДа. Связывает компоненты комплемента C3b и С4b, что делает их доступными для расщепления протеазой - фактором I. Рецептор для вируса кори (OMIM 120920), для патогенной Neisseria и для Streptococcus pyogenes группы А. (+) - (норма): все клетки крови, кроме эритроцитов; клетки эпителия, эндотелия, фибробласты.
CD47
IAP, MER6. Ассоциированный с интегрином белок (OMIM 601028; 3q13.1-q13.2). Молекулярная масса 45-60 кДа. Рецептор для тромбоспондина; физически и функционально связан с β3-цепью интегрина (CD61). Принадлежит к суперсемейству иммуноглобулинов, содержит IgV-подобный внеклеточный домен, 5 мембранных сегментов и гидрофобный цитоплазматический хвост. (+) - (норма): гемопоэтические клетки, эпителиальные клетки, эндотелий, фибробласты, клетки мезенхимы. (+) - (патология): линии злокачественных клеток.
• CD47R (новое обозначение антигена CDw149) - относят к антигенам Rh-фактора.
CD48
BLAST1, BCM1. Гликопротеин суперсемейства иммуноглобулинов. Молекулярная масса 40-47 кДа (1q21.3-q22). С низкой аффинностью связывается с CD2, с высокой - с CD244. Участвует в активации T-лимфоцитов; в качестве дополнительной молекулы участвует в процессе распознавания антигена γδT-лимфоцитами. (+) - (норма): большинство лейкоцитов, активированные лимфоциты.
CD49
α-Цепь интегринов αβ1(VLA - Very Late Activation antigen - очень поздний активационный антиген), формируемых объединением различных α- (CD49) и β1-цепей (CD29). Все антигены CD49 участвуют в процессах адгезии, взаимодействия клеток с межклеточным матриксом, трансдукции внутриклеточного сигнала.
• CD49а - α1-цепь (5р11) интегрина (VLA-1) - рецептор для ламинина-1 и коллагена. Молекулярная масса 200 кДа. (+) - (норма): активированные B- и T-клетки, моноциты. • CD49b - α2-цепь интегрина α2β1 (VLA-2) (OMIM 192975; 5q2331) - рецептор для ламинина-1 и коллагена. Молекулярная масса 160 кДа. Участвует в процессах свёртывания крови, ангиогенеза, гистогенеза, органогенеза. (+) - T- и В-лимфоциты, моноциты, макрофаги, гранулоциты, клетки эндотелия. • CD49с - α3-цепь (димер с молекулярной массой цепей 125 и 30 кДа) интегрина α3β1 (VLA-3) (OMIM 605025; 17q23.3) - рецептор для ламинина-5, коллагена, фибронектина, тромбоспондина. (+) - (норма): негемопоэтические клетки. • CD49d - α4-цепь интегрина α4β1 (VLA-4) - рецептор для фибронектина, молекул MAdCAM-1 (Mucosal Addressin Cell Adhesion Molecule-1) и VCAM-1 (Vascular Cell Adhesion Molecule) (2q31-q32). Молекулярная масса 145 кДа. (+) - (норма): моноциты, макрофаги, T- и B-клетки, тимоциты, эозинофилы, базофилы, тучные клетки, NK-клетки, ДК, миелоидные клетки, предшественники эритроцитов. (+) - (патология): клетки меланомы. • CD49e - α5-цепь (димер с молекулярной массой цепей 135 и 25 кДа) (12q11-q13) интегрина α5β1 (VLA-5) - рецептор для фибронектина, интегрина, инвазина. (+) - (норма): тромбоциты, моноциты, нейтрофильные лейкоциты, T-клетки памяти. • CD49f - α6-цепь (димер с молекулярной массой 125 и 25 кДа) (2q31.1) интегрина α6β1 (VLA-6) - рецептор для ламинина, инвазина, мерозина. (+) - (норма): T-лимфоциты, моноциты, тромбоциты, мегакариоциты, эпителиальные клетки.
CD51-100
[править]CD50
Мембранная молекула межклеточной адгезии ICAM-3 (Intercellular Adhesion Molecule 3), член суперсемейства иммуноглобулинов. Молекулярная масса 110-140 кДа (19р13.3-р13.2). Лиганд - LFA-1 (CD11a/ CD18). (+) - (норма): лейкоциты, эпидермальные клетки Лангерганса, эндотелий.
CD51
ITGAV; VNRA. Интегрин αV (2q31-q32). Молекулярная масса 125 кДа. Вместе с β3-цепью (CD61) образует адгезивный рецептор для витронектина, фибриногена, фактора фон Виллебранда, тромбоспондина. (+) - (норма): тромбоциты, эндотелий, мегакариоциты.
CD52
Короткий пептид (1р36), относящийся к семейству заякоренных белков GPI (CD24/HAS/CD52). (+) - (норма): тимоциты, моноциты/макрофаги, эозинофилы, эпителиальные клетки мужской половой системы. (+) - (патология): большинство лимфоидных злокачественных клеток.
CD53
Поверхностный антиген лейкоцитов (OMIM 151525; 1р13). Молекулярная масса 32-42 кДа. Относится к семейству тетраспанинов. (+) - (норма): лейкоциты. (-) - тромбоциты, эритроциты, негемопоэтические клетки.
CD54
ICAM-1 - Intercellular Adhesion Molecule-1. Молекула межклеточной адгезии 1 (OMIM 147840; 19р13.3-р13.2). Молекулярная масса 90 кДа. Трансмембранный антиген активированных клеток эндотелия, активированных T- и B-лимфоцитов; рецептор для риновирусов и инфицированных плазмодиями эритроцитов. Принадлежит к суперсемейству иммуноглобулинов. Лиганды: LFA-1 (CD11a/CD18), Mac-1 (CD11b/ CD18), CD43, CD227. (+) - (норма): B- и T-клетки, моноциты, эндотелий, эпителиальные клетки. (+) - (патология): острый лимфолейкоз, кератоакантома, плоскоклеточная карцинома.
CD55
DAF - Decay Acceleration Factor. Фактор, ускоряющий разрушение комплемента (1q32), антиген группы крови Cromer (OMIM 125240), рецептор для CD97, вирусов Коксаки B. Молекулярная масса 55-70 кДа. (+) - (норма): гемопоэтические клетки, эритроциты, внеклеточный матрикс.
CD56
NCAM-1 - Neural Cell Adhesion Molecule-1. Молекула межклеточной адгезии невральная (OMIM 116930; 11q23.1), трансмембранный гликопротеин суперсемейства иммуноглобулинов. (+) - (норма): NK-клетки (80-90%), активированные T-клетки, головной мозг, нейроэндокринные клетки. (+) - (патология): миелома, миелолейкоз, опухоль Вильмса, нейробластома, NKT-клеточные лимфомы, панкреокарцинома, феохромоцитома, мелкоклеточная карцинома лёгких.
CD57
LEU7, HNK-1. Антиген естественных киллеров (OMIM 151290), олигосахарид. (+) - (норма): 60% NK- и T-клеток, 15-20% мононуклеаров периферической крови, нейроэктодермальные производные, мозг, простата, канальцы почки. (+) - (патология): нейроэктодермальные,мелкоклеточная карцинома лёгких, аденокарцинома простаты, метанефрическая аденома, карциноиды почки, светлоклеточные опухоли почки, некоторые лимфомы.
CD58
LFA-3 (Lymphocyte Function-Associated antigen 3). Антиген 3, ассоциированный с функцией лимфоцитов (OMIM 153420; 1р13). Молекулярная масса 40-70 кДа. Принадлежит к суперсемейству иммуноглобулинов. Лиганд для CD2, экспрессируется многими типами клеток, опосредует адгезию между АПК и T-хелперами, тимоцитами и клетками эпителия тимуса, клетками-киллерами и клетками-мишенями. (+) - (норма): лейкоциты, эритроциты, эндотелий, эпителиальные клетки, фибробласты.
CD59
Протектин (OMIM 107271; 11р13). Молекулярная масса 18-25 кДа. Мембранный гликопротеин, препятствующий вызванному комплементом лизису собственных клеток. (+) - (норма): большинство клеток.
CD60
Антиген семейства гликолипидов.
• CD60a - GD3 - ганглиозид D3. • CD60b - 9-O-ацетил-GD3. • CD60c - 7-O-ацетил-GD3. (+) - (норма): тромбоциты, CD4+ и CD8+ T-клетки, эпителий тимуса, активированные кератиноциты, синовиальные фибробласты, гладкомышечные клетки, астроциты.
CD61
ITGB3, GP3A. β3-Субъединица интегрина, гликопротеин тромбоцитов IIIa, компонент рецептора для фибриногена (OMIM 173470). Участвует в трансдукции внутриклеточного сигнала. (+) - (норма): тромбоциты, мегакариоциты, миелоидные предшественники, эндотелий. (+) - (патология): острые миелолейкозы - M7, острые миелолейкозы - M6 (некоторые), бласты.
CD62
Селектины - молекулы межклеточной адгезии (OMIM 153240). Принадлежат к семейству лектинов типа С.
• CD62P (селектин P, PADGEM) (1q22-q25). Молекулярная масса 120 кДа. (+) - (норма): тромбоциты, мегакариоциты, эпителий, эндотелий. • CD62L (селектин L, LAM-1, LECAM-1) (1q23-q25). Молекулярная масса 65-95 кДа. (+) - (норма): NK-клетки, наивные B-, T-клетки; тимоциты, мононуклеары костного мозга, моноциты, нейтрофильные лейкоциты, эозинофилы. • CD62E (селектин E, ELAM-1) (OMIM 131210; 1q22-q25). Молекулярная масса 115 кДа. (+) - (норма): эндотелий (после стимуляции цитокинами).
CD63
ME491, LAMP-3, NKI-C3. Антиген меланомы - гранулофизин (OMIM 155740; 12q12-q13). Молекулярная масса 53 кДа. Член суперсемейства тетраспанинов, маркёр активации базофилов, вместе с CD82 защищает молекулы MHC-II от протеолитических ферментов. (+) - (норма): B-лимфоциты, активированные T-клетки, макрофаги, нейтрофилы, ДК, базофилы, активированные тромбоциты, фибробласты, остеокласты, эндотелий, гладкие мышцы, нервная ткань, синовиальная выстилка. (+) - (патология): меланома.
CD64
FCGR1B. Высокоаффинный рецептор FcγRI для IgG (OMIM 601502; 1q211). Молекулярная масса 72 кДа. Опосредует фагоцитоз, сорбцию антигенов и иммунных комплексов, антителозависимую клеточную цитотоксичность, высвобождение цитокинов и активных форм кислорода. (+) - (норма): макрофаги/моноциты, ДК, ранние миелоидные клетки, активированные гранулоциты. (+) - (патология): острые миелолейко-
зы M0-M2; M3 (обычно), M4, M5.
CD65
VIM2. Церамид-додекасахарид - молекула адгезии. (+) - (норма): миелоидные клетки, моноциты.
• CD65S - сиалилированный CD65. (+) - (норма): гранулоциты, моноциты. (+) - (патология): клетки миелолейкоза.
CD66
Разные гликопротеины (OMIM 109770), относящиеся к раковоэмбриональным антигенам.
• CD66а (CEACAM1, BGP, C-CAM) - предшественник раковоэмбрионального антигена, рецептор для Neisseria gonorrhoeae и N. meningitidis. (+) - (норма): гранулоциты, эпителиальные клетки, простата, жёлчные капилляры. (+) - (патология): карцинома простаты. • CD66b (ранее назывался CD67) (CEACAM8) - родственная раковоэмбриональному антигену молекула адгезии 8. (+) - (норма): гранулоциты. (+) - (патология): хронический миелолейкоз. • CD66c (NCA). (+) - (норма): гранулоциты. • CD66d - (+) - (норма): гранулоциты. • CD66e (CEA) - раково-эмбриональный антиген. (+) - (норма): жёлчные протоки, толстая кишка плода, эпителиальные клетки, аденокарциномы пищеварительного тракта, гранулоциты, муцин бокаловидных клеток. (+) - (патология): аденокарцинома лёгких и органов пищеварения, карцинома щитовидной железы. • CD66f - (+) - (норма): синцитиотрофобласт, печень плода.
CD67
Переименован в CD66b.
Антиген макрофагов - макросиалин (OMIM 153634; 17р13). Молекулярная масса 110 кДа. (+) - (норма): макрофаги/моноциты, базофилы, ДК, тучные клетки, миелоидные клетки, нейтрофильные лейкоциты, остеокласты, активированные тромбоциты, B- и T-клетки. (+) - (патология): острые миелолейкозы M4/M5, ангиосаркома, B-клеточная лимфома, гигантоклеточная ангиобластома, волосатоклеточный лейкоз, гистиоцитарная саркома, гистиоцитоз клеток Лангерганса, мастоцитоз, меланомы (некоторые).
CD69
Маркёр активации клеток гемопоэтической линии развития, наиболее ранний активационный антиген T-лимфоцитов (OMIM 107273). Гомодимер (молекулярная масса 23 кДа) с дисульфидной связью (12р13). (+) - (норма): активированные T-клетки, B-клетки, NK-клетки, нейтрофильные лейкоциты, эозинофилы, эпидермальные клетки Лангерганса. (+) - (патология): T-клеточные лимфомы.
CD70
CD27L, TNFSF7. Принадлежит к суперсемейству лигандов ФНО (OMIM 602840), лиганд для CD27 (19р13). Молекулярная масса 75- 170 кДа. (+) - (норма): активированные B- и T-клетки, макрофаги. (+) - (патология): клетки Рид-Штернберга.
CD71
TFRC, TFR, TRFR. Рецептор для трансферрина (OMIM 190010).
Трансмембранный гликопротеин, состоящий из двух идентичных мономеров (молекулярной массой 90-95 кДа каждый), соединённых дисульфидной связью. (+) - (норма): все пролиферирующие клетки, нуждающиеся в железе: эритроидные предшественники костного мозга, ретикулоциты, эндотелий мозга. (+) - (патология): острые миелолейкозы M6.
CD72
Общий B-клеточный маркёр (9р13.1). Экспрессируется начиная с про-B-клеток. Молекулярная масса 45 кДа. Характеризуют как ингибиторный рецептор B-лимфоцитов. (+) - (норма): B-клетки. (+) - (патология): волосатоклеточный лейкоз.
CD73
NT5E, E5NT, ENT, NTE. Экто-5'-нуклеотидаза (6q14-q21). Молекулярная масса 69-72 кДа. (+) - (норма): субпопуляции T-клеток (CD3 - 25%, CD4 - 10%, CD8 - 50%) и B-клеток (75%), эндотелий, ФДК, эпителиальные клетки. (+) - (патология): хронический лимфолейкоз, острый лимфолейкоз.
HLADG. Трансмембранная инвариантная цепь Ii, выполняющая роль шаперона при внутриклеточном транспорте молекул HLA класса II в АПК (5q32). Имеет изоформы с молекулярной массой 33 кДа, 35 кДа и 41 кДа. Участвует во внутриклеточной укладке и сборке образующихся a- и Р-цепей HLA-DR. Является рецептором для цитокина MIF (Macrophage migration Inhibitory Factor - фактор подавления миграции макрофагов). (+) - (норма): B-клетки, активированные T-клетки, макрофаги, активированные эндотелиальные и эпителиальные клетки.
Лактозамин, член семейства сиалогликанов, лиганд для CD22. (+) - (норма): B-клетки, некоторые эпителиальные клетки, эритроциты. (+) - (патология): «popcorn»-клетки при болезни Ходжкина. • CD75s - α2,6-сиалированный лактозамин (ранее назывался CDw75 или CDw76). Лиганд для CD22. (+) - (норма): зрелые В-клетки, в особенности клетки зародышевых центров, небольшая часть T-лимфоцитов.
CDw76
Переименован в CD75s.
Глоботриасиалцерамид (антиген группы крови Pk) - связывается с токсином Shigella dysenteriae, веротоксином 1 E. coli, CD19. (+) - (норма): B-клетки. (+) - (патология): лимфома Беркитта.
CD78
Также известный как CDw78, Ba-антиген, Leu21 или LO-panB-a. Присутствует на некоторых незрелых и на некоторых зрелых В-клетках. Его экспрессия значительно усиливается после активации В-клеток in vitro. Он также обнаружен на тканевых макрофагах и на эпителиальных клетках, но не на Т-лимфоцитах, NK-клетках, моноцитах и гранулоцитах. Антиген CDw78 экспрессируется как часть одной из молекул, кодируемых генами МНС класса II, и является сходной (если не идентичной) с α/β-гетеродимерным антигеном МНС-II.
CD79
• CD79a - инвариантный компонент Igα BCR (OMIM 112205; 19q13.2). Молекулярная масса 40-45 кДа. Участвует в трансдукции внутриклеточного сигнала. (+) - (норма): B-клетки. (+) - (патология): B-клеточные лимфомы, лимфома Ходжкина. • CD79b - инвариантный компонент Igβ BCR (OMIM 147245; 17q23). Молекулярная масса 37 кДа. Участвует в трансдукции внутриклеточного сигнала.
CD80
B7.1, B71, BB1. Трансмембранный гликопротеин суперсемейства иммуноглобулинов (OMIM 112203; 3q13.3-q21). Молекулярная масса 60 кДа. Лиганд для CD28 и для CD152 (CTLA-4) T-клеток, необходимый для их активации (через CD28) и торможения активации (через CD152). Участвует в T-B-взаимодействии и в «диалоге» T-лимфоцитов с АПК. (+) - (норма): активированные B-клетки, T-клетки, макрофаги, ДК.
CD81
TAPA-1 (Targetof AntiProliferative Antibody). Мишень для антипролиферативных антител - интегральный мембранный белок (OMIM 186845; 11p15.5) суперсемейства тетраспанинов. Молекулярная масса 26 кДа. Экспрессируется разными клетками (в том числе лимфоцитами, тимоцитами, частью макрофагов, гранулоцитами). Участвует в процессах роста, развития, подвижности, во взаимодействии и активации клеток. Связывается, в частности, с белками оболочки вируса гепатита C. CD81 входит в состав комплекса с CD19, физически и функциональ-
но связан с отдельными интегринами, взаимодействует с молекулами HLA класса II.
CD81P3
См. CD316.
CD82
Антиген суперсемейства тетраспанинов с четырьмя трансмембранными доменами, разделёнными двумя внеклеточными петлями, и двумя короткими цитоплазматическими сегментами (11р11.2). Молекулярная масса 45-90 кДа. Участвует в активации T-клеток - пролиферация, выработка цитокинов и др. (OMIM 600623). Образует кластеры с CD63, защищающие молекулы HLA класса II от действия протеаз. (+) - (норма): активированные/дифференцированные гемопоэтические клетки. (-) - эритроциты.
CD83
Трансмембранный белок суперсемейства иммуноглобулинов c цитоплазматическим сегментом и одним внеклеточным доменом (6р23). Молекулярная масса 43 кДа. Основной маркёр зрелых ДК (OMIM 604534). Экспрессируется также на активированных B-лимфоцитах, клетках Лангерганса. CD83 связывается с моноцитами и служит рецептором адгезии клеток семейства SIGLEC (OMIM 600751). (+) - (норма): ДК, клетки Лангерганса, лимфоциты. (+) - (патология): воспалительный инфильтрат миокарда при синдроме Чёрджа-Стросс.
CD84
Молекула адгезии (OMIM 604513) суперсемейства иммуноглобулинов (1q24). Молекулярная масса 68-80 кДа. (+) - (норма): B-клетки, тимоциты, некоторые T-клетки, моноциты/макрофаги, тромбоциты.
CD85
Семейство иммуноглобулиноподобных рецепторов ILT/LIR/MIR (Immunoglobulin-Like Transcript/Leukocyte Immunoglobulin-like Receptor/ Macrophage Immunoglobulin-like Receptor). Принадлежит к суперсемейству иммуноглобулинов, кодируется генами лейкоцитарного кластера LRC (Leukocyte Receptor Cluster), (19q13.4). Включает рецепторы как активирующего (ILT1/LIR7, LIR6, ILT7, ILT8), так и ингибирующего типов (ILT2/LIR1/MIR7, ILT3/LIR5, ILT4/LIR2/MIR10, ILT5/LIR3, LIR8). (+) - (норма): миелоидные клетки, B-лимфоциты, NK-клетки, часть T-лимфоцитов. (+) - (патология): клетки волосатоклеточного лейкоза.
• CD85a (ILT5, LIR3) (OMIM 604820). • CD85b (ILT8). • CD85c (LIR8) (OMIM 604814). • CD85d (ILT4, LIR2, MIR10) (OMIM 604815). • CD85e (ILT6, LIR4) (OMIM 604818). • CD85f (ILT11) (OMIM 606047). • CD85g (ILT7). • CD85h (ILT1, LIR7) (OMIM 604812). • CD85i (LIR6) (OMIM 604810). • CD85j (ILT2, LIR1, MIR7) (OMIM 604811). • CD85k (ILT3, LIR5) (OMIM 604821). • CD851 (ILT9). • CD85m (ILT10).
CD86
B7.2. Одноцепочечный гликопротеин суперсемейства иммуноглобулинов (3q21). Молекулярная масса 80 кДа. Содержит внеклеточный и трансмембранный домены и цитоплазматический участок. Связывается с CTLA-4 на T-лимфоцитах. Взаимодействуя с лигандом CD28, формирует одну из двух пар костимулирующих молекул, необходимых для активации T-хелперов и стимуляции АПК. (+) - (норма): ДК в T-зонах, клетки Лангерганса, B-клетки памяти, моноциты, эндотелий, активированные T-клетки.
CD87
PLAUR, uPAR. Рецептор активатора плазминогена урокиназный (OMIM 173391; 19q13). Молекулярная масса 35-39 кДа. (+) - (норма): T-клетки, NK-клетки, моноциты, нейтрофильные лейкоциты, эндотелий, фибробласты, гладкие мышцы, кератиноциты, плацента, гепатоциты. (+) - (патология): карциномы молочной железы, толстой кишки и простаты, меланома.
CD88
Рецептор для компонента комплемента, анафилатоксина и хемоаттрактанта C5a; гликопротеин семейства G-связывающих белков (19q13.3-q13.4). Молекулярная масса 43 кДа. Связывается с CD222; участвует в индукции синтеза белков острой фазы. (+) - (норма): гранулоциты, нейтрофилы, макрофаги/моноциты, ДК, тучные клетки, гепатоциты, астроциты, микроглия.
FcaRI. Рецептор типа I для Fc-фрагмента IgA (OMIM 147045), гликопротеин суперсемейства иммуноглобулинов (19q13.2-q13.4). Включает 2 внеклеточных домена, трансмембранный домен и цитоплазматический участок. Молекулярная масса 45-100 кДа. (+) - (норма): гранулоциты, моноциты, активированные эозинофилы, альвеолярные макрофаги.
CD90
Thy-1. Маркёр ранних гемопоэтических клеток-предшественников, гликопротеин суперсемейства иммуноглобулинов (11q22.3-q23). Молекулярная масса 25-35 кДа. (+) - (норма): гемопоэтические стволовые клетки, нейроны, соединительная ткань.
CD91
Рецептор для α2-микроглобулина (12q13-q14). Димер с молекулярной массой цепей 515 кДа и 85 кДа. Относится к семейству рецепторов липопротеинов низкой плотности. (+) - (норма): фибробласты, ДК, макрофаги; печень, мозг, лёгкие.
CD92
Переносчик холина (9q31.2). Возможно, участвует в мембранном синтезе SLC44A1 - холин-транспортирующегоподобного белка 1. Молекулярная масса 70 кДа. (+) - (норма): лейкоциты, эндотелий.
CD93
C1QR1. Компонент комплемента 1q, субкомпонент рецептора 1. Рецептор (или элемент большего рецепторного комплекса) для C1q, MBL (MBL2) и белка легочного сурфактанта А (SPA). Может быть медиатором усиления фагоцитоза в моноцитах и макрофагах за счёт взаимодействия с растворимыми защитными коллагенами. Может участвовать в межклеточной адгезии. (+) - (норма): гранулоциты, моноциты, тромбоциты, нейтрофилы, клетки эндотелия. (+) - (патология): бласты при остром миелолейкозе.
CD94
Член подсемейства лектиноподобных рецепторов типа D для молекул MHC-I. Содержат внеклеточный участок с лектиновым доменом типа С (12р13). Молекулярная масса 43 кДа. На поверхности NK-клеток и части T-лимфоцитов экспрессируется в виде гетеродимера, ковалентно связанного с рецептором семейства NKG2 (CD94/NKG2). Способен как активировать прохождение внутриклеточного сигнала (CD94/NKG2C, CD94/NKG2E, CD94/NKG2H), так и подавлять его (CD94/NKG2A, CD94/NKG2В). Активирующие и ингибирующие свойства рецептора определяются структурным строением их трансмембранных и цитоплазматических доменов - связью с ITAM-содержащим адапторным белком DAP12 (активирующие рецепторы) или наличием двух доменов ITIM (ингибирующие рецепторы). (+) - (норма): NK-клетки, некоторые T-клетки.
CD95
Fas/APO-1, TNFRSF6. Мембранный рецептор для Fas-лиганда (CD95L или CD178). Относится к суперсемейству рецепторов фактора некроза опухоли (OMIM 134637; 10q24.1). Молекулярная масса 160 кДа. CD95 характеризуют как рецептор смерти - DR (Death Receptor), содержащий в цитоплазматической части домен смерти DD (Death Domain) - центральный физиологический регулятор апоптоза. (+) - (норма): лимфоидная ткань, печень, лёгкие, молочная железа, эпителий влагалища, матки, яичников. (+) - (патология): эпителий щитовидной железы при тиреоидите Хасимото, клетки Рид-Штернберга, пищевод Баррета, аденокарцинома пищевода.
CD96
TACTILE (T cell Activation, Increased Late Expression). Антиген повышенной поздней экспрессии на активированных T-клетках (3q13.13). Принадлежит к суперсемейству иммуноглобулинов. Молекулярная масса 160 кДа. (+) - (норма): активированные T-клетки, NK-лимфоциты.
CD97
(OMIM 601211; 19р13.2-р13.12). Гликопротеин семейства G-связывающих белков. Молекулярная масса (в зависимости от изоформы) 28-89 кДа. Связывается с лигандом CD55 (фактор DAF, ускоряющий разрушение комплемента). (+) - (норма): активированные T- и B-клетки, моноциты/макрофаги, ДК, гранулоциты. (+) - (патология): клетки карцином щитовидной железы и органов пищеварения.
CD98
SLC3A2. Активатор транспорта двухосновных и нейтральных аминокислот (11q13). Гетеродимер с соединёнными дисульфидной связью цепями: тяжёлой гликозилированной (80 кДа) и лёгкой негликозилированной (45 кДа). Связывается с актином. (+) - (норма): многие клетки. (+) - (патология): трансформированные опухолевые клетки.
MIC2, MIC2X, O13 (OMIM 313470; Xp22.32-Yp11.3). Гликопротеин клеточной поверхности. Молекулярная масса 32 кДа. Участвует в процессах адгезии T-лимфоцитов. (+) - (норма): тимоциты, лимфоциты периферической крови, клетки гранулёзы яичника, островки Лангерганса, клетки Сертоли. (+) - (патология): T-клеточный острый лимфолейкоз, саркома Юинга/недифференцированная нейроэктодермальная опухоль (95%), многие карциномы и стромальные опухоли.
CD100
SEMA4D, SEMAJ, COLL4. Гомодимер с молекулярной массой 300 кДа (9q22-q31). Относится к семейству семафоринов и к суперсемейству иммуноглобулинов. Содержит несколько доменов, в том числе трансмембранный и цитоплазматический - семафорин 4D (коллапсин 4; OMIM 601866). (+) - (норма): гемопоэтические клетки.
CD101-150
[править]CD101
IGSF2. Гликопротеин суперсемейства иммуноглобулинов (OMIM 604516; 1р13). Молекулярная масса 240 кДа. Участвует в активации T-клеток. (+) - (норма): моноциты, гранулоциты, ДК, активированные T-лимфоциты.
CD102
ICAM-2 (Intercellular Adhesion Molecule 2). Молекула межклеточной адгезии 2 (17q23-q25). Молекулярная масса 55-65 кДа. Трансмембранный гликопротеин суперсемейства иммуноглобулинов. Связывает LFA-1 (CD11a/CD18), участвует в процессах рециркуляции лимфоцитов, активации NK-клеток, в адгезивных взаимодействиях при иммунном ответе; проявляет костимулирующую активность для T-клеток. (+) - (норма): моноциты, тромбоциты, часть покоящихся лимфоцитов, эндотелий сосудов. (+) - (патология): некоторые лимфомы.
CD103
ITGAE. α-Субъединица интегрина Е (интегрин αE) (OMIM 604682; 17р13). Маркёр внутриэпителиальных лимфоцитов. Лиганды: интегрин β7, Е-кадгерин. (+) - (норма): внутриэпителиальные лимфоциты, некоторые T-лимфоциты слизистой оболочки кишечника. (+) - (патология): волосатоклеточный лейкоз; острый миелолейкоз, а также T-клеточные лимфомы, связанные с энтеропатиями.
β4-Субъединица интегрина (интегрин β4). (+) - (норма): тимоциты, эпителий, эндотелий, нейроны.
CD105
ENG. Эндоглин (OMIM 131195). Гомодимерный гликопротеин молекулярной массой 180 кДа (9q33-q34.1). Служит регуляторной частью рецептора для ТФРР. Лиганды: ТФРР1, ТФРР3. (+) - (норма): активированные моноциты, макрофаги, эндотелий, эритроидные предшественники; синцитиотрофобласт, цитотрофобласт.
CD106
VCAM-1 (Vascular Cell Adhesion Molecule 1). Молекула адгезии сосудистых клеток, сиалогликопротеин, член суперсемейства иммуноглобулинов (1p32-p31). Молекулярная масса 100-110 кДа. Опосредует адгезию между лейкоцитами и клетками эндотелия. Лиганд: VLA-4 (CD49d).
CD107
Ассоциированные с мембраной лизосом гликопротеины. Молекулярная масса 110-120 кДа. (+) - (норма): тромбоциты, активированные T-клетки, нейтрофильные лейкоциты, эндотелий.
• CD107a (LAMP-1 - Lysosome-Associated Membrane Protein 1)(13q34). • CD107b (LAMP-2) (Xq24).
CD108
SEMA7A. Ранее назывался CDw108. Семафорин, мембранный гликопротеин (15q22.3-q23). Молекулярная масса 76 кДа. Антиген группы крови John-Milton-Hagen (JMH). (+) - (норма): эритроциты, лимфобласты, лимфоциты.
CD109
ФАТ, гликопротеин с молекулярной массой 175 кДа. Экспрессируется на тромбоцитах, активированных T-лимфоцитах, клетках эндотелия.
CD110
TPO-R, MPL. Рецептор для тромбопоэтина (1р34). Член суперсемейства иммуноглобулинов. Молекулярная масса 85-92 кДа. Опосредует образование и стимуляцию функций мегакариоцитов, дифференцировку тромбоцитов, защищает стволовые клетки от апоптоза. (+) - (норма): СКК, мегакариоциты, тромбоциты.
PRR1. Белок адгезии нектин 1 (11q23-q24). Имеет 3 изоформы - нектин 1α (50 кДа, мембраносвязанный), 15 (57 кДа, мембраносвязанный) и нектин 1 γ (39 кДа, секретируемый). Служит рецептором для вирусов простого герпеса 1 и 2. (+) - (норма): клетки миелоидной, моноцитарной, эритроидной и мегакариоцитарной линий; эпителиальные клетки, нейроны, эндотелий.
CD112
PRR2. Молекула адгезии (19q13.2-q13.4). Имеет 2 изоформы - CD112a (64 кДа) и CD1125 (75 кДа). Служит рецептором для псевдорабического вируса и для отдельных мутантов вируса герпеса. (+) - (норма): клетки миелоидной, моноцитарной, эритроидной и мегакариоцитарной линий, эпителиальные клетки, нейроны, эндотелий.
CD113
PRR3. Нектин 3. Молекула адгезии эпителиальных клеток. Принадлежит к суперсемейству иммуноглобулинов.
CD114
G-CSFR. Рецептор для G-CSF (1р35-р34.3). Принадлежит к суперсемейству иммуноглобулинов. Молекулярная масса 130 кДа. Специфический регулятор процессов пролиферации и дифференцировки клеток миелоидного ряда. (+) - (норма): гранулоциты, моноциты, тромбоциты, эндотелий, плацента, клетки трофобласта. (+) - (патология): культивируемые опухолевые клетки.
CD115
c-fms. Рецептор для M-CSF (5q33.2-q33.3). Принадлежит к суперсемейству иммуноглобулинов. Молекулярная масса 150 кДа. Опосредует действие M-CSF на клетки мононуклеарных фагоцитов (рост, активацию, выживаемость). CD115 характеризуют как рецепторную тирозинкиназу. (+) - (норма): макрофаги, остеокласты, трофобласт, молочная железа, микроглия, нейроны, астроциты. (+) - (патология): 10% острых миелолейкозов, некоторые карциномы эндометрия, яичника и молочной железы, а также клетки хориокарциномы.
CD116
GM-CSFR. α-Субъединица рецептора GM-CSF (Xp22.32, Yp11.3). Молекулярная масса 80 кДа. Взаимодействует с общей β-субъединицей (CD131) рецепторов для GM-CSF, ИЛ-3 и ИЛ-5. (+) - (норма): макрофаги, нейтрофилы, эозинофилы, фибробласты, эндотелий, ДК.
с-kit. Рецептор фактора стволовых клеток (SCF - Stem Cell Factor) (4q11-q12). Принадлежит к суперсемейству иммуноглобулинов. Молекулярная масса 145 кДа. Участвует в регуляции гемопоэза. Лиганды: SCF, фактор роста тучных клеток. (+) - (норма): гемопоэтические стволовые клетки, меланоциты, мозг эмбриона и плода, эндотелий, тучные клетки, гонады, молочная железа, интерстициальные клетки Кахаля, гоноциты. (+) - (патология): острые миелолейкозы, ангиосаркомы (50%), светлоклеточная саркома, хронический миелолейкоз, эпителиоидная саркома, саркома Юинга, гранулоцитарная саркома, лимфомы, семиномы, герминомы.
CD118
LIFR - Leukemia Inhibitory Factor Receptor a. Гликопротеин типа I. Растворимый CD118 обнаружен в сыворотке, его уровень возрастает во время беременности. (+) - (норма): гемопоэтические стволовые клетки, эпителиальные клетки, моноциты, фибробласты, печень, плацента.
CD119
IFNGR1 - Interferon Gamma Receptor 1. a-Цепь рецептора для ИФНу (6q23-q24). Высокоаффинный рецептор к ИНФу. Гетеродимер, состоящий из двух цепей, - α (54 кДа; собственно CD119 или IFNGR1; связывает лиганд - ИНФу) и β (38 кДа; (21q22.11); IFNGR2; передаёт сигнал в клетку). (+) - (норма): моноциты/макрофаги, B-клетки. NK-клетки, эндотелий.
CD120
TNF-R - Tumor Necrosis Factor Receptor. Рецептор для ФНО. Относится к семейству рецепторов смерти DR (Death Receptor). Опосредует провоспалительный ответ. Экспрессируется на гемопоэтических и негемопоэтических клетках.
• CD120a (p55/60, TNF-RI) - рецептор типа I для ФНОα и ФНОβ (12р13.2). Молекулярная масса 55 кДа. Участвует в запуске апоптоза. Цитоплазматический участок рецептора содержит домен смерти DD (Death Domain). • CD120b (p75/80, TNF-RII) - рецептор типа II для ФНОα и ФНОβ (1p36.3-p36.2). Молекулярная масса 75 кДа. Сигналы, индуцирующие апоптоз, непосредственно не запускает. Цитоплазматический участок лишён домена смерти DD.
Рецептор ИЛ-1. Принадлежит к суперсемейству иммуноглобулинов.
• CD121a - рецептор типа I (2q12). Связывает все формы ИЛ-1, способен к передаче активирующего внутриклеточного сигнала. Молекулярная масса 80 кДа. (+) - (норма): T-клетки, тимоциты, фибробласты, эндотелий, гепатоциты, кератиноциты, астроциты. • CDw121b - рецептор типа II (2q12-q22). Является ловушкой для ИЛ-1, блокирует эффекты, связанные с его повышенной выработкой. Молекулярная масса 68 кДа. (+) - (норма): B-клетки, моноциты/макрофаги, нейтрофилы, клетки костного мозга.
CD122
IL2RB. Р-Цепь рецепторов для ИЛ-2 и для ИЛ-15 (OMIM 146710; 22q13.1). Молекулярная масса 75 кДа. Вместе с у-цепью (CD132) формирует рецептор для ИЛ-2, а вместе с IL15RA входит в состав рецептора для ИЛ-15. (+) - (норма): B- и T-лимфоциты, NK, моноциты, макрофаги.
CD123
IL3RA. Низкоаффинная α-цепь рецептора для ИЛ-3 (OMIM 308385). Вместе с β-цепью (CD131) формирует высокоаффинный рецептор. Служит маркёром плазмоцитоидных ДК (фенотипа CD123+ CD11c+).
CD124
Общая α-субъединица рецептора ИЛ-4 и ИЛ-13 (16р11.2-12.1). Гликопротеин. Принадлежит к суперсемейству иммуноглобулинов. Молекулярная масса 140 кДа. Вместе с у-цепью (CD132) формирует рецептор для ИЛ-4, а вместе с цепью α1 (CD213a1) - рецептор для ИЛ-13. (+) - (норма): гемопоэтические и негемопоэтические клетки (фибробласты, нейробласты, клетки стромы, эндотелий, эпителий, мышечные клетки, кератиноциты, гепатоциты).
CD125
Низкоаффинный рецептор ИЛ-5, α-цепь высокоаффинного рецептора ИЛ-5 [формирует его вместе с β-цепью (CD131)] (3р26-р24). Белок суперсемейства иммуноглобулинов. Молекулярная масса 55-60 кДа. (+) - (норма): эозинофилы, активированные B-клетки, базофилы.
CD126
IL6RA. α-Цепь рецептора ИЛ-6 (OMIM 147880; 1q21). Вместе с β-цепью (CD130) формирует рецептор, α-цепь которого связывает интерлейкин, а β-цепь обеспечивает передачу активирующего сигнала
внутрь клетки. Одноцепочечный гликопротеин суперсемейства иммуноглобулинов с внеклеточным, трансмембранным и внутриклеточным сегментами. Молекулярная масса 80 кДа. (+) - норма: плазматические клетки, T-лимфоциты и активированные B-клетки, моноциты, гепатоциты.
CD127
α-Цепь рецептора ИЛ-7 (5p13). Вместе с γ-цепью (CD132) формирует высокоаффинный рецептор для ИЛ-7. Гликопротеин суперсемейства иммуноглобулинов. Молекулярная масса 65-90 кДа. (+) - (норма): предшественники B-клеток, большинство T-клеток, моноциты.
CDw128a
Переименован в CD181.
CDw128b
Переименован в CD182.
CD129
Трансмембранный белок типа I. Индуцирует рост клеток и/или их дифференцировку. (+) - (норма): некоторые Т-клетки, миелоидные и эритроидные предшественники, а также тучные клетки. (+) - (патология): болезнь Ходжкина, большеклеточные лимфомы и мегакариобластические лейкозы.
CD130
gp130 (5q11). Общая β-субъединица, входящая в качестве трансдуктора сигналов в состав ряда рецепторов цитокинов - ИЛ-6 и ИЛ-11, лейкозингибирующего фактора (LIF), онкостатина М (OSM), цилиарного нейротропного фактора, кардиотропина-1. CD130 непосредственно связывается только с OSM, а с другими лигандами - в составе комплекса, например, с ИЛ-6 взаимодействует комплекс CD126/CD130. CD130 принадлежит к суперсемейству иммуноглобулинов. Одноцепочечная трансмембранная молекула. Молекулярная масса 130-140 кДа. (+) - (норма): практически все типы клеток.
CD131
Ранее известен как CDw131. Общая Р-субъединица рецепторов ИЛ-3, ИЛ-5 и GM-CSF (22q13.1). Трансмембранный гликопротеин суперсемейства иммуноглобулинов. Молекулярная масса 120-140 кДа. (+) - (норма): миелоидные клетки, ранние B-клетки.
IL2RG. Общая у-цепь рецепторов интерлейкинов (ИЛ-2, ИЛ-4, ИЛ-7, ИЛ-9, ИЛ-15 и ИЛ-21). Принадлежит к суперсемейству иммуноглобулинов. Молекулярная масса 64 кДа (Xq13.1). (+) - (норма): Tи B-лимфоциты, NK-клетки, моноциты/макрофаги, нейтрофильные лейкоциты, тучные клетки.
CD133
Гликопротеин. Относится к пентаспанинам семейства промининов (4р16.2-р12). Молекулярная масса 120 кДа. Маркёр родоначальных и гемопоэтических стволовых клеток. (+) - (норма): ранние родоначальные клетки, включая CD34+ гемопоэтические клетки-предшественники, нейральные и эндотелиальные стволовые клетки. (+) - (патология): ретинобластома, гемангиобласты.
CD134
TNFRSF4, OX40. Белок суперсемейства рецепторов для фактора некроза опухоли (OMIM 600315; 1q36). Молекулярная масса 50 кДа. Стимулирует адгезивные взаимодействия клеток, экспрессируется на активированных T-лимфоцитах. • CD134L (TNFSF4, OX40L, OMIM 603594) - лиганд для ОХ40. Bзаимодействие Т- и В-лимфоцитов, опосредованное CD134 и CD134L, сопровождается активацией выработки IgG.
CD135
Flt3. Рецептор фактора роста ранних родоначальных гемопоэтических клеток (13q12). Принадлежит к суперсемейству иммуноглобулинов. Молекулярная масса 130 кДа. (+) - (норма): полипотентные СКК. (+) - (патология): большинство острых миелолейкозов, острых лимфолейкозов и хронических миелолейкозов.
CD136
Рецептор белка, стимулирующего макрофаги (MSP - Macrophage Stimulating Protein) (3р21.3). Относится к семейству протеинкиназ. Гетеродимер с дисульфидными связями, состоящий из внеклеточной a-цепи (40 кДа) и Р-цепи (150 кДа) с внеклеточным и трансмембранным сегментами и внутриклеточным тирозинкиназным доменом. (+) - (норма): эпителий кожи, почек, лёгкого, печени, кишечника; моноциты, отдельные гемопоэтические и нейроэндокринные клетки.
TNFRSF9, ILA. Член суперсемейства рецепторов фактора некроза опухоли (OMIM 602250; 1р36). Гликопротеин с внеклеточным, трансмембранным и внутриклеточным фрагментами. Проявляет свойства костимулирующей молекулы или молекулы, передающей внутриклеточный активирующий сигнал. (+) - (норма): NK-клетки, внутриэпителиальные лимфоциты, эозинофилы, тимоциты, активированные T-лимфоциты (CD4+ и CD8+) - особенно CD45RA и CD45RО; B-клетки, моноциты, эпителиальные клетки.
CD138
Syndecan-1. Синдекан 1 (OMIM 186355; 2р24.1). Мембранный протеогликан, функционирующий как рецептор для внеклеточного матрикса. (+) - (норма): маркёр B-лимфоцитов, дифференцирующихся на стадии после миграции из зародышевых центров; высокоспецифичный маркёр плазматических клеток, представлен на поверхности эндотелиальных и многих других типов клеток. (+) - (патология) - отдельные B-клеточные лимфомы.
CD139
Молекулярная масса 209-228 кДа. (+) - (норма): B-лимфоциты, моноциты, гранулоциты, ФДК.
CD140
Рецептор для фактора роста, продуцируемый тромбоцитами (PDGFR - Platelet Derived Growth Factor Receptor). • CD140a (PDGFRα). • CD140b (PDGFRβ). (+) - (норма): фибробласты, клетки гладких мышц, клетки глии и хондроциты.
CD141
Тромбомодулин - кофактор, активирующий белок С и участвующий в развитии противосвёртывающего каскада. Относится к семейству лектинов типа С. Одноцепочечный гликопротеин с внеклеточным, трансмембранным и внутриклеточным регионами. Молекулярная масса 75 кДа. (+) - (норма): эндотелий, мегакариоциты, кератиноциты, мезотелий, моноциты, нейтрофильные лейкоциты, тромбоциты, гладкие мышцы, синцитиотрофобласт, синовиальная оболочка, уротелий. (+) - (патология): мезотелиома (эпителиоидная), плоскоклеточные карциномы, опухоли трофобласта, уротелиальная карцинома, сосудистые опухоли, синовиальная саркома. (-) - (патология): аденокарцинома толстой кишки, эндометрия, почки, простаты.
CD142
Главный тканевой фактор коагуляции (фактор III), или тромбопластин - одноцепочечный белок с внеклеточным, трансмембранным и внутриклеточным фрагментами (1р22-р21). Молекулярная масса 45- 47 кДа. Связывает фактор VIIa свёртывания крови. В соотношении 1:1 комплекс CD142/VIIa активирует факторы свёртывания крови (VII, IX и X) и запускает этот каскад. (+) - (норма): эпидермальные кератиноциты, различные эпителии, адвентициальные клетки кровеносных сосудов, астроциты, миокард, шванновские клетки, клетки стромы печени, поджелудочной железы, селезёнки.
CD143
Ангиотензинпревращающий фермент - заякоренный в клеточной мембране член семейства пептидаз М2 (17q23). Молекулярная масса 110-180 кДа. Вовлекает в метаболизм вазоактивные пептиды брадикинин и ангиотензин II, участвует в связывании сперматозоидов с яйцеклеткой. (+) - (норма): эндотелий артериол, эндотелий капилляров лёгкого, щёточная каёмка проксимальных извитых канальцев, клетки гранулёзы, клетки Лейдига.
CD144
Кадгерин-5. Участвует в межклеточных контактах эндотелия. (+) - (норма): эндотелий, мозг.
CDw145
Экспрессируется на эндотелиальных клетках; другая информация в настоящее время отсутствует.
CD146
Молекула адгезии клеток меланомы (11q23.3). Член суперсемейства иммуноглобулинов. Молекулярная масса 118 кДа. Участвует в процессах роста и расселения опухолевых клеток. (+) - (норма): гладкие мышцы, эндотелий, трофобласт, часть активированных T-клеток, шванновские клетки. (+) - (патология): светлоклеточная саркома (90%), лейомиосаркома, меланома, нейрофиброма (40%), аденокарцинома простаты.
CD147
Нейротелин (19p13.3). Одноцепочечная молекула адгезии суперсемейства иммуноглобулинов с внеклеточным, трансмембранным и цитоплазматическим участками. Молекулярная масса 50-60 кДа. (+) - (норма): лейкоциты, эритроциты, тромбоциты, эндотелий.
CD148
Одноцепочечный трансмембранный рецептор с протеинтирозинфосфатазным доменом в цитоплазматической части (11p.11.2). Молекулярная масса 240-260 кДа. (+) - (норма): гранулоциты, моноциты, T-клетки памяти, ДК, тромбоциты, фибробласты, нейроны, клетки Купфера.
CDw149
Переименован в CD47R.
CD150
Костимулирующий рецептор - одноцепочечная трансмембранная молекула суперсемейства иммуноглобулинов (1q22-q23). Молекулярная масса 65-95 кДа. (+) - (норма): тимоциты, T-клетки фенотипа CD45RO, B-клетки, ДК, эндотелий.
CD151-200
[править]CD151
Трансмембранная молекула семейства тетраспанинов (PETA3, SFA1) (OMIM 602243; 11р15.5). Молекулярная масса 32 кДа. (+) - (норма): эндотелий, тромбоциты, мегакариоциты, эпителий.
CD152
CTLA-4 (Cytotoxic T Lymphocyte-Associated antigen 4). Гликопротеин цитотоксических T-лимфоцитов 4 (OMIM 123890; 2q33). Гомодимер с дисульфидными связями. Принадлежит к суперсемейству иммуноглобулинов. Характеризуют как ингибиторный рецептор T-клеток, лиганд для В7-1 (CD80) и В7-2 (CD86). Молекулярная масса 33 кДа. (+) - (норма): активированные T-клетки, некоторые активированные B-клетки.
CD153
CD30L, TNFSF8, CD30LG. Член суперсемейства фактора некроза опухоли (OMIM 603875; 9q33) - лиганд для CD30. Трансмембранная молекула молекулярной массой 38-40 кДа. Экспрессируется на макрофагах, нейтрофильных лейкоцитах, активированных T- и B-лимфоцитах. CD154
CD40L, gp39. Член суперсемейства фактора некроза опухоли (OMIM 300386; Xq26) - лиганд для CD40. Трансмембранная молекула молекулярной массой 32-39 кДа. Взаимодействие CD154+ T-лимфоцитов с CD40+ АПК - важнейший этап развития гу-
морального и клеточного иммунного ответа. CD154 необходим для формирования B-клеток памяти. (+) - (норма): преимущественно активированные зрелые CD4+ T-клетки, небольшая часть активированных CD8+ T-лимфоцитов.
CD155
PVR. Рецептор для вируса полиомиелита (OMIM 173850; 9q13.2). Молекулярная масса 80-90 кДа. Участвует в процессах межклеточной адгезии. (+) - (норма): тимоциты, моноциты, макрофаги, нейроны.
CD156a
ADAM4 (OMIM 602267; 10q26.3). Относится к семейству металлопротеаз-дезинтегринов. Молекулярная масса 69 кДа. (+) - (норма): нейтрофильные лейкоциты, моноциты.
CD156b
TACE (Tumor necrosis factor Alpha Converting Enzyme). Фермент, конвертирующий ФНОα, - многодоменный трансмембранный белок семейства металлопротеаз-дезинтегринов (2p25). Молекулярная масса 100-120 кДа. (+) - (норма): все клетки.
CD157 АДФ-рибозилциклаза и гидролаза для АДФ-рибозы - одноцепочечная молекула, заякоренная в G-белке (OMIM 600387; 4р15). Молекулярная масса 42-50 кДа. (+) - (норма): гранулоциты, моноциты, макрофаги, предшественники B-клеток, часть T-клеток, ФДК, линии стромальных клеток костного мозга.
CD158
KIR (Killer Immunoglobulin-like Receptors). Иммуноглобулиноподобные рецепторы NK-клеток. Контролируются генами кластера LRC (Leukocyte Receptor Cluster) хромосомы 19 (19q13.4). Гликопротеины клеточной поверхности, несущие 2 или 3 внеклеточных домена (KIR2D или KIR3D соответственно). KIR характеризуют как активирующие или ингибирующие рецепторы. Активирующие имеют короткий (индекс «S» в наименовании - от англ. Short; KIR2DS или KIR3DS), а ингибирующие - длинный цитоплазматический сегмент (индекс «L» в наименовании - от англ. Long; KIR2DL или KIR3DL). Следующая цифра означает номер рецептора. Рецепторы типа «S» взаимодействуют положительно заряженным коротким цитоплазматическим сегментом с отрицательно заряженным адапторным белком DAP12, несущим домены ITAM и участвующим в активации клетки. Рецепторы типа «L» в цитоплазматическом сегменте содержат домены ITIM c функцией подавления клеточной активности. Лиганды: MHC-I. (+) - (норма): NK-клетки, некоторые T-клетки. • CD158a (KIR2DL1, OMIM 604936). • CD158b1 (KIR2DL2, OMIM 604937). • CD158b2 (KIR2DL3, OMIM 604938). • CD158c (KIR2DS6/KIRX). • CD158d (KIR2DL4, OMIM 604945). • CD158e1 (KIR3DL1, OMIM 604946). • CD158e2 (KIR3DS1, OMIM 604957). • CD158f (KIR2DL5, OMIM 605305). • CD158g (KIR2DS5, OMIM 604956). • CD158h (KIR2DS1, OMIM 604952). • CD158i (KIR2DS4, OMIM 604955). • CD158j (KIR2DS2, OMIM 604953). • CD158k (KIR3DL2, OMIM 604947). • CD158z (KIR3DL7/KIRC1).
CD159a
NKG2A. Подобный лектину типа С (12p13). Принадлежит семейству рецепторов NKG2, преимущественно экспрессируемых NK-клетками. В результате ковалентного связывания с CD94 формирует ингибиторный рецептор NK-клеток - CD94/NKG2A. (+) - (норма): NK-клетки.
CD160
Гликопротеиновый мультимер с дисульфидными связями (1q42.3). Член суперсемейства иммуноглобулинов. Молекулярная масса 80 кДа. (+) - (норма): NK-клетки периферической крови, CD8+ T-клетки, внутриэпителиальные лимфоциты кишечника.
CD161
Рецептор Р1А NK-клеток - NKR-P1A (12р13). Трансмембранный гликопротеин, член семейства лектинов типа С. Молекулярная масса 80 кДа. Участвует в регуляции функций NK-клеток. (+) - (норма): NKклетки, некоторые CD4+ и CD8+ T-клетки, преимущественно клетки памяти.
CD162
PSGL-1 (P-Selectin Glycoprotein Ligand), SELPLG (Selectin P Ligand) (OMIM 600738; 12q24). Лиганд селектина Р (CD62P). Молекулярная масса 220-250 кДа. Образует связанный дисульфидной связью гомодимер, играет ключевую роль в адгезивных взаимодействиях, опосредует перекатывание лейкоцитов по активированным, содержащим Р-селектин эндотелиальным клеткам. (+) - (норма): большинство T-клеток, некоторые B-лимфоциты, гранулоциты, моноциты.
• CD162R (PSGL-1) (12q24) - посттрансляционный вариант PSGL-1. Молекулярная масса 240 кДа. (+) - (норма): естественные киллеры.
CD163
Рецептор для гаптоглобина (OMIM 605545; 12р13.3). Принадлежит к семейству обогащённых цистеином рецепторов-«мусорщиков» SRCR. Молекулярная масса 130 кДа. (+) - (норма): моноциты/макрофаги.
CD164
Сиаломуцин; гликопротеин, подобный муцину (OMIM 603356; 6q21). Молекулярная масса 80 кДа. Участвует в процессах адгезии клеток фенотипа CD34+, а также в пролиферации гемопоэтических клеток. (+) - (норма): эпителий, моноциты, клетки стромы костного мозга. (+) - (патология): колоректальная карцинома, аденокарцинома поджелудочной железы.
CD165
Мембранный гликопротеин. Молекулярная масса 37 кДа. Участвует в процессах адгезии тимоцитов к эпителиальным клеткам тимуса. (+) - (норма): часть периферических лимфоцитов (высокий уровень экспрессии), большинство тимоцитов, клетки эпителия тимуса, моноциты, тромбоциты, нейроны центральной нервной системы (низкий уровень экспрессии). (+) - (патология): многие T-клеточные острые лимфолейкозы.
CD166
ALCAM. Молекула адгезии, связывающаяся с CD6 (3q13.1). Принадлежит к суперсемейству иммуноглобулинов, Молекулярная масса 100-105 кДа. (+) - (норма): нейроны, активированные T-клетки, активированные макрофаги, эпителий тимуса, фибробласты.
CD167a
DDR1 - рецептор с дискоидиновым доменом типа 1 (6р21.3). Принадлежит к подсемейству тирозинкиназных рецепторов. Димер с молекулярной массой 63-64 кДа. Активируется коллагеном. (+) - (норма): эпителиальные клетки (молочная железа, почка, лёгкое, пищеварительный тракт, мозг, островки Лангерганса). (+) - (патология): карциномы.
RHAMM (Receptor for Hyaluronan-Mediated Motility) - поверхностный, лишённый трансмембранного домена, рецептор для клеток с опосредованной гиалуронаном подвижностью (5q33.2). Молекулярная масса 52-125 кДа. (+) - (норма): эпителий бронхов, нейроны центральной нервной системы. (+) - (патология): некоторые изоформы являются онкогенами и экспрессируются клетками рака груди.
CD169
SIGLEC1 (Sialic acid binding Ig-like Lectin 1). Сиалоадгезин (OMIM 600751; 20p13). Молекулярная масса 180 кДа. Трансмембранный иммуноглобулиноподобный лектин 1, связывающий сиаловую кислоту. (+) - макрофаги (кроме клеток микроглии), в том числе при ревматоидном артрите, атеросклерозе.
CD170
SIGLEC5 (Sialic acid binding Ig-like Lectin 5) (19q13.3). Иммуноглобулиноподобный лектин 5, связывающий сиаловую кислоту. Гомодимер с молекулярной массой 67 кДа, участвует в процессах межклеточных взаимодействий. (+): нейтрофилы.
CD171
Трансмембранная молекула адгезии клеток L1 (Xq28). Принадлежит к суперсемейству иммуноглобулинов. Молекулярная масса 180-200 кДа. Связывает CD171 (гомофильная адгезия), CD9, CD24, CD56, CD51/ CD61, CD29/CD49e, ламинин и др. (+) - (норма): постмитотические нейроны, глиоциты, некоторые эпителиальные клетки, CD4+ (но не CD8+) T-лимфоциты, моноциты, ДК, некоторые B-лимфоциты.
CD172a
SIRPa (Signal-Regulatory Protein a). Сигнальный регуляторный белок a (20p30). Трансмембранный гликопротеин суперсемейства иммуноглобулинов; субстрат для связанных с рецептором активированных тирозинкиназ. Участвует в процессах межклеточной адгезии и в ответе клеток на факторы роста. Лиганд для CD47. (+) - моноциты, некоторые T-клетки.
CD173
Антиген группы крови H2 - маркёр ранних гемопоэтических клеток. (+) - (норма): CD34+ гемопоэтические предшественники. (-) - зрелые лимфоциты.
Антиген группы крови Y Льюис (Lewis - LeY; 19q13.3). Дифукозилированный олигосахарид типа 2 - маркёр раннего гемопоэза. (+) - (норма): гемопоэтические предшественники фенотипа CD34+. (-) - зрелые лимфоциты.
CD175
Tn. Антиген ранних этапов синтеза муцина.
• CD175s (STN).
(+) - (патология): карциномы.
CD176
Томсена-Фридренрайха онкофетальный групповой антиген. Выявляют при колоректальной карциноме и колитах.
CD177
NB1, HNA2A. Антиген нейтрофилов специфический 1 (OMIM 162860). (+) - (норма): миелоидные клетки.
CD178
FasL. Fas-лиганд (CD95L) для рецептора CD95 (Fas/APO-1) (OMIM 134638; 1q23). Принадлежит к суперсемейству фактора некроза опухоли. Молекулярная масса 38-42 кДа. Взаимодействие CD178 (CD95L) c CD95 приводит к развитию апоптоза. (+) - (норма): активированные хелперные и цитотоксические T-клетки, NK-клетки, нейтрофилы, зрелые эритробласты, клетки Сертоли, нейроны, эпителиальные клетки щитовидной железы, яички, передняя камера глаза, плацента. (+) - (патология): клетки Рид-Штернберга.
CD179
• CD179a (VpreBI) - полипептид суперсемейства иммуноглобулинов (22q11.22). Молекулярная масса 16-18 кДа. В результате нековалентного связывания с CD179b формирует суррогатную лёгкую цепь преB-клеточного рецептора. (+) - (норма): про-B- и пре-B-клетки.
• CD179b (λ-5) - полипептид суперсемейства иммуноглобулинов (22q11.23). Молекулярная масса 22 кДа. (+) - (норма): про-B- и пре-B-клетки.
CD180
RP105 - трансмембранный белок с коротким цитоплазматическим регионом (5q12). Молекулярная масса 95-105 кДа. Внеклеточный регион белка формирует с молекулой MD-1 рецепторный комплекс RP105/
MD-1, относящийся к семейству Toll-подобных рецепторов (TLR - Toll-Like Receptors). (+) - (норма): B-клетки мантии и краевой зоны, B-клетки зародышевых центров (слабо), моноциты, ДК.
CD181
Ранее был известен как CDw128a. α-Цепь рецептора для ИЛ-8; рецептор типа 1 для хемокинов СХС (CXCR1 - Chemokine C-X-C receptor 1) (2q35). Связанный с G-белком гликопротеин, относящийся к семейству родопсинов. Молекулярная масса 58-67 кДа. (+) - (норма): нейтрофильные лейкоциты, моноциты, NK-клетки, некоторые T-лимфоциты, ДК, базофилы, кератиноциты.
CD182
Ранее был известен как CDw128b. β-Цепь рецептора ИЛ-8, рецептор типа 2 для хемокинов СХС (CXCR2) (2q35). Связанный с G-белком гликопротеин, относящийся к семейству родопсиноподобных рецепторов. (+) - (норма): нейтрофильные лейкоциты, моноциты, ДК, NK-клетки, зрелые гранулоциты, проекционные нейроны, нейроэндокринные клетки. (+) - (патология): карциноиды, аденомы гипофиза, феохромоцитомы, медуллярные карциномы.
CD183
GRP9. Трансмембранный рецептор CXCR3 для хемокинов семейства CXC (OMIM 600894). Молекулярная масса 40,6 кДа. Связывается с индуцированными интерфероном хемокинами СХCL9 (монокин MIG), CXCL10 (IP-10), CXCL11 (T-клеточный α-хемоаттрактант I-TAC). Обеспечивает хемотаксическую миграцию клеток. (+) - (норма): активированные T-эффекторы, клетки памяти (CD4+, CD8+), T-клетки при воспалении, эозинофилы, плазмоцитоидные ДК. (-) - наивные T-клетки.
CD184
Рецептор CXCR4 для хемокинов семейства CXC (2q21). Молекулярная масса 46-52 кДа. Опосредует хемотаксис клеток в ответ на связывание хемокина CXCL12 (SDF1α и SDF1β - Stromal cell-Derived Factor 1). Корецептор для ВИЧ. (+) - (норма): все зрелые клетки крови, эндотелиальные и эпителиальные клетки, астроциты, нейроны.
CD185
Рецептор CXCR5 для хемоаттрактанта В-лимфоцитов BLC (B Lymphocyte Chemoattractant) (11q23.3). Молекулярная масса 45 кДа. Экспрессирован на зрелых В-клетках и клетках лимфомы Беркитта.
Рецептор CXCR6 для хемокина CXCL16 (3p21). Молекулярная масса 40 кДа. Корецептор для ВИЧ. Экспрессирован на активированных Т-лимфоцитах.
CD191
MIP-1αR, RANTES-R. Рецептор CCR1 для хемокинов семейства CC (3p21). Молекулярная масса 39 кДа. Экспрессирован на Т-лимфоцитах, моноцитах, некоторых стволовых клетках.
CD192
MCP-1-R. Рецептор CCR2 для хемокинов семейства CC - MCP-1, MCP-3 и MCP-4 (3p21). Молекулярная масса 40 кДа. Корецептор с CD4 для ВИЧ. Экспрессирован на активированных NK-клетках и мононуклеарных фагоцитах, на некоторых Т-клетках, В-лимфоцитах, эндотелиальных клетках.
CD193
Рецептор CCR3 для хемокинов семейства CC - эотаксина, MCP-1, MCP-3, MCP-4, RANTES, MIP-1δ (3p21.3). Молекулярная масса 45 кДа. Корецептор с CD4 для ВИЧ. Экспрессирован на эозинофилах, моноцитах, некоторых Т-лимфоцитах.
CD194
Рецептор CCR4 для хемокинов семейства CC - эотаксина, MCP-1, CCL17/TARC, RANTES, MIP-1 (3p22.3). Молекулярная масса 41 кДа. Экспрессирован на тромбоцитах, моноцитах, некоторых Т-лимфоцитах.
CD195
Трансмембранный рецептор CCR5 для хемокинов семейства СС (3р21). Молекулярная масса 40 кДа. Участвует в процессах хемотаксиса T-лимфоцитов (чаще Th1), моноцитов, ДК, связывая хемокины CCL3 (MIP-1α - Macrophage Inflammatory Protein 1α - макрофагальный воспалительный белок 1α), CCL4 (MIP-1β - Macrophage Inflammatory Protein 1β- макрофагальный воспалительный белок 1β), CCL5 (RANTES - Regulated on Activation, Normal T cell Expressed and Secreted chemokine - хемокин, экспрессируемый и секретируемый нормальными T-клетками и регулируемый процессами активации).
CD196
Рецептор CCR6 для хемокинов семейства СС. Связывается с MIP3a/LARC и последовательно проводит сигнал, повышая внутриклеточный уровень ионов кальция. (+) - (норма): селезёнка, лимфатические узлы, аппендикс, фетальная печень. Экспрессируется на лимфоцитах, Т- и В-клетках, но не на NK-клетках, моноцитах и гранулоцитах.
CD197
Рецептор CCR7 для хемокинов семейства СС (17q12-q21.2). Молекулярная масса 46-52 кДа. Связывает хемокины CCL19 (MIP3β- Macrophage Inflammatory Protein 3β - макрофагальный воспалительный белок 3β) и CCL21 (SLC - Secondary Lymphoid tissue Chemokine - хемокин вторичной лимфоидной ткани). (+) - (норма): активированные B-клетки, T-лимфоциты, NK-клетки, ДК. (+) - (патология): ген CD197 индуцируется вирусом Эпштейна-Барр, рецептор опосредует действие вируса на B-клетки.
CDw198
Рецептор CCR8 для хемокинов семейства СС (3p22). Молекулярная масса 50 кДа. Корецептор c СD4 для ВИЧ. Экспрессирован на Т-лимфоцитах (особенно Th2), моноцитах, NK-клетках.
CDw199
Рецептор CCR9 для хемокинов семейства СС (3p21.3). Молекулярная масса 43 кДа. Связывает TECK. Корецептор c СD4 для ВИЧ. Экспрессирован на Т-лимфоцитах памяти, мононуклеарных клетках lamina propria.
CD200
OX-2, MOX2, OX2. Мембранный гликопротеин (OMIM 155970; 3q12q13). Член суперсемейства иммуноглобулинов. (+) - (норма): ФДК, тимоциты, B-клетки, T-клетки, нейроны, почка, эндотелий.
• CD200R (OX2R) - рецептор для CD200 (OMIM 607546).
CD201-250
[править]CD201
EPCR (Endothelial protein C receptor). Рецептор для белка С эндотелия (20q11.2). Содержит домены α1 и α2 молекул MHC-I. Относится к семейству CD1/MHC-I - MHC-подобных гликопротеинов класса I, включающих CD1.
CD202b
Tie2, Tek. Рецептор для ангиопоэтиновых лигандов, связанный с тирозинкиназами (9р21). Молекулярная масса 145 кДа. Участвует в образовании и функционировании эндотелия сосудов. (+) - (норма): эндотелий, ранние гемопоэтические клетки.
CD203c
E-NPP3/PDNP3. Трансмембранный белок (6q22). Молекулярная масса 270 кДа. Принадлежит к семейству эктонуклеотидпирофосфатаз/ фосфодиэстераз. Участвует в процессах расщепления внеклеточных нуклеотидов, катализирует распад фосфодиэфирных и фосфосульфатных связей в дезоксинуклеотидах, никотинамиддинуклеотидах и нуклеотидных сахарах. (+) - (норма): простата, матка, базофилы, тучные клетки, миелоидные клетки. (+) - (патология): глиомы.
CD204
MSR1 (Macrophage Scavenger Receptor 1). Макрофагальный рецептор«мусорщик» 1 (8р22). Молекулярная масса 220 кДа. Обеспечивает связывание, поглощение и фрагментацию многих отрицательно заряженных макромолекул. (+) - (норма): миелоидные клетки.
CD205
DEC-205. Лимфоцитарный антиген 75 (LY75 - Lymphocyte antigen 75) (2q24). Рецептор ДК для связывания и поглощения антигена. (+) - (норма): ДК.
CD206
MMR. Рецептор макрофагов для маннозы - мембранный гликопротеин семейства лектинов типа С (10р13). Молекулярная масса 162 кДа. Связывает структуры, содержащие маннозу, на поверхности бактерий, вирусов, грибов. (+) - (норма): макрофаги, ДК.
CD207
LANGERIN (Langerhans cell specific C-type lectin). Специфический лектин типа С клеток Лангерганса (2р13). Молекулярная масса 40 кДа. (+) - (норма): клетки Лангерганса.
CD208
DC-LAMP (Dendritic Cell-specific Lysosomal-Associated Membrane Protein). Связанный с лизосомами мембранный белок, специфичный для
ДК (3q26.3-q27). (+) - (норма): ДК.
CD209
DC-SIGN (Dendritic Cell-Specific ICAM3-Grabbing Nonintegrin). Специфичный для ДК неинтегрин, связывающий ICAM3 (OMIM 604672). (+) - (норма): ДК.
• CD209L (LSIGN, DCSIGNR) - лиганд для CD209 (OMIM 605872).
CDw210
Рецептор для ИЛ-10.
• CD210a - субъединица α рецептора (IL10Rα, IL10R1) (1q23). • CDw210b - субъединица β рецептора (IL10Rβ, IL10R2) (21q22.11). Обе субъединицы относятся к семейству рецепторов для интерферона. Их совместная экспрессия обеспечивает трансдукцию сигнала, индуцируемого взаимодействием лиганд-рецептор. (+) - (норма): моноциты, B-клетки, T-клетки, естественные киллеры, селезёнка, тимус, плацента, лёгкое, печень.
CD212
Субъединица β1 рецептора ИЛ-12. Трансмембранный белок типа I. Принадлежит к суперсемейству рецепторов для цитокинов (гемопоэтинов). (+) - (норма): T-клетки, NK-клетки.
CD213
Рецептор ИЛ-13 (цепи α1 и α2).
• CD213a1. Цепь α1 рецептора ИЛ-13 (Xq24). Трансмембранный белок с молекулярной массой 65 кДа. Принадлежит к суперсемейству иммуноглобулинов. (+) - (норма): экспрессируется повсеместно, включая эндотелий, T- и B-клетки. • CD213a2. Цепь α2 рецептора ИЛ-13 (Xq13.1-q28). Растворимая форма цепи подавляет связывание ИЛ-13 с рецептором. (+) - (норма): плацента.
CD217
Рецептор ИЛ-17 (22q11.1). Мембранный гликопротеин. Участвует в активации T-лимфоцитов и в индукции выработки ИЛ-2.
CD218
Рецептор ИЛ-18 (цепи α и β). Принадлежит к семейству рецепторов к ИЛ-1.
• CD218a IL18Rα (цепь α рецептора ИЛ-18) (2q12). Трансмембранный белок с молекулярной массой 70 кДа. Непосредственно связывает ИЛ-17. • CD218b IL18Rβ (цепь β рецептора ИЛ-18) (2p24.3-2p24.1). Трансмембранный белок с молекулярной массой 70 кДа. Образует гетеродимер с α-цепью, усиливая связывание рецептора с ИЛ-17.
Экспрессия: T-клетки, NK-клетки, ДК.
CD219
L10RA, это рецептор IL 10. тормозит синтез провоспалительных цитокинов. Cпособствует выживанию миелоидных клеток-предшественников через рецептора инсулина субстрат-2/PI-3-киназы/AKT пути. Активация CD219 приводит к фосфорилирования тирозина JAK1 и TYK2 киназы.
INSR (Insulin Receptor). Рецептор для инсулина (19p13.3-p13.2). Трансмембранный гликопротеин. Состоит из двух α- и двух β-цепей. После аутофосфорилирования проявляет собственную тирозинкиназную активность. Экспрессия: гепатоциты, скелетная мышца, адипоциты, клетки плаценты, активированные T- и B-лимфоциты, моноциты, эритроциты.
IGF1R (Insulin-like Growth Factor 1 Receptor). Рецептор для инсулиноподобного фактора роста 1 (15q25-q26). Проявляет тирозинкиназную активность и обладает антиапоптогенными свойствами. Состоит из двух цепей - α (135 кДа) и β (90 кДа). Экспрессируется на многих клетках и на большинстве опухолей.
CD222
IGF2R (Insulin-like Growth Factor 2 Receptor). Рецептор для инсулиноподобного фактора роста 2 (6q26). Молекулярная масса 250 кДа. Полифункциональный трансмембранный лектин. Имеет короткий цитоплазматический фрагмент с участком, проявляющим способность перемещать лиганды внутрь клетки. Характеризуется как рецептор лизосомных гидролаз. Экспрессируется на многих клетках.
CD223
LAG3 (Lymphocyte Activation Gene 3) - ген активации лимфоцитов 3 (OMIM 153337; 12q13.3). Экспрессируется только на активированных T- и NK-клетках. Активирует моноциты и ДК, взаимодействуя с их молекулами главного комплекса гистосовместимости класса II.
CD224
γ-Глутамилтрансфераза (22q11.1-q11.2) - трансмембранный эктофермент, состоящий из двух нековалентно связанных полипептидных цепей - тяжёлой (62-68 кДа) и лёгкой (22 кДа). (+) - (норма): часть Tи B-лимфоцитов, эпителий сосудов, поджелудочная железа, почечные канальцы, семенники.
CD225
Leu13. Трансмембранный белок адгезии. Индуцируемый интерфероном трансмембранный рецептор, участвующий в контроле клеточного цикла. Способен передавать сигнал внутрь клетки. (+) - (норма): лейкоциты, эндотелий.
DNAM-1, PTA1. Гликопротеин с адгезивными свойствами (18q22.3). Молекулярная масса 65 кДа. Принадлежит к суперсемейству иммуноглобулинов. (+) - (норма): NK-клетки, тромбоциты, моноциты, некоторые B- и T-клетки.
CD227
MUC.1. Эписиалин. Трансмембранный муциновый гликопротеин c большим внеклеточным фрагментом и тандемными повторами из 20 аминокислот. Цитоплазматический фрагмент лишён киназной активности, но участвует в передаче сигнала. Лиганды: CD54, CD169, селектины и др. (+) - (норма): железистые эпителиальные клетки, гемопоэтические клетки (включая активированные), T- и некоторые B-лимфоциты, моноциты, клетки периневрия, ФДК. (+) - (патология): аденокарциномы, анапластические лимфомы, эпителиоидная саркома, менингиома, мезотелиома, миелома, плазмоцитома. (-) - карцинома печени и надпочечника.
CD228
Меланотрансферрин (3q28-q29). Поверхностный гликопротеин клеток меланомы. Существует в двух изоформах. Принадлежит к семейству трансферринов. Экспрессирован также на стволовых клетках.
CD229
Ly-9. Поверхностный антиген T- и В-лимфоцитов (OMIM 600684; 1q21.3-q22). Член суперсемейства иммуноглобулинов.
CD230
Прионовый белок. Экспрессируется на многих клетках.
CD231
TALLA-1. Антиген T-клеточного острого лимфолейкоза (Xq11.4). Мембранный гликопротеин семейства тетраспанинов. Молекулярная масса 150 кДа. (+) - (норма): нейроны. (+) - (патология): T-клеточный острый лимфолейкоз, нейробластома. (-) - В-клетки, моноциты.
CD232
Плексин C1 (PLXNC1) (12q233). Молекулярная масса 200 кДа. Рецептор для семафоринов, кодируемых генами вирусов. Экспрессируется на многих клетках.
CD233
Гликопротеин плазматической мембраны эритроцитов (17q21-q22). Молекулярная масса 93-110 кДа. Относится к антигенам группы крови Diego (D1). Через интегральный домен обеспечивает транспорт через мембрану (обмен 1:1) неорганических анионов. Через цитоплазматический домен связан с белками цитоскелета, гемоглобином и белками гликолиза. Сохраняет механические свойства и интегрированность эритроцитов.
CD234
Гликопротеин Fy (1q21-q22). Антиген группы крови Duffy. Рецептор эритроцитов для многих хемокинов (ИЛ-8, RANTES, MCP-1, GRO, TARC), а также для Plasmodium vivax и P. knowlesi. Молекулярная масса 35 кДа. (+) - эритроциты; эндотелий посткапиллярных венул, синусоидов селезёнки и костного мозга; клетки Пуркинье мозжечка, эпителий почки и лёгочных альвеол.
CD235
Гликофорины. (+) - (норма): эритроидные клетки.
• CD235a (гликофорин А). Несёт детерминанты антигенов групп крови MN и Ss. N-концевой сегмент служит рецептором для вируса гриппа. • CD235b (гликофорин B). Несёт детерминанты антигенов группы крови Ss). • CD235ab (гликофорин A/B).
CD236
Гликофорин C/D. (+) - эритроидные клетки.
CD236R (гликофорин C). Антиген группы крови Gerbich. Регулирует механическую стабильность эритроцитов. При мутациях кодирующего гена возникают гликофорины D, известные как антигены групп крови Gerbich и Duch. (+) - эритроидные клетки, некоторые стволовые клетки.
CD238
Антиген группы крови Kell(7q33).Трансмембранный гликопротеин. (+) - (норма): эритроидные клетки, некоторые стволовые клетки.
CD239
B-CAM. B-клеточная молекула адгезии (19q13.2). Антиген группы крови Lutheran. Антиген b группы крови Auberger. Гликопротеин суперсемейства иммуноглобулинов. (+) - (норма): эритроидные клетки, некоторые стволовые клетки.
CD240CE
Антигены Rh - Cc и Ee. (+) - (норма): эритроидные клетки.
CD240D
Антиген Rh D. (+) - (норма): эритроидные клетки.
CD240DCE
Антиген Rh. Выявляется моноклональными антителами Rh30D/CE. (+) - (норма): эритроидные клетки.
CD241
Антиген Rh (6p21.1-p11). Участвует в процессах транспорта аммония. Является частью макромолекулярных комплексов с CD48, а также антигенов группы крови Ландштейнера-Винера (Landsteiner-Wiener) и гликофорина B. (+) - (норма): эритроидные клетки.
CD242
ICAM-4 (Intercellular Adhesion Molecule 4) - молекула межклеточной адгезии 4. Антиген группы крови Ландштейнера-Винера (Landsteiner- Wiener) - LW. Принадлежит к суперсемейству иммуноглобулинов. Взаимодействует с интегрином LFA-1. (+) - (норма): эритроидные клетки.
CD243
MDR-1. П-гликопротеин типа 1 (7q21.1). Член семейства белковтранспортёров ABC (ATP-Binding Cassette - АТФ-связывающих), осуществляющих транспорт различных веществ через наружные и внутренние мембраны клеток. В норме MDR-1 также транспортирует вещества через гематоэнцефалический барьер. В раковых клетках выполняет функцию насоса, выводящего из клеток химиотерапевтические препараты, приводя к снижению их токсичности. Отвечает за развитие множественной лекарственной устойчивости (MDR - MultiDrug Resistance). (+) - (норма): кора надпочечников, жёлчные канальцы; эндотелий капилляров мозга; яички, плацента, пищеварительный тракт, стволовые клетки.
CD244
2B4. Активационный рецептор NK-клеток (OMIM 605554; 1q22). Молекулярная масса 70 кДа. Относится к мембранным гликопротеинам подсемейства CD2 и входит в состав суперсемейства иммуноглобулинов. Функционирует как корецептор активирующего рецептора
NK-клеток NKp46. Участвует в цитолитических реакциях NK-клеток. С высокой степенью аффинности связывается с CD48. Экспрессируется на всех NK-лимфоцитах и у5Т-лимфоцитах, моноцитах, базофилах, на CD8+ T-клетках (50%) и на CD4+ T-лимфоцитах (0,5-5%). На B-клетках отсутствует.
CD245
p220/240. Рецептор лимфоцитов. Экспрессируется на части Т-клеток.
CD246
Киназа анапластической лимфомы (Alk, Alk-1 - Anaplastic lymphoma kinase) (2p23). Протеинтирозинкиназный рецептор с внеклеточным и трансмембранным доменами. Играет значимую роль в развитии мозга, влияет на специфические нейроны центральной нервной системы. Сходен с киназами суперсемейства рецепторов для инсулина. (+) - (норма): кишечник, T-клетки.
CD247
Также известный как CD3Z (Z) (OMIM 186780; 1q22-q23). Полипептидная цепь дзета - ζ. Молекулярная масса 12 кДа. В виде гомодимера формирует совместно с цепями δ, γ и ε CD3 внутриклеточную область комплекса молекул TCR. Каждая из ζ-цепей содержит по 3 домена ITAM c функцией проведения сигнала, инициированного взаимодействием лиганд-рецептор. (+) - (норма): αβT-клетки или γδT-клетки.
CD248
TEM1. Эндосиалин (Endosialin). Молекулярная масса 175 кДа. Поверхностный эндосиалин. Экспрессируется преимущественно фибробластами и субпопуляцией перицитов (малодифференцированные соединительнотканные клетки, примыкающие к наружной поверхности капилляра), ассоциированных с сосудами. Внутриклеточный маркёр эпителиальных опухолей, но не нормального эндотелия. Локализуется совместно с тромбомодулином (CD141) и, возможно, играет роль в ангиогенезе опухолей.
CD249
Глютамиламинопептидаза (аминопептидаза А), ассоциированная с мембраной. Металлопептидаза. Деградирует биоактивные пептиды, включая ангиотензин II. Молекулярная масса 160 кДа. Экспрессия возрастает на клетках карциномы под влиянием сосудистого эндотелиального ростового фактора (VEGF) и при взаимодействии между клетками опухоли и стромы (фибробластами).
CD251-300
[править]CD252
TNFSF4 [Tumor Necrosis Factor (ligand) Superfamily, member 4]. Молекулярная масса 34 кДа. Цитокин семейства лигандов фактора некроза опухоли. Служит лигандом рецептора TNFRSF4. Участвует во взаимодействии между Т-лимфоцитами и АПК, В-клетками, NK-лимфоцитами, тучными клетками. Опосредует адгезию активированных Т-клеток к эндотелию сосудов. CD252 селективно индуцирует Th2-тип иммунного ответа, повышая выработку CD4+ Т-клетками ИЛ-4, ИЛ-5 и ИЛ-13. Полиморфизм TNFSF4 повышает риск развития атеросклероза.
CD253
TRAIL (Tumor Necrosis Factor-Related Apoptosis Inducing Ligand). TNFSF10 [Tumor Necrosis Factor (ligand) SuperFamily, member 10]. Молекулярная масса 33-34 кДа. Цитокин семейства лигандов фактора некроза опухоли. Связывается с некоторыми членами суперсемейства рецепторов фактора некроза опухоли. Участвует в регуляции активации Т-клеток человека. CD253 играет важную роль в апоптозе клеток эпителия желудка под влиянием Helicobacter pylori. Индуцирует апоптоз преимущественно в трансформированных и опухолевых клетках, хотя активно экспрессируется клетками большинства нормальных тканей. (+) - (патология): выявляют в поражённых участках мозга больных болезнью Альцгеймера.
CD254
TNFSF11 [Tumor Necrosis Factor (ligand) SuperFamily, member 11]. Молекулярная масса 35 кДа. Член цитокинового семейства лигандов фактора некроза опухоли - лиганд остеопротегерина (фактор развития и активации остеокластов). Важен для остеокластогенеза. Один из факторов выживаемости ДК при их взаимодействии с Т-лимфоцитами в очаге воспаления. Может опосредовать связь между сосудистой, скелетной и иммунной системами. Играет центральную роль в регуляции кальцификации сосудов. Экспрессия CD254 повышена при периодонтите.
CD255
TWEAK. TNFSF12 [Tumor Necrosis Factor (ligand) SuperFamily, member 12]. Молекулярная масса 18 кДа. Член цитокинового семейства лигандов фактора некроза опухоли - лиганд TWEAKR (CD266). Существует в мембраносвязанной и растворимой формах. Экспрессируется моноцитами, эндотелиальными клетками и лимфоцитами при стимуляции ИФНу.
CD256
APRIL. TNFSF13 [Tumor Necrosis Factor (ligand) SuperFamily, member 13]. Молекулярная масса 16 кДа. Член семейства лигандов фактора некроза опухоли. Служит лигандом для TNFRSF17 - члена семейства рецепторов фактора некроза опухоли. Важен для развития В-клеток. Уровни растворимых CD256 и CD257 молекул повышены в сыворотке при синдроме Шегрена и при множественной миеломе, а уровень CD256 - при хроническом В-клеточном лимфолейкозе. В основном CD256 и CD257 вырабатываются моноцитами и нейтрофилами в костном мозге. Гепарин-сульфат протеогликан служит рецептором CD256. CD256 способствует физиологической выработке тромбоцитов.
CD257
TNFSF13B [Tumor Necrosis Factor (ligand) SuperFamily, member 13b]. Молекулярная масса 45 кДа. Синонимы - BAFF и BLyS (B-cell Activating Factor - В-клеточный активирующий фактор). Цитокин семейства лигандов фактора некроза опухоли. Служит лигандом рецепторов TNFRF13B, TNFRF17 и TNFSF13C. Экспрессируется на Т-лимфоцитах, макрофагах, ДК. Существует также в секретируемой форме. Аутокринно секретируется активированными В-клетками и действует как сильный активатор их развития. Вместе с CD256 поддерживают выживаемость лейкозных В-клеток. Защищает В-клетки от апоптоза в условиях воспаления. Уровень растворимого CD257 повышен при системной красной волчанке, ревматоидном артрите, синдроме Шегрена, множественной миеломе. Играет роль во взаимодействии между моноцитами (продуцентами CD257) и В-лимфоцитами при некоторых аутоиммунных заболеваниях.
CD258
TNFSF14 [Tumor Necrosis Factor (ligand) SuperFamily, member 14]. Молекулярная масса 28 кДа. Цитокин семейства лигандов фактора некроза опухоли. Служит лигандом для TNFRSF14 и рецептора лимфотоксина β. Трансмембранный белок типа II. Имеет 30% идентичность с FasL и лимфотоксином β. Экспрессируется на активированных лимфоцитах и незрелых ДК, способствуя их созреванию. Стимулирует пролиферацию Т-клеток и запускает апоптоз различных опухолевых клеток. CD258 опосредует взаимодействие между Т-клетками и АПК. Присутствует на NK-клетках и Т-лимфоцитах кишечника и играет роль в регуляции иммунных процессов на слизистых оболочках.
CD261
TNFRSF10A (Tumor Necrosis Factor Receptor SuperFamily, member 10a). Молекулярная масса 57 кДа. Белок суперсемейства рецепторов фактора некроза опухоли, ответственный за передачу «сигнала смерти». Активируется под влиянием лиганда TNFSF10/TRAIL. Этот цитотоксический лиганд принадлежит к семейству фактора некроза опухоли и индуцирует апоптоз в клетках-мишенях. Запуск апоптоза реализуется с участием дополнительного цитоплазматического адапторного белка, содержащего домен смерти (FADD - Fas-Associated Death Domain). CD261 широко распространён на опухолевых (клетки саркомы желудка) и нормальных клетках, включая тимоциты человека, миелоидные предшественники, нейроны, астроциты, олигодендроциты. Полиморфизм CD261 ассоциируется с риском развития рака мочевого пузыря.
CD262
TNFRSF10B (Tumor Necrosis Factor Receptor SuperFamily, member 10b). Белок суперсемейства рецепторов фактора некроза опухоли. Содержит внутриклеточный домен смерти. Молекулярная масса 60 кДа. CD262 активируется через лиганд TNFSF10. CD262 широко представлен на нормальных и опухолевых клетках. Выявлен на тимоцитах человека, на клетках HepG2, инфицированных вирусом Денге 2. CD261 и CD262 отличаются по используемым факторам трансдукции сигнала и силе индукции апоптоза опухолевых клеток. Синовиальные клетки больных ревматоидным артритом экспрессируют высокий уровень CD262 и высоко чувствительны к апоптозу, индуцированному через CD262. При холестазе в печени возрастает экспрессия мРНК и белка CD262.
CD263
TNFRSF10C (Tumor Necrosis Factor Receptor Superfamily, member 10c). Молекулярная масса 65 кДа. Белок суперсемейства рецепторов фактора некроза опухоли. Заякорен в мембране через гликофосфатидилинозитовый хвост. Апоптоз не запускает, но играет роль антагонистического рецептора, защищающего клетки от апоптоза. CD263 присутствует на клетках многих нормальных тканей и большинства опухолевых линий.
CD264
TNFRSF10D (Tumor Necrosis Factor Receptor SuperFamily, member 10d). Молекулярная масса 35 кДа. Белок суперсемейства рецепторов факто-
ра некроза опухоли. Содержит усечённый нефункционирующий цитоплазматический домен смерти. Рецептор не запускает апоптоз и играет роль ингибитора апоптоза. На клетках периферической крови здоровых людей экспрессируются разные рецепторы анализируемой серии: TRAILR1 - В-лимфоциты, TRAILR2 - моноциты, TRAILR3 - нейтрофилы. (+) - CD8+ Т- и NKT-лимфоциты. (-) - CD4+ Т-клетки.
CD265
TNFRSF11A (Tumor Necrosis Factor Receptor SuperFamily, member 11a). Молекулярная масса 97 кДа. Белок суперсемейства рецепторов фактора некроза опухоли. Может взаимодействовать с разными белками TRAF семейства и активировать NF-kB (NF-kB-активатор) и MAPK8/JNK киназы. Участвует в кооперации Т-лимфоцитов и ДК в процессе воспаления. CD265 может играть ключевую роль в регуляции кальцификации сосудов и быть связан с возрастным снижением минерализации, остеопорозом, атеросклерозом и различными метаболическими патологиями. (+) - соматические и гемопоэтические клетки (макрофаги, ДК и другие клетки).
CD266
TNFRSF12A (Tumor Necrosis Factor Receptor SuperFamily, member 12a). Трансмембранный белок типа I. Член суперсемейства рецепторов фактора некроза опухоли. Молекулярная масса 14 кДа. Активирует NF-kB, индуцирует экспрессию антиапоптозных белков BCL-XL и ВCL-W. Участвует в запуске апоптоза некоторых опухолевых клеток, а также может отвечать за индукцию пролиферации клеток эндотелия и ангиогенез. (+) - клетки глиомы, влияет на клеточную устойчивость к цитотоксической терапии, вызывающей апоптоз. CD266 постоянно экспрессируется на культивируемых фибробластах человека, которые в ответ на связывание лиганда TNFSF12/TWEAK вырабатывают хемокин RANTES.
CD267
TNFRSF13B (Tumor Necrosis Factor Receptor SuperFamily, member 13b). Молекулярная масса 32 кДа. Специфичный для лимфоцитов член суперсемейства рецепторов фактора некроза опухоли. Лиганд - CAML (Calcium-Modulator and cyclophilin Ligand) через CD267 вызывает активацию факторов транскрипции NFAT, AP-1 и NF-kB и играет важную роль в гуморальном иммунитете.
CD268
BAFFR. TNFRSF13C (Tumor Necrosis Factor Receptor SuperFamily, member 13c). Молекулярная масса 25 кДа. Трансмембранный белок типа III суперсемейства рецепторов фактора некроза опухоли, содержащий один внеклеточный домен, обогащённый цистеином. Главный рецептор, необходимый для выживаемости нормальных зрелых В-лимфоцитов и регуляции периферической популяции В-клеток. Поддерживает рост и выживаемость клеток множественной миеломы. Через CD268 регулируется выживаемость и созревание В-клеток при системной красной волчанке.
CD269
TNFRSF17 (Tumor Necrosis Factor Receptor SuperFamily, member 17). Молекулярная масса 27 кДа. Важный регулятор функции В-клеток. Во внеклеточном участке рецептор содержит полный или частичный домен, обогащённый цистеином. Белок суперсемейства рецепторов фактора некроза опухоли (рецептор для BAFF и APRIL). (+) - селективно экспрессируется зрелыми В-лимфоцитами и важен для их развития и аутоиммунного ответа. Присутствует на клетках множественной миеломы.
CD270
TNFRSF14 (Tumor Necrosis Factor Receptor SuperFamily, member 14). Молекулярная масса 30 кДа. Активатор лимфоцитов. Белок суперсемейства рецепторов фактора некроза опухоли (рецептор для BTLA, TNFSF14/LIGHT и лимфотоксина альфа). Экспрессируется разными популяциями лимфоцитов и лейкоцитов. Этот рецептор используется вирусом простого герпеса (HSV) для проникновения в активированные Т-лимфоциты.
CD271
NGFR (Nerve Growth Factor Receptor). Рецептор фактора роста нервов. Молекулярная масса 75 кДа. CD271 участвует в регуляции выживаемости, дифференцировки и миелинизации нейронов и, в зависимости от типа анализируемых клеток мишеней, индуцирует выживаемость или апоптоз. CD271 служит одним из наиболее специфических маркёров мезенхимальных стволовых клеток, происходящих из костного мозга. Может опосредовать клеточную гибель в разных моделях, включая нейроны гиппокампа. Обнаружен в пренатальном гипофизе человека. В развивающейся сетчатке глаза клеточная гибель происходит в результате взаимодействия фактора роста нервов с CD271. Это взаимодействие может играть роль в патогенезе дегенерации нервов при болезни Альцгеймера.
BTLA (B and T Lymphocyte Associated). Важный негативный регулятор активации Т-лимфоцитов и/или гомеостаза иммунного ответа. (+) - экспрессируется в процессе активации Т-клеток и сохраняется на Th1-клетках, а также на развивающихся Т- и В-клетках, всех зрелых лимфоцитах, селезёночных макрофагах, зрелых ДК костномозгового происхождения. (-) - Th2-клетки.
CD273
PDCD1LD2 (Programmed Cell Death 1 Ligand 2). Молекулярная масса 25 кДа. Негативный регулятор активации Т-клеток. Играет важную роль в уклонении опухоли от действия иммунной системы. Экспрессия CD273 может контролироваться на посттранскрипционном уровне через альтернативный сплайсинг. Модуляция изоформы CD273 может влиять на исход иммунного ответа. У человека экспрессия CD273 обратно коррелирует с уровнем CD8+ Т-клеток, инфильтрирующих рак пищевода.
CD274
B7-H1 или PD-L1 (см. CD273). Молекулярная масса 40 кДа. Регуляторная молекула, член семейства В7. Присутствует постоянно на моноцитах, макрофагах и ДК и индуцируется на активированных Т- и В-лимфоцитах, клетках эпителия и эндотелия. Белок суперсемейства иммуноглобулинов. Положительная регуляторная роль PD-L1 показана преимущественно in vitro и на экспериментальных моделях, тогда как отрицательная регуляторная роль показана при многих заболеваниях человека (рак, ревматоидный артрит, ВИЧ-инфекция). Может вовлекаться в иммунное отклонение при развитии ряда опухолей. Поверхностная экспрессия и количество мРНК PD-L1 и выработка ИЛ-10 возрастают при инфекции ВИЧ-1 и снижаются после высокоактивной противоретровирусной терапии.
CD275
B7-H2. ICOSLG (Inducible T cell Co-Stimulator Ligand). ICOSL (см. CD274). Молекулярная масса 60 кДа. Экспрессия функциональной молекулы ICOSL может привести к прогрессированию острого миелолейкоза. Костимуляция через ICOS-ICOSL может участвовать в отрицательной регуляции клеточного иммунного ответа и способствовать уклонению опухоли от иммунной системы. Взаимодействие ICOS- ICOSL играет роль в патогенезе волчаночного нефрита. CD275 экспрессируют клетки эпителия дыхательных путей. Возможно, эти молекулы могут участвовать в презентации антигена эпителиальными клетками, а также в активации Т-клеток памяти.
CD276
B7-H3. Член семейства В7. Костимулятор молекул В7 (В7.1, или CD80), действующий через молекулы семейства CD28 (CD28, CTLA4 и ICOS). Молекулярная масса 40-45 кДа. (+) - представлен на моноцитах. Его экспрессию на ДК могут индуцировать провоспалительные цитокины. Растворимые молекулы B7-H3 человека соединяются с активированными Т-лимфоцитами и костимулируют их пролиферацию и выработку этими клетками преимущественно ИФНу. B7-H3 экспрессируют клетки назального эпителия. Они могут через этот рецептор взаимодействовать с активированными назальными Т-лимфоцитами.
CD277
BTN3A1 (Butyrophilin, subfamily 3, member A1). Член суперсемейства иммуноглобулинов. Молекулярная масса 56 кДа. Присутствует на лимфоцитах, моноцитах. Участвует в активации Т-лимфоцитов.
CD278
ICOS (Inducible T-cell Co-Stimulator). Белок семейства рецепторов CD28 и CTLA4. Молекулярная масса 56 кДа. Играет важную роль в межклеточной передаче сигналов, иммунном ответе и регуляции пролиферации клеток. Уровень ICOS повышается на Т-клетках человека после стимуляции с модуляцией выработки Th1- и Th2-цитокинов. Усиливает костимулирующий эффект в отношении Т-клеток памяти. Экспрессия ICOS на активированных Т-хелперах (преимущественно Th2) может усиливать эффекторный Т-клеточный ответ в периферических тканях. Взаимодействие ICOSL-ICOS активно усиливает выработку ИЛ-10. Локальный иммунный ответ может модулироваться под влиянием ICOS на Т-клетках в суставах больных ревматоидным артритом.
CD279
PD-1 (Programmed cell Death). Поверхностный мембранный белок суперсемейства иммуноглобулинов. Молекулярная масса 55 кДа. Участвует в индукции толерантности лимфоцитов. Взаимодействует с CD274. Экспрессируется на активированных Т- и В-лимфоцитах, миелоидных клетках. PD-1 выявляют на Т-лимфоцитах, а его лиганд PD-L1 - на клетках эпителия при воспалении слюнных желёз у больных синдромом Шегрена. Полиморфизм гена, кодирующего PD-1, ассоциируется с чувствительностью к ревматоидному артриту.
MRC2 (Mannose Receptor C type 22). Молекулярная масса 180 кДа. Семейство рецепторов маннозы включает: маннозный рецептор, рецептор М-типа фосфолипазы А2. CD280 не функционирует в качестве фагоцитарного рецептора in vitro. CD280 играет важную физиологическую роль в деградации и ремодулировании внеклеточного матрикса в процессе развития тканей и гомеостаза. Вызывая дисбаланс метаболизма коллагена, CD280 может участвовать в развитии патологических процессов, таких, как воспаление, фиброз и метастазирование опухоли.
CD281
TLR1 (Toll-Like Receptor 1). Молекулярная масса 90 кДа. Член семейства Toll-подобных рецепторов, играющих главную роль в распознавании патогенов и активации врождённого иммунитета. Реагирует с бактериальным липопротеином.
CD282
TLR2 (Toll-Like Receptor 22). Молекулярная масса 85 кДа. Член семейства Toll-подобных рецепторов. Реагирует с пептидогликаном. Экспрессируется, преимущественно, лейкоцитами периферической крови и опосредует ответ на грамположительные бактерии и грибы через стимуляцию NF-kB.
CD283
TLR3 (Toll-Like Receptor 3). Молекулярная масса 100 кДа. Член семейства Toll-подобных рецепторов. В большом количестве представлен в плаценте, поджелудочной железе и на миелоидных ДК. Распознаёт двуцепочечную РНК, ассоциированную с вирусной инфекцией. Вызывает активацию NF-kB и выработку провоспалительных цитокинов и интерферонов типа I. Может участвовать в противовирусной защите.
CD284
TLR4 (Toll-Like Receptor 4). Молекулярная масса 85 кДа. Член семейства Toll-подобных рецепторов. Экспрессируется преимущественно на клетках плаценты и незрелых миелоидных ДК. Связывает ЛПС, присутствующий у большинства грамотрицательных бактерий. Мутации гена обусловливают различия по отвечаемости на ЛПС.
CD286
TLR6 (Toll-Like Receptor 6). Член семейства Toll-подобных рецепторов. Функционально димеризуется с TLR2 для реализации клеточного ответа на бактериальные липопротеины.
TLR8 (Toll-Like Receptor 8). Член семейства Toll-подобных рецепторов. Экспрессируется преимущественно лейкоцитами лёгких и периферической крови. Взаимодействует с пареховирусом человека типа 1 и активирует сигналы, приводящие к выработке провоспалительных молекул.
CD289
TLR9 (Toll-Like Receptor 9). Молекулярная масса 115-120 кДа. Член семейства Toll-подобных рецепторов. Экспрессируется преимущественно в тканях, обогащённых иммунными клетками (селезёнка, лимфатические узлы, костный мозг), а также на лейкоцитах периферической крови. Лиганд - неметилированные CpG олигодинуклеотиды бактериальной ДНК. CpG стимулирует экспрессию TLR9 на В-клетках.
CD290
TLR10 (Toll-Like Receptor 10). Член семейства Toll-подобных рецепторов. N-гликозилированный белок. Высокоэкспрессирован на клетках в селезёнке, лимфатических узлах, тимусе, лёгких. Выявляют на В-клетках периферической крови, плазмоцитоидных ДК миндалин. Генетические варианты TLR10 связаны с риском развития бронхиальной астмы.
CD292
BMPR1A (Bone Morphogenetic Protein Receptor, type 1A). Молекулярная масса 50-58 кДа. Рецептор белка, участвующего в остеогенезе (ВМР). Принадлежит к семейству трансмембранных серин-треониновых киназ, включающих рецепторы типа I (BMPR1A и BMPR2A) и типа II (BMPR2). Тесно связаны с рецепторами активина (ACVR1 и ACVR2). Лигандами CD292 служат члены суперсемейства ТФРР. Поверхностная экспрессия и интернализации BMPR1A нарушены у больных прогрессирующей фиброзной остеодисплазией (болезнь Лихтейнштайна-Брайцева). У эмбрионов и взрослых людей CD292 высоко и специфически экспрессируется всеми клетками ганглиев нервной системы кишечника. Генетические мутации зародышевой линии в BMPR1A выявляют у некоторых больных юношеским полипозом и больных болезнью Коудена.
CDw293
BMPR1B (Bone Morphogenetic Protein Receptor, type 1B) (см. CD292). CDw293 член семейства трансмембранных серин-треониновых киназ. Молекулярная масса 50-58 кДа. Лиганды CDw293 - белки, участвующие в остеогенезе (BMP), входящие в суперсемейство фактора некроза опухоли p. BMP вовлекаются в эндохондриальное образование кости и в эмбриогенез. Через BMPR1B опосредуется апоптоз остеобластных клеток, независимо от их дифференцировки. Мутации гена, кодирующего CDw293, ассоциированы с первичной лёгочной гипертензией.
CD294
GPR44 (G Protein-Coupled Receptor 44). Член семейства рецепторов, соединённых с белком G. Интегральный мембранный белок, содержащий 7 трансмембранных доменов. Молекулярная масса 55-70 кДа. CD294 в качестве хемоаттрактантного рецептора простагландина D2 опосредует его провоспалительное действие. Провоспалительные эффекты CD294 связаны с привлечением эозинофилов и Th2-клеток в очаг воспаления. Присутствует на базофилах, эозинофилах. Селективно экспрессируется на Th2-, но не Th1-лимфоцитах. При атопическом дерматите увеличивается количество CD4+ CD294+ Тh2-клеток. Характерна ассоциация генетических вариантов CD294 с бронхиальной астмой.
CD295
LEPR (Leptin Receptor). Молекулярная масса 130-150 кДа. Лиганд CD295 - гормон лептин, участвующий в контроле состояния сытости, расхода энергии, потребления пищи и ряда репродуктивных процессов. Лептин регулирует пролиферативную и антиапоптотическую активность многих типов клеток, включая Т-лимфоциты; стимулирует макрофаги и нейтрофилы в процессе воспаления. Через CD295 лептин замедляет апоптоз зрелых нейтрофилов in vitro. (+) - CD295 выявляют на поверхности клеток многих тканей: в мозге, плаценте, поджелудочной железе, надпочечниках, печени, сердце, лёгких, на гемопоэтических клетках, а также на опухолевых клетках (рак лёгких, желудка, эндометрия, молочной железы, на лейкозных клетках). Тромбоциты рассматривают как главный источник лептиновых рецепторов в циркуляции.
CD296
ART1 (ADP-RibosylTransferase 1). Молекулярная масса 37 кДа. АДФ-рибозилтрансфераза катализирует рибозилирование АДФ на остатке аргинина в белке. Аргининспецифические моно-АДФрибозилтрансферазы опосредуют модификацию белков на посттрансляционной стадии. ART1 локализуется на поверхности клеток многих тканей, включая лейкоциты, и прикреплён к мембране через GPI-якорь. CD296 участвует в контроле цитолитической активности, пролиферации и межклеточной адгезии ЦТЛ. На поверхности нейтрофилов человека ART1 участвует в реализации их каталитической активности.
ART4 (ADP-RibosylTransferase 4) антиген группы крови Dombrock. Моно-АДФ-рибозилтрансфераза типа 4 относится к семейству эктоферментов, катализирующих перенос АДФ-рибозы из NAD+ в намеченный белок. Молекулярная масса 38 кДа. Антиген группы крови Dombrock локализуется на генном продукте, заякоренном через GPI на мембране эритроцита. Аллельные варианты CD297 могут быть связаны с трансфузионными осложнениями.
CD298
ATP1B3 (ATPase, Na+/K+ transporting, Beta 3 polypeptide). Молекулярная масса 50-60 кДа. CD298 является одной из бета-субъединиц Na+/ K+ АТФазы, интегрального мембранного белка, ответственного за установление и поддержание электрохимического градиента ионов Na+ и К+, проникающих через плазматическую мембрану, что важно для электрической возбудимости нервов и мышц.
CD299
CLEC4M (C-type Lectin domain family 4 member M). Интегральный мембранный белок типа II на 77% идентичный CD209. Молекулярная масса 45 кДа. Участвует в распознавании разных гликопротеинов через лектиновый домен, опосредующий узнавание углеводов. CD299 выявляют в клетках слизистых оболочек влагалища и прямой кишки. CD299 рассматривают как кофактор в половом пути трансмиссии ВИЧ-1. Опосредует проникновение в клетки вируса Эбола.
CD300a
CMRF35H. Член суперсемейства иммуноглобулинов с одним V-подобным иммуноглобулиновым доменом. В цитоплазматическом домене содержит ITIM. Молекулярная масса 60 кДа. Обладает свойством иммунорегуляторных сигнальных молекул. Присутствует преимущественно на миелоидных клетках (моноциты, нейтрофилы), а также на некоторых Т- и В-клетках.
CD300c
CMRF35A. Лейкоцитарный иммуноглобулиноподобный рецептор. Так же как CD300a - член семейства иммунорегуляторных сигнальных молекул, играющих важную роль в регуляции иммунного ответа. Экспрессирован на моноцитах, нейтрофилах, некоторых Т- и В-лимфоцитах.
CD300e
CMRF35L1. Экспрессирован на моноцитах, макрофагах.
CD301-400
[править]CD301
CLEC10A (C-type Lectin domain family 10, member A). Молекулярная масса 38 кДа. Член суперсемейства молекул с доменом, подобным лектину С-типа. Трансмембранный белок типа II функционирует как поверхностный клеточный антиген, в частности, на макрофагах. Участвует в адгезии, межклеточной передаче сигналов, в воспалительном и иммунном ответах. Может связывать Т-независимые антигены.
CD302
DCL-1. Трансмембранный лектин С-типа I. DCL-1 - необычный лектиновый рецептор, важный не только для эндоцитоза и фагоцитоза, но и для адгезии и миграции клеток. В качестве фузионного белка с DЕС-205 (CD205) экспрессируется на линиях клеток Березовского-Штенберга, имеющих многие характеристики АПК и связанных с развитием классической лимфомы Ходжкина. Молекулярная масса 30 кДа. В норме экспрессируется на моноцитах, макрофагах, гранулоцитах и ДК.
CD303
CLEC4C (C-type Lectin domain family 4, member C) (см. CD301). Молекулярная масса 38 кДа. Трансмембранный белок типа II может играть роль в реализации функций ДК (в частности, плазмоцитоидных ДК). Подавляет синтез ИФНα этими клетками.
CD304
NRP1 (NeuRoPilin 1 - нейронный рецептор). Молекулярная масса 140 кДа. Связанный с клеточной мембраной корецептор тирозинкиназного рецептора (VEGFR2) для членов семейств фактора роста сосудистого эндотелия (VEGF; мощный медиатор проницаемости эндотелия, хемотаксиса и пролиферации) и семафорина. Многофункциональный рецептор, участвующий в ангиогенезе, росте аксонов, а также выживаемости, миграции и инвазии клеток. Нейронный рецептор CD304 экспрессируется ДК и покоящимися Т-клетками человека. Высокий уровень CD304 на клетках многих опухолей усиливает ангиогенез. Сверхэкспрессия гена NRP1 коррелирует с плохим прогнозом глиомы человека.
CD305
LAIR-1 (Leukocyte-Associated Ig-like Receptor 1). Принадлежит к суперсемейству иммуноглобулинов и семейству ингибиторных рецепторов,
ассоциированных с лейкоцитами. Молекулярная масса 40 кДа. Особенность LAIR-1 - широкая представленность в иммунной системе и неспособность распознавать молекулы MHC-I. CD305 экспрессирован на большинстве периферических мононуклеарных клеток, включая NK-клетки, Т-лимфоциты, В-лимфоциты, моноциты, ДК, а также тимоциты. Плотность экспрессии CD305 непосредственно связана с подавлением функций Т-лимфоцитов человека, включая цитотоксичность, пролиферацию, выработку цитокинов. Хроническая с обострениями инфекция вирусом Эпштейна-Барр ассоциируется с низкой экспрессией LAIR-1 на NK-клетках.
CD306
LAIR-2 (Leukocyte-Associated Ig-like Receptor 2). Сходен с LAIR-1. Экспрессирован на мононуклеарных лейкоцитах и обладает свойствами ингибиторного рецептора.
CD307
FCRL5 (Fc Receptor-Like 5). Молекулярная масса 100 кДа. CD307 участвует в клеточной дифференцировке, иммунном ответе и, возможно, в развитии В-клеточных опухолей.
CD309
VEGFR2/KDR [Kinase insert Domain Receptor (a type III receptor tyrosine kinase)]. Рецептор - тирозинкиназа. Один из рецепторов для важного ангиогенного цитокина VEGF (сосудистый пермеабилизирующий фактор). Молекулярная масса 230 кДа. CD309 присутствует на плазматической мембране, эндосомах и околоядерной области клеток эндотелия и колокализуется с передающей сигнал ГТФазой, вовлекаемой в эндоцитоз рецептора. В ответ на связывание лиганда тирозинкиназный домен VEGFR2 проводит внутрь клетки сигналы, ответственные за митогенное действие, хемотаксис, клеточную проницаемость и выживаемость сосудистого эндотелия. Экспрессия CD309 играет важную роль в ангиогенезе, в том числе саркомы Капоши, связанной с синдромом приобретённого иммунодефицита.
CD312
EMR2 (Egf-like module containing, Mucin-like, hormone Receptor-like 2). Принадлежит к классу В семейства спаниновых трансмембранных рецепторов, 7-кратно пронизывающих клеточную мембрану (TM7). Молекулярная масса 90 кДа. Экспрессируется преимущественно миелоидными клетками, а также гладкомышечными клетками. CD312 опосредуют межклеточное прилипание через лиганд хондроитинсульфат из группы глюкозаминогликанов.
CD314
KLRK1 (Killer cell Lectin-like Receptor subfamily K, member 1). Молекулярная масса 42 кДа. В качестве активационного рецептора экспрессируется на всех NK-клетках, γδТ-клетках и на большинстве CD8+ Т-клеток. CD314 принадлежит к семейству молекул NKG2, экспрессируемых, главным образом, NK-клетками и представленных трансмембранными белками с характерным типом II мембранной ориентации (внеклеточный С-конец) и с зависимым от кальция С-типом лектиновым доменом. В ответ на инфицирование цитомегаловирусом человека фибробласты экспрессируют лиганды NKG2D и становятся чувствительными к лизису NK-клетками.
CD315
PTGFRN (Prostaglandin F2a Receptor Negative regulator). Молекулярная масса 135 кДа. Регуляторный белок рецептора простагландина F2α. Поверхностный белок суперсемейства иммуноглобулинов, включающий 6 внеклеточных иммуноглобулиновых доменов. С высокой специфичностью и стехиометричностью ассоциирует с CD81 или с CD81 и CD9 (комплекс CD81-CD9-FPRP), но не с интегринами или другими TM4SF-белками. PTGFRN взаимодействует с рецептором простагландина F2α и, возможно, с другими 7-кратно пронизывающими мембрану трансмембранными рецепторами, что приводит к снижению способности данных рецепторов связывать лиганд.
CD316
Предыдущее название CD81P3. IGSF8 (Immunoglobulin SuperFamily, member 8). PGRL (Prostaglandin regulatory-like) / (OMIM 606644; 1q23.1). Молекулярная масса 63 кДа. Принадлежит к суперсемейству иммуноглобулинов. Ассоциируется с тетраспанинами CD9, CD81 и CD82, образуя сеть молекулярных взаимодействий - тетраспаниновую паутину. (+) - на поверхности свежевыделенных гепатоцитов в связи с CD81, на большинстве В- и Т-лимфоцитов, NK-клеток. CD316 образует высокостехиометрический комплекс с CD82 и участвует в подавлении миграции раковых клеток, опосредованном через CD82.
CD317
BST2 (Bone marrow Stromal cell antigen 2). Костномозговые стромальные клетки вовлекаются в развитие и рост В-лимфоцитов. Играет роль в развитии пре-В-клеток и в патогенезе ревматоидного артрита.
CDCP1 (CUB Domain Containing Protein 1). Молекулярная масса 140 кДа. Под влиянием плазмина (сывороточная протеаза) и при адгезии происходит конверсия gp140 в р80. Фосфорилирование gp140 и р80 опосредуется через Src-семейство киназ на тирозиновых остатках, в частности, в эпидермальных ранах. Присутствует на поверхности метастазирующих клеток рака толстой кишки, лёгких, грудной железы, на лейкозных бластных клетках (преимущественно CD34+CD133+ миелолейкозных бластах), гемопоэтических стволовых клетках, негемопоэтических клетках с фенотипом стволовых и родоначальных (мезенхимальные стволовые клетки, нервные родоначальные клетки). Экспрессируется эпителиальными клетками нормальной толстой кишки.
CD319
SLAMF7 (SLAM Family member 7). Молекулярная масса 66 кДа. Участвует в регуляции адгезии лимфоцитов. Экспрессируется активированными NK-клетками, цитотоксическими лимфоцитами, активированными В-клетками, зрелыми ДК. CRACC является аутолигандом, и гомофильное взаимодействие CRACC регулирует цитолитическую активность NK-клеток.
CD320
8D6A. Белок массой 30 кДа, присутствующий на ФДК, блокада которого приводит к нарушению костимулирующей функции в отношении В-лимфоцитов.
CD321
F11R (F11 Receptor). Белок суперсемейства иммуноглобулинов. Молекулярная масса 32-35 кДа. Участвует в трансмиграции мононуклеарных клеток через стенки сосудов в очаги воспаления. Локализуется в области межклеточного контакта покоящихся эндотелиальных клеток. При обработке основным фактором роста фибробластов (bFGF) перемещается на клеточную поверхность.
CD322
JAM2 (Junctional Adhesion Molecule 2). JAM2 локализуется в области тесного контакта между клетками высокого эндотелия в лимфоидных органах, где лимфоциты постоянно покидают кровоток (трансмиграция). Присутствует также на эндотелии артериол и вокруг воспалительных и опухолевых очагов. Действует как адгезивный лиганд для взаимодействия между многими иммунными клетками и может играть роль в хоминге лимфоцитов во вторичные лимфоидные органы.
CDH1 (Cadherin 1). Молекулярная масса 120 кДа. CD324 классическая молекула из суперсемейства кадгеринов. Лиганд - CD103. Е-кадгерин играет роль в развитии опухолей и их метастазировании. Мутации CDH1 гена коррелируют с раком желудка, молочной железы, толстой кишки, щитовидной железы, яичников и др. Снижение экспрессии и функции CDH1 делает вклад в прогрессирование рака, усиливая пролиферацию, инвазию и/или метастазирование. Распределение Е-кадгерина в клетках эмбриона человека зависит от стадии развития. Белок Vpr ВИЧ-1 повышает экспрессию кадгерина на клетках-мишенях. Адгезивные механизмы, опосредованные через Е-кадгерин, участвуют во взаимодействии сперматозоида с оболочкой яйцеклетки.
CD325
CDH2 (Cadherin 2, type 1). Молекулярная масса 140 кДа. N-кадгерин - трансмембранный гликопротеин. CD325 участвует в процессе гаструляции и нужен для установления левоправой асимметрии. В центральной нервной системе участвует в адгезии синапсов, пре- и постсинапсов. N-кадгерин усиливает клеточную подвижность и инвазивность, играет ключевую роль в миграции клеток меланомы через эндотелий сосудов, вовлекается в прогрессирование первичного рака толстой кишки, участвует в контроле выживаемости поверхностных эпителиальных клеток яичников человека.
CD326
TACSTD1 (Tumor-Associated Calcium Signal Transducer 1). Трансмембранный гликопротеин. Молекулярная масса 30-40 кДа. Ассоциирован с доброкачественной и опухолевой пролиферацией. Экспрессируется на поверхности большинства нормальных клеток аденоматозного и простого эпителия, клетках желудочно-кишечных карцином и вовлекается в гомофильную адгезию на базолатеральной мембране. CD326 рассматривают как мишень для иммунотерапии карцином человека.
CD327
SIGLEC6 (Sialic acid binding Ig-like Lectin 6). Член суперсемейства иммуноглобулинов (подсемейство сиалоадгезинов). Участвует в межклеточной адгезии. Экспрессирован на наружной мембране клеток и способен связывать расположенные на клетках-партнёрах сиаловые кислоты, входящие в состав гликопротеинов и гликолипидов. Имеет цитоплазматический тирозиновый ингибиторный мотив ITIM (Immunoglobulin receptorfamily Tyrosine-basedInhibitory Motif). Высокий уровень экспрессии
CD327 выявляют в цито- и синцитиотрофобластах плаценты человека. Умеренная экспрессия белка характерна в селезёнке, лейкоцитах периферической крови (почти исключительно на В-клетках) и клетках тонкой кишки. Участвует в регуляции сывороточного уровня лептина.
CD328
SIGLEC7 (Sialic acid binding Ig-like Lectin 7). Молекулярная масса 75 кДа. SIGLEC7 и SIGLEC9 являются связанными с CD33-ингибирующими рецепторами NK-клеток. SIGLEC7 как ингибирующий рецептор, связывающий сиаловые кислоты, экспрессируется NK-клетками (преимущественно), субпопуляциями периферических Т-клеток (CD8+ Т-клетки), моноцитами (слабо).
CD329
SIGLEC9 (Sialic acid binding Ig-like Lectin 9) (см. CD328). Молекулярная масса 50 кДа. Молекула адгезии. Играет роль ингибирующего рецептора за счёт наличия цитоплазматического тирозинового ингибиторного мотива ITIM. Связывание сиаловых кислот приводит к подавлению активности естественных киллеров, снижению передачи сигнала с Т-клеточного рецептора, а в случае нейтрофилов, находящихся в очаге воспаления, - к индукции апоптоза. В макрофагах связывание SIGLEC9 усиливает образование ИЛ-10 и понижает ФНОа. SIGLEC9 экспрессирован в больших количествах на моноцитах и нейтрофилах и в меньшей степени на естественных киллерах, Т- и В-лимфоцитах. Провоспалительные цитокины повышают уровень CD329 на нормальных нейтрофилах. У больных острым септическим шоком или ревматоидным артритом на нейтрофилах экспрессия SIGLEC9 повышена.
CD331
FGFR1 (Fibroblast Growth Factor Receptor 1). Молекулярная масса 130 кДа. CD331 - член семейства FGFR. Рецептор для факторов роста фибробластов (FGF). FGFR1 экспрессируется ранними предшественниками гемопоэтических и эндотелиальных клеток, а также субпопуляциями клеток эндотелия в сосудах опухолей. CD331 критичен для гемопоэза, но не ангиогенеза. Приблизительно 5% CD34+ клеток, выделенных из костного мозга, пуповинной крови и мобилизованных в периферической крови, экспрессируют FGFR1. Мутация гена, кодирующего CD331, приводит к развитию синдрома Пфейффера (острое доброкачественное вирусное заболевание с поражением лимфоидной ткани, генерализованное или регионарное увеличение лимфатических узлов).
FGFR2 (Fibroblast Growth Factor Receptor 2) (см. CD331). Молекулярная масса 115-135 кДа. FGFR2 - высокоаффинный рецептор для кислого и основного фактора роста фибробластов (FGF) и фактора роста кератиноцитов (KGF). Амплификация гена, кодирующего FGFR2, ассоциирована со многими типами опухолей. FGFR2 играет важную роль в регуляции передачи сигналов в остеобластах, участвуя в нормальной оссификации черепа у человека. Активация FGFR2 снижает присоединение остеобластов к фибронектину, приводит к индукции апоптоза остеобластов. Мутации гена СD332 ассоциированы со многими синдромами преждевременного заращения швов черепа и костной мальформации.
CD333
FGFR3 (Fibroblast Growth Factor Receptor 3) (см. CD331). Молекулярная масса 115-135 кДа. Член семейства FGFR. Связывает кислый и основной фактор роста фибробластов, участвует в развитии и сохранении костной ткани. Мутации гена CD333 приводят к преждевременному сращению швов черепа, разнообразным типам костной дисплазии (ахондроплазии и танатофорической дисплазии). Мутация гена, кодирующего FGFR3, влияет на развитие, но не на прогрессирование рака мочевого пузыря. Повышенная экспрессия FGFR3 может играть важную канцерогенную роль в печени.
CD334
FGFR4 (см. CD331). Молекулярная масса 110 кДа. Взаимодействует преимущественно с кислым фактором роста фибробластов (FGF). Повышена экспрессия на опухолях женской половой сферы. Участвует в развитии рака молочной железы и яичников. Аллель Arg388 гена, кодирующего FGFR4, ассоциирован с повышением частоты и клинической агрессивности рака простаты.
CD335
NCR1 (Natural Cytotoxicity triggering Receptor 1). Молекулярная масса 46 кДа. Член семейства рецепторов естественной цитотоксичности (NCR). Экспрессируются почти исключительно NK-клетками и выполняют функцию главных активирующих рецепторов. Плотность NCR на NK-клетках коррелирует с цитолитической активностью против опухолевых клеток. Связывание NCR с предполагаемым лигандом опухолевых клеток может запускать апоптоз NK-лимфоцитов. NKp46рецепторы участвуют в клеточно-опосредованном лизисе клеток, инфицированных внутриклеточными патогенами. Ослабление этой функции ассоциируется с тяжёлыми проявлениями инфекционных заболеваний.
CD336
NCR2 (Natural Cytotoxicity triggering Receptor 2) (см. CD335). Молекулярная масса 44 кДа. Член семейства рецепторов естественной цитотоксичности (NCR), важных для распознавания опухолевых клеток-мишеней. Экспрессируется только на активированных NK-клетках человека. CD336 существенен не только для противоопухолевой защиты, но и участвует в «самоубийстве» NK-клеток.
CD337
NCR3 (Natural Cytotoxicity triggering Receptor 3) (см. CD335). Молекулярная масса 30 кДа. Экспрессируется на субпопуляции NK-клеток периферической крови человека и вовлекается в киллинг опухолевых клеток NK-лимфоцитами. Участвует в запуске активации NK-клеток при взаимодействии со стромальными клетками костного мозга in vitro. Опосредованная через NK-клетки индукция созревания ДК зависит от CD337. Уровень CD337 в крови и синовиальной жидкости возрастает у больных ревматоидным артритом и коррелирует с тяжестью воспалительного процесса в синовии.
CD338
ABCG2 [ATP-Binding Cassette, sub-family G (WHITE), member 2]. Мембранный белок суперсемейства транспортёров АТФ-связывающих кассет (АВС - ATP-binding cassette). Молекулярная масса 72 кДа. CD338 экспрессируется в большом количестве на синцитиотрофобластах плаценты, на апикальной мембране эпителия тонкой кишки, на мембране канальцев печени и на клетках эндотелия микрососудов мозга человека. CD338 экспрессируется и функционирует как транспортёр в мозге; выявлен на многих стволовых клетках и может защищать их от экзогенных и эндогенных токсинов; защищает развивающийся плод от воздействия потенциально токсичных ксенобиотиков. Повышенная экспрессия CD338 ассоциируется с высокими уровнями устойчивости ко многим противораковым агентам, включая антрациклины, митоксантрон и камптотехины, повышая выведение лекарственных средств. Взаимодействует с гемом и другими порфиринами, защищает клетки и/или ткани от накопления протопорфирина при гипоксии.
CD339
JAG1 [ Jagged 1 (Alagille syndrome)]. «Зазубренный» белок типа 1 (JAG1). Аналог соответствующего белка дрозофил. Трансмембранный белковый лиганд для эволюционно консервативного Notch1 рецептора. Молекулярная масса 150 кДа. JAG1 играет важную роль в гемопоэзе. Микроделеция гена JAG1 (20p12) приводит к развитию синдрома Алажиля (артериопечёночная дисплазия, синдром Алажиля-Ватсона) - генетического заболевания, наследуемого по аутосомно-доминантному типу. • Семейство Notch гетеродимерных трансмембранных белков играет интегральную роль в судьбе клеток, положительно или отрицательно влияя на пролиферацию, дифференцировку и апоптоз. У человека выявлены 4 Notch-рецептора - Notch1, Notch2, Notch3 и Notch4. Notch1 состоит из внеклеточного домена с 36 повторами, подобными эпидермальному фактору роста, одного трансмембранного домена и внутриклеточного домена, состоящего из молекулы, ассоциированной с RBP-JK, акрилиновых доменов и региона, обогащенного последовательностью пролин-глютаматсерин-треонин. Известно несколько лигандов Notch-рецепторов: Delta-1, Delta-2, Delta-3, Delta-4, гомологичные Delta дрозофил, и Jagged-1, Jagged-2, гомологичные Serrate дрозофил. При связывании лигандами Notch-рецепторы протеолитически расщепляются, при этом освобождается внутриклеточный домен Notch (NICD), который перемещается в ядро и активирует гены-мишени. Notch-рецепторы, экспрессируемые на гемопоэтических стволовых клетках, взаимодействуют с лигандами на костномозговых стромальных клетках и контролируют развитие и дифференцировку Т-лимфоцитов. Дефицит и мутации Notch-рецепторов и лигандов приводят к тяжёлым дефектам внутриутробного развития мышей. Notch-рецепторы и их лиганд JAG1 с высокой частотой присутствуют на культивируемых и первичных клетках множественной миеломы и глиомы человека. Мутация гена Jag1 приводит к развитию аутосомнодоминантного синдрома Алажиля, характеризующегося пятью главными симптомами: холестазом, деформацией позвоночника, дефектами сердца, глаз и лица, а также хронической почечной недостаточностью и гипертензией.
CD340
ERBB2 (v-erb-b2 erythroblastic leukemia viral oncogene homolog 22). Член тирозинкиназного семейства рецепторов типа III. Повышенную экспрессию CD340 выявляют при многих формах рака, включая рак молочной железы и яичника. Она коррелирует с плохим прогнозом. CD340 рассматривают как биомаркёр и мишень для иммунотерапии рака.
FZD4 [Frizzled homolog 4 (Drosophila)]. Аналог соответствующего белка дрозофилы (D. melanogaster). Относится к семейству (FZD1-10) белка «завивки» (frizzled). Большинство рецепторов frizzled соединены с β-катениновым сигнальным путём. FZD4 играет важную роль в ангиогенезе сетчатки. Мутации в N- или C-концевых регионах FZD4 ассоциируются с семейной аутосомно-доминантной экссудативной витреоретинопатией.
CD349
FZD9 [Frizzled homolog 9 (Drosophila)]. Экспрессируется в мозге, в частности в гиппокампе. CD349 также выявлен в клетках рака желудка. В астроцитомах человека FZD9 присутствует в микрососудах и опухолевых клетках. FZD9 - один из маркёров мезенхимальных стволовых клеток, происходящих из костного мозга.
CD350
FZD10 (см. CD344). Большое количество мРНК FZD10 обнаружено в плаценте и тканях эмбриона: почках, лёгких и мозге. В мозге взрослых в большом количестве представлен в мозжечке. Обильно экспрессируется в культивируемых опухолевых клетках (рака шейки матки, толстой кишки и др.). FZD10 имеет 65,7% аминокислотную гомологию с FZD9. Усиление регуляции мРНК FZD10 в некоторых типах клеток человека может привести к канцерогенезу через активацию p-катенинового сигнального пути.
CD351-CD400
[править]CD351
FCAMR, высокоаффинный Fc-рецептор к IgA, IgM. (+) - Т-и В-клетки, макрофаги/моноциты.
CD352
SLAMF6, Ly108, NTB-A. Трансмембранный белок суперсемейства иммуноглобулинов, принадлежащий к подсемейству CD2. Участвует в активации NK-клеток. (+) - дендритные, Т-, В-, NK-клетки, макрофаги/моноциты, гранулоциты.
CD353
SLAMF8, BLAME. Присутствует на В-клетках и на макрофагах/моноцитах. Играет роль в дифференцировке В-лимфоцитов и модуляции сигнала с BCR.
TREM1. Поверхностный рецептор, активация которого вызывает выброс клетками провоспалительных хемокинов и цитокинов. (+) - дендритные, Т-, В-, NK-клетки, макрофаги/моноциты, гранулоциты.
CD355
CRTAM, цитотоксическая и регуляторная молекула Т-клетки. Взаимодействие с CADM1 приводит к усилению цитотоксичности и увеличению секреции ИФНγ (+) -Т-, В-, NK-клетки.
CD357
TNFRSF18, 18-й член суперсемейства рецепторов ФНО, GITR. Вовлечен во взаимодействия между активированными Т-лимфоцитами и эндотелиальными клетками. Участвует в активации NF-kB. (+) - дендритные, Т-, В-, NK-клетки, макрофаги/моноциты.
CD358
TNFRSF21, 21-й член суперсемейства рецепторов ФНО, рецептор DR6 (от Death Receptor). Лигандом служит N-APP. Участвует в активации NF-kB и индукции апоптоза. (+) - Т-, В-клетки, макрофаги/моноциты.
CD359
PI16. Ингибитор сериновых протеаз. Присутствует на Т-клетках.
CD360
IL21R. Гетеромеризуется с общей y-субъединицей рецепторов интерлейкинов (CD132), (+) - дендритные, Т-, В-, NK-клетки, макрофаги/ моноциты, гранулоциты.
CD361
EVI2B - сайт эктопической вирусной интеграции 2B. (+) - Т-, В-клетки, макрофаги/моноциты, гранулоциты.
CD362
Syndecan-2. Поверхностный протеогликан, содержащий гепарансульфат. Играет роль в регуляции пролиферации и адгезии. (+) - Т-, В-клетки, макрофаги/моноциты, гранулоциты, кератиноциты.
CD363
S1PR1, сфингозин-1-фосфатный рецептор 1. Рецепторы этого семейства передают сигнал внутрь клетки через G-белки. Активация этого рецептора вызывает адгезию клеток. (+) - Т-, В-, NK-клетки, эндотелий.


